对抗知识焦虑,从看懂这条开始
App 下载
肠道里的抗炎卫士:酪酸梭菌如何守护肠健康
丁酸菌|肠漏|肠道菌群|炎症性肠病|酪酸梭菌|感染性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
丁酸菌|肠漏|肠道菌群|炎症性肠病|酪酸梭菌|感染性疾病|医学健康
你有没有过这样的经历:吃了一顿重口火锅后,肚子绞痛、腹泻不止,甚至便血?这可能不只是普通的肠胃不适——炎症性肠病(IBD)正以惊人的速度在全球蔓延,仅中国患者就超300万。这种慢性肠道炎症反复发作,不仅让患者长期受腹痛、腹泻困扰,还可能引发肠癌等致命并发症。更棘手的是,现有药物的有效率不足50%,且长期使用副作用明显。直到科学家把目光投向肠道里一种不起眼的细菌——酪酸梭菌,才发现它可能是破解IBD难题的关键钥匙。
炎症性肠病的核心问题,其实是肠道里的“生态灾难”。健康人的肠道里,住着上千种细菌,其中产丁酸的菌群是维持肠道稳定的“基石”——它们能发酵膳食纤维产生丁酸,这是肠上皮细胞的主要能量来源,就像给肠道黏膜“充电”,让细胞紧密排列,形成一道坚固的屏障,阻止细菌、毒素等有害物质进入血液(也就是俗称的“肠漏”)。
但IBD患者的肠道里,这种产丁酸的菌群数量骤降,尤其是酪酸梭菌这类核心菌株几乎消失。没有了丁酸的滋养,肠上皮细胞失去能量,紧密连接蛋白像松动的砖块一样脱落,肠道屏障出现漏洞。与此同时,致病菌趁机大量繁殖,释放炎症因子,免疫系统被过度激活,陷入“炎症-屏障破坏-更严重炎症”的恶性循环。
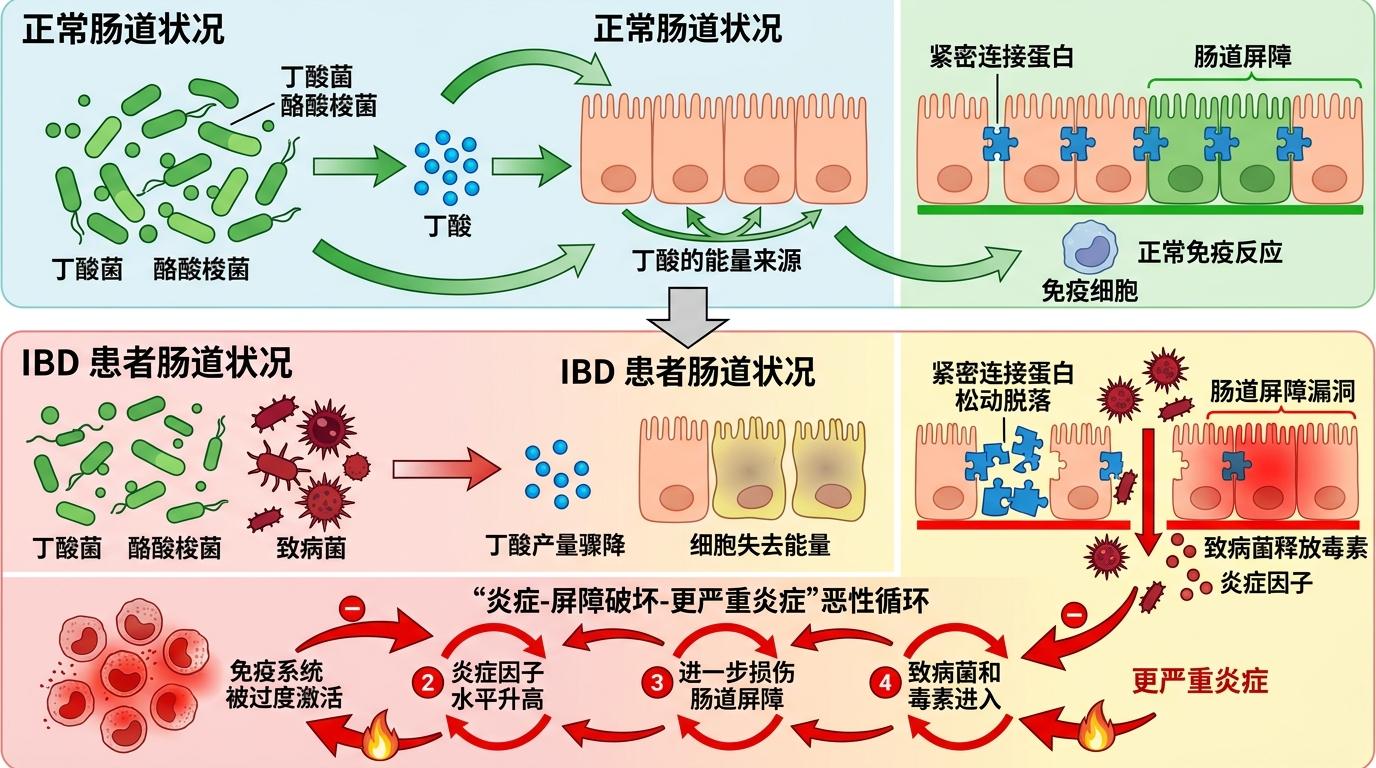
更关键的是,丁酸不仅能修复肠屏障,还能调节免疫:它能促进抗炎的调节性T细胞(Treg)分化,抑制促炎的Th17细胞,就像给免疫系统安装了“刹车”,防止它过度攻击肠道自身组织。
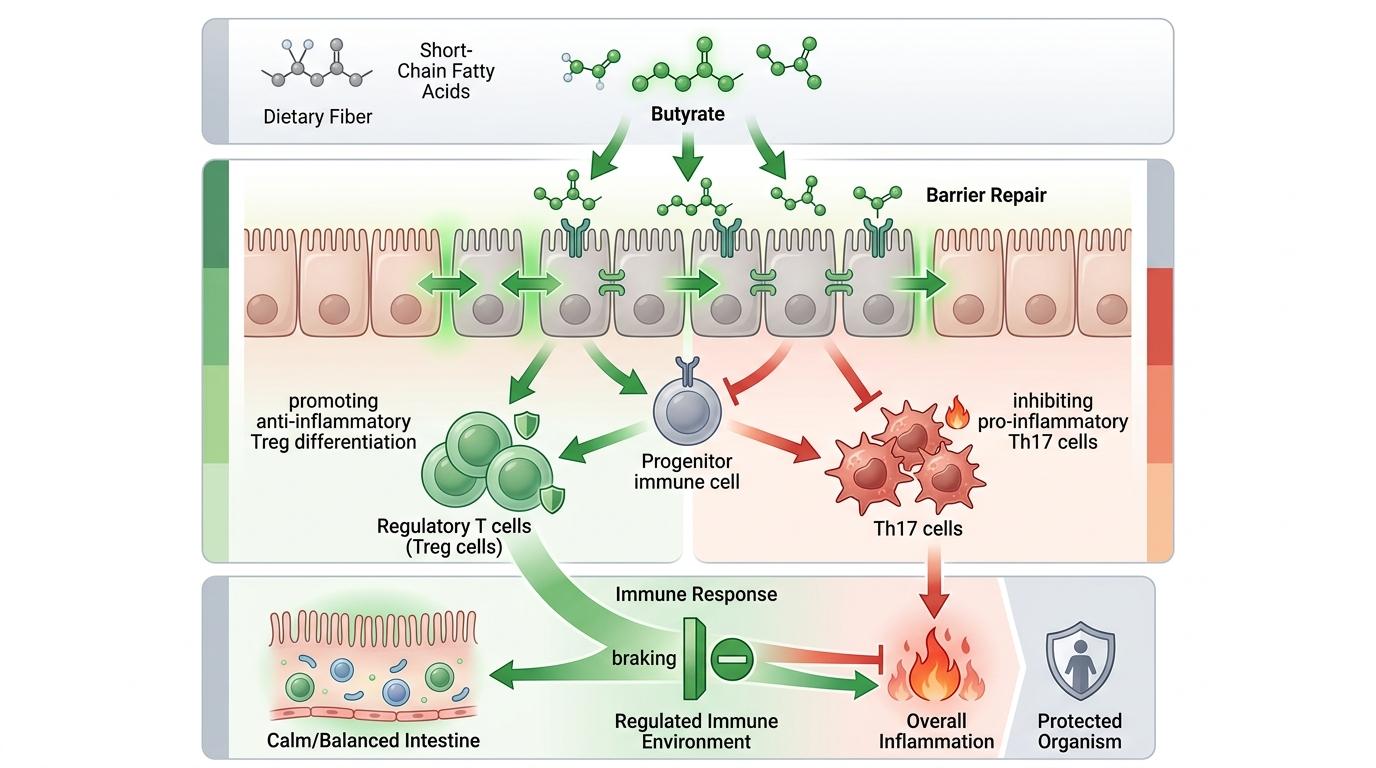
酪酸梭菌之所以能成为IBD的“克星”,靠的是三重协同作用的分子机制:
第一重是“补能修复”。它能高效发酵膳食纤维产生丁酸,直接给肠上皮细胞供能,促进紧密连接蛋白(如ZO-1、occludin)的表达,快速填补肠道屏障的漏洞。在动物实验中,补充酪酸梭菌的结肠炎小鼠,结肠长度恢复了30%-40%,炎症因子水平下降了60%-80%。
第二重是“菌群调控”。酪酸梭菌能降低肠道pH值,抑制大肠杆菌、沙门氏菌等致病菌的生长,同时促进双歧杆菌、 Akkermansia等有益菌的繁殖,重新构建健康的肠道菌群平衡。它还能通过“交叉喂养”机制,给其他产丁酸菌提供代谢原料,形成产丁酸的“连锁反应”。
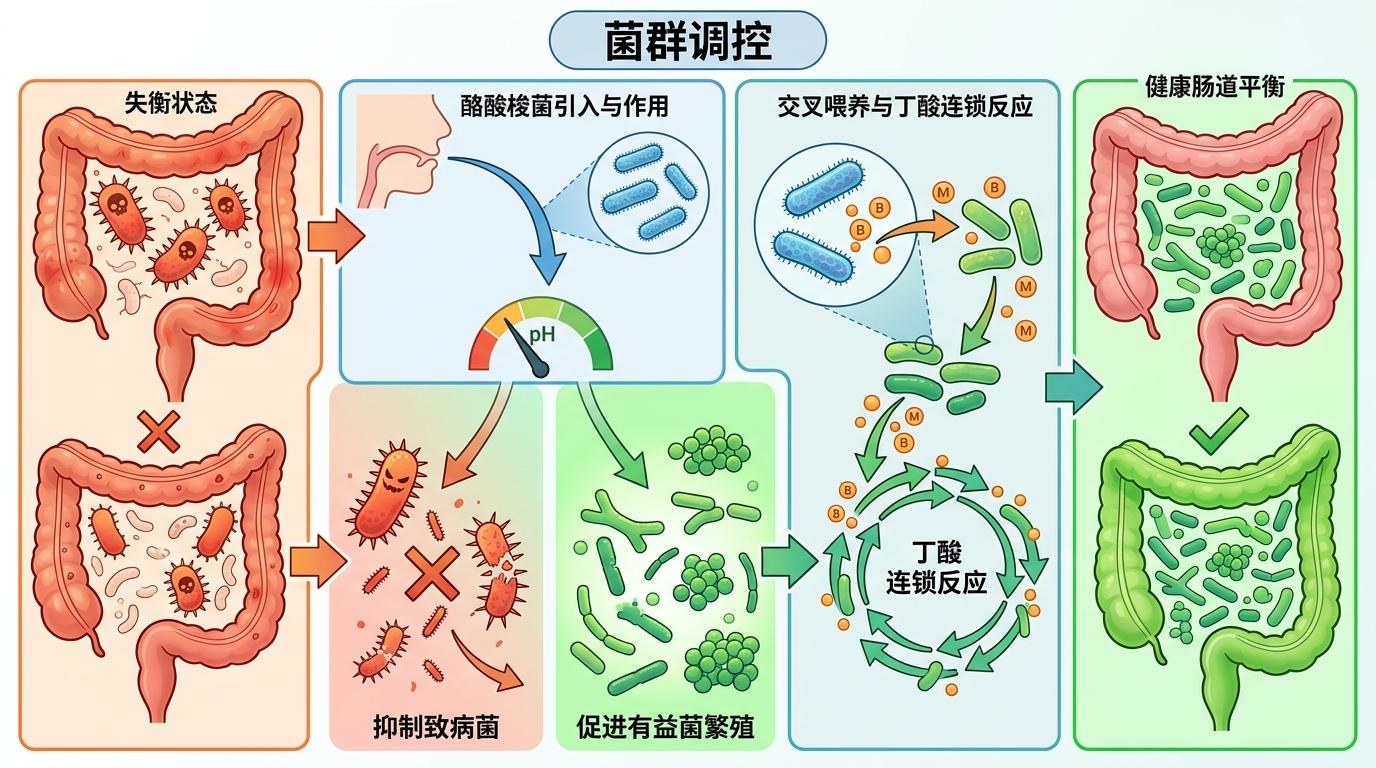
第三重是“免疫调节”。它能通过TLR2/MyD88信号通路激活巨噬细胞,促使其分泌抗炎因子IL-10;同时,它产生的丁酸能作为组蛋白去乙酰化酶抑制剂,调节免疫细胞的基因表达,从根源上抑制炎症反应。
值得注意的是,酪酸梭菌的芽孢结构能耐受胃酸和胆汁的侵蚀,活着到达结肠发挥作用,这是很多益生菌不具备的优势。
动物实验的成功,让酪酸梭菌很快走进了临床。研究显示,在常规药物治疗基础上联合酪酸梭菌,能将溃疡性结肠炎的临床缓解率提高20%以上,还能有效预防术后并发症贮袋炎。更重要的是,它的安全性良好,即使是儿童和免疫低下患者也能耐受,仅极少数病例报告了菌血症风险。
但目前的研究仍存在一些局限:首先,菌株的选择、剂量和疗程尚无统一标准,不同菌株的疗效差异较大;其次,个体肠道菌群的差异导致治疗反应不一,部分患者可能效果不佳;最后,长期使用的安全性还需要大规模临床试验验证。
为了克服这些问题,科学家正在探索“后生元”疗法——也就是使用酪酸梭菌的代谢产物(如丁酸、胞外囊泡),既能发挥抗炎作用,又能避免活菌定植的不确定性。同时,结合AI技术的个性化微生态调控策略也在发展,未来可以根据患者的菌群特征定制治疗方案。
当我们把目光从复杂的药物分子转向肠道里的微小细菌时,才发现健康的秘密可能就藏在这些不起眼的“原住民”身上。酪酸梭菌的发现,不仅为IBD治疗提供了新方向,更让我们意识到:肠道不是一个孤立的消化器官,而是一个由菌群、黏膜和免疫系统组成的复杂生态系统。
“肠道健康的核心,是菌群的平衡。”这句话不仅适用于IBD,也适用于肥胖、糖尿病甚至神经退行性疾病等多种慢性疾病。未来,随着微生态医学的发展,我们或许能通过调节肠道菌群,从根源上预防和治疗这些疾病。而酪酸梭菌,就是这个领域里一颗正在发光的“明星”。