对抗知识焦虑,从看懂这条开始
App 下载
微生物信号触发细胞绕路送蛋白强化屏障
防御蛋白|肠上皮细胞|细菌信号分子|应急蛋白运输通道|华中科技大学林珑团队|分子细胞生物学|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
防御蛋白|肠上皮细胞|细菌信号分子|应急蛋白运输通道|华中科技大学林珑团队|分子细胞生物学|生命科学
当肠道遭遇细菌入侵,你的肠上皮细胞需要在几分钟内把防御蛋白送到最前线——这比快递小哥的急件配送还要紧迫。传统的蛋白运输路线要经过内质网、高尔基体层层审批,根本赶不上应急需求。2026年,华中科技大学林珑团队在《Autophagy》杂志上公布了一个惊人发现:细胞里藏着一条「应急绿色通道」,能绕过高尔基体直接把关键防御蛋白送到细胞膜,而启动这条通道的开关,居然是细菌分泌的信号分子。这到底是一条怎样的秘密通道?它又是如何被微生物精准触发的?
你可以把细胞的蛋白运输系统想象成一个物流网络:内质网是工厂,高尔基体是分拣中心,要把新生产的蛋白打包、贴标签再送到细胞膜。但遇到紧急情况,比如细菌入侵,等新蛋白生产、分拣再配送,早就来不及了。
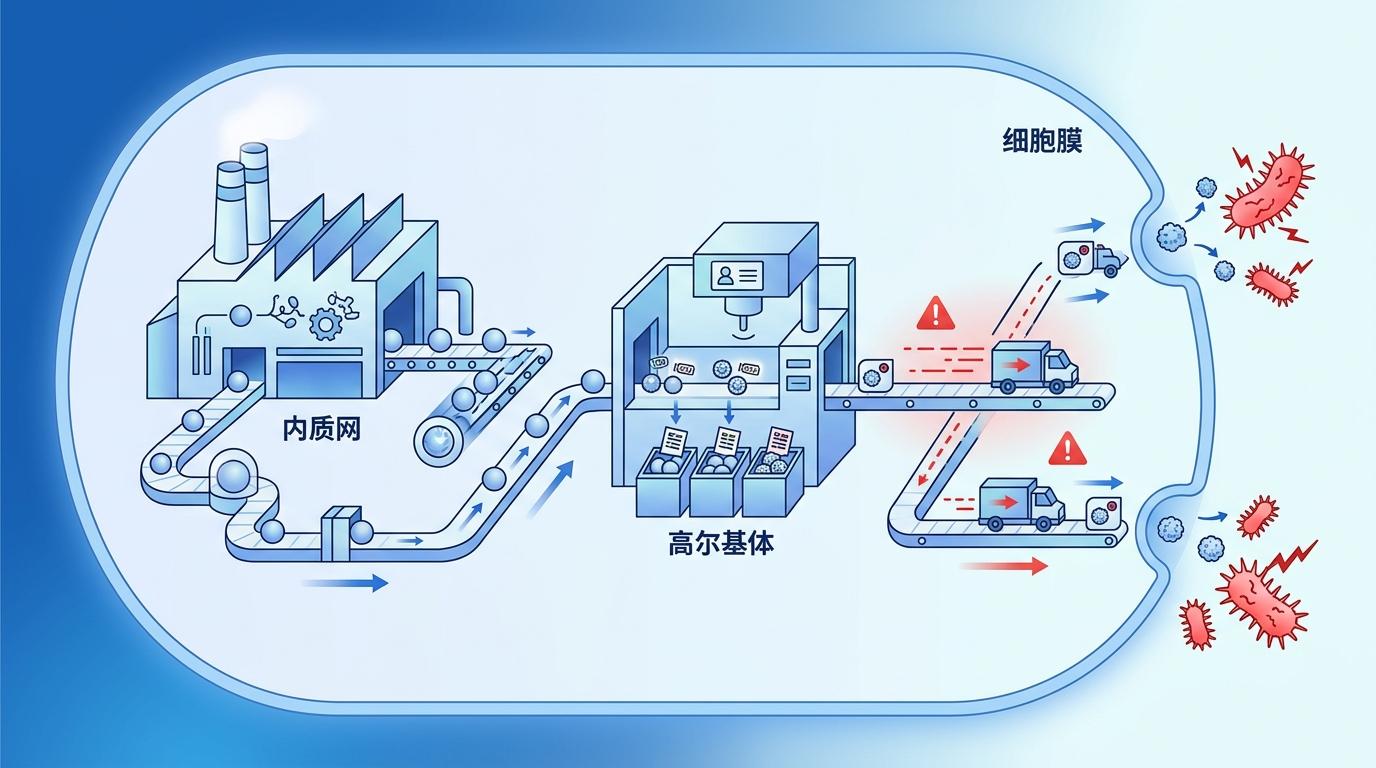
林珑团队发现的这条名为LACES(LC3/Atg8相关载体胞吐作用)的通道,走的是完全不同的逻辑——它不生产新蛋白,而是调动细胞里已经备好的「库存」。在秀丽隐杆线虫的肠道里,细菌分泌的吩嗪-1-甲酰胺(PCN)会触发内质网-高尔基体中间区的一个亚结构,让一种叫VPS-34的酶生成信号分子PtdIns3P,这种分子会给预先存在的单膜RAB-8载体贴上「应急配送」的标签——也就是Atg8化修饰。
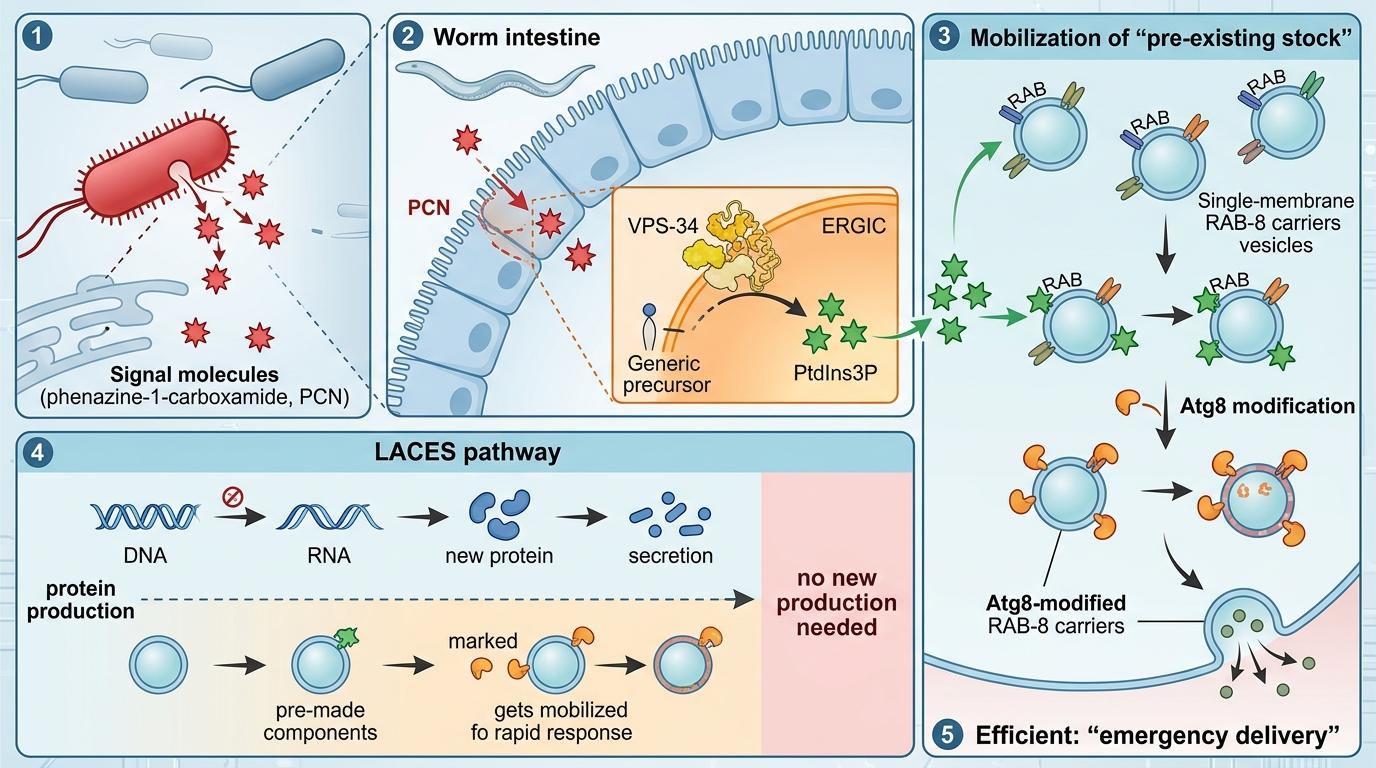
被标记的RAB-8载体立刻带着ABC转运蛋白PGP-1出发,直接送到肠上皮细胞的顶端膜,全程绕过高尔基体。实验数据显示,这条通道能让PGP-1的递送速度大幅提升,线虫在感染后的存活率明显提高。更关键的是,它完全不依赖经典的自噬启动模块、未折叠蛋白反应这些已知的细胞应急机制——这是一条全新的、专门为应对微生物入侵设计的快速通道。
这条应急通道不是线虫的专属。研究团队在哺乳动物细胞里也验证了它的存在:在PCN的作用下,人类结肠癌细胞系Caco-2的囊泡中,一种叫ΔF508-CFTR的突变蛋白被快速递送到顶膜,而且功能得到了改善——这种蛋白正是囊性纤维化患者体内缺失功能的关键蛋白。小鼠肠上皮细胞中,LC3和RAB8的交互作用也明显增强,证明这条通道在哺乳动物中同样有效。
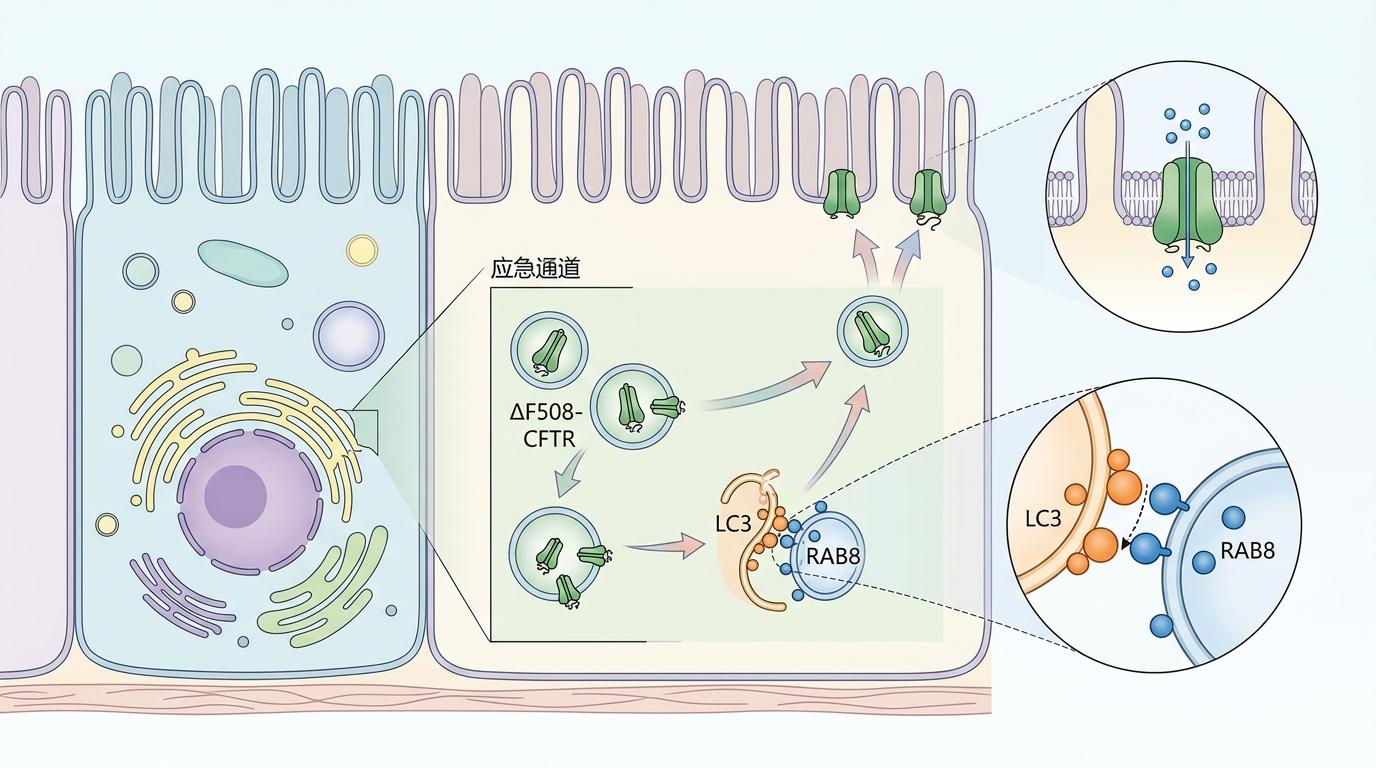
有意思的是,LACES通道和我们熟知的自噬系统既有关联又有区别:它用到了自噬相关的LC3蛋白,但不是用来降解细胞垃圾,而是给运输载体贴标签;它不需要自噬启动的核心模块,却依赖特定的磷脂信号和单膜载体。这就好比你平时用快递寄垃圾(自噬),但遇到紧急情况,直接用家里的备用快递袋(预先存在的RAB-8载体)装着应急物资就出门了,连快递站(高尔基体)都不用去。
不过这条通道也不是万能的。目前的研究只证实它能被多种胞外细菌激活,但具体还有哪些信号能触发它,不同细胞类型里的运作细节有什么差异,还需要进一步探索。而且它的「库存」毕竟有限,只能应对短期的紧急防御,长期的屏障强化还是需要依赖传统的蛋白合成路线。
LACES通道的发现,不仅刷新了我们对细胞膜运输的认知,还为疾病治疗提供了新的靶点。比如囊性纤维化患者,他们体内的ΔF508-CFTR蛋白因为折叠错误,大多被细胞降解了,只有少数能到达细胞膜。如果能通过触发LACES通道,把这些「半成品」蛋白直接送到细胞膜,就能改善患者的症状。
研究团队已经在细胞实验里看到了初步效果:PCN处理能让ΔF508-CFTR的顶膜递送增加,并且功能得到改善。这意味着未来可能开发出专门触发LACES通道的药物,不用纠正蛋白的折叠错误,直接绕开这个难题,把蛋白送到该去的地方。
当然,这一切还处于基础研究阶段。要把实验室里的发现转化为临床治疗,还要解决很多问题:比如如何特异性地触发肠道上皮细胞的LACES通道,而不影响其他细胞;如何控制通道的激活时间,避免过度激活带来的副作用。但至少,我们已经找到了一个新的方向——原来细胞应对感染的策略,比我们想象的要聪明得多。
当我们把目光聚焦在细胞的微观世界,会发现生命的防御机制远比我们想象的精妙。LACES通道的存在,说明细胞在漫长的进化中,早就为微生物入侵准备好了「应急预案」——不是从头搭建生产线,而是优化现有的运输网络,用最快的速度把防御物资送到前线。
微生物和宿主的博弈,从来都是一场军备竞赛。细菌在进化出各种入侵手段的同时,宿主也在不断升级自己的防御系统。LACES通道的发现,只是这场竞赛中我们看到的一个小片段。
**应急的本质,是对存量的精准调用。**未来,当我们能更深入地理解这些微观世界的应急策略,或许就能为人类的健康防护,找到更高效的解决方案。