1 天前

1 天前
当5.89亿糖尿病患者等待着能替代自身受损胰岛的「救命细胞」时,干细胞来源的类胰岛器官——也就是从干细胞分化来的、模拟真实胰岛功能的细胞团——却卡在了最后一步:移植后超过一半的细胞会在一周内死亡。不是因为免疫排斥,也不是因为细胞没长好,而是因为它们「缺氧窒息」,还不会自己喊「救命」。
同济大学和云南省第一人民医院的团队最近找到了解法:给这些细胞提前「断锌」。这个听起来简单的操作,居然让移植后的细胞存活率翻了倍,还能自己召唤血管来供氧。这背后,藏着一个被忽略了几十年的细胞生存密码。
你可以把胰岛移植想象成给沙漠里的植物浇水——刚种下去的前几天,根还没扎进土里,全靠自身储存的水分活着。对于移植的类胰岛细胞来说,「根」就是血管:原来的血管连接被切断后,新血管要7到14天才能长出来,这期间细胞只能在缺氧环境里挣扎。
正常细胞遇到缺氧会启动自救:缺氧诱导因子HIF1α会稳定下来,指挥细胞分泌血管内皮生长因子VEGFA——相当于细胞喊「快给我送氧来」,召唤血管生成。但胰岛β细胞是个例外,它们天生「代谢脆弱」:靠燃烧氧气产生胰岛素,耗氧速度是其他细胞的好几倍,缺氧时最先撑不住,连喊救命的力气都没有。
研究人员发现,问题出在锌离子上。β细胞里的锌含量是其他细胞的几十倍,用来帮助胰岛素结晶储存,但缺氧时这些锌会跑出来「捣乱」:过量的锌会引发氧化应激,直接抑制细胞里的能量传感器AMPK的活性。没有AMPK,细胞既没法成熟,也没法抵抗缺氧,更别说分泌VEGFA召唤血管了。
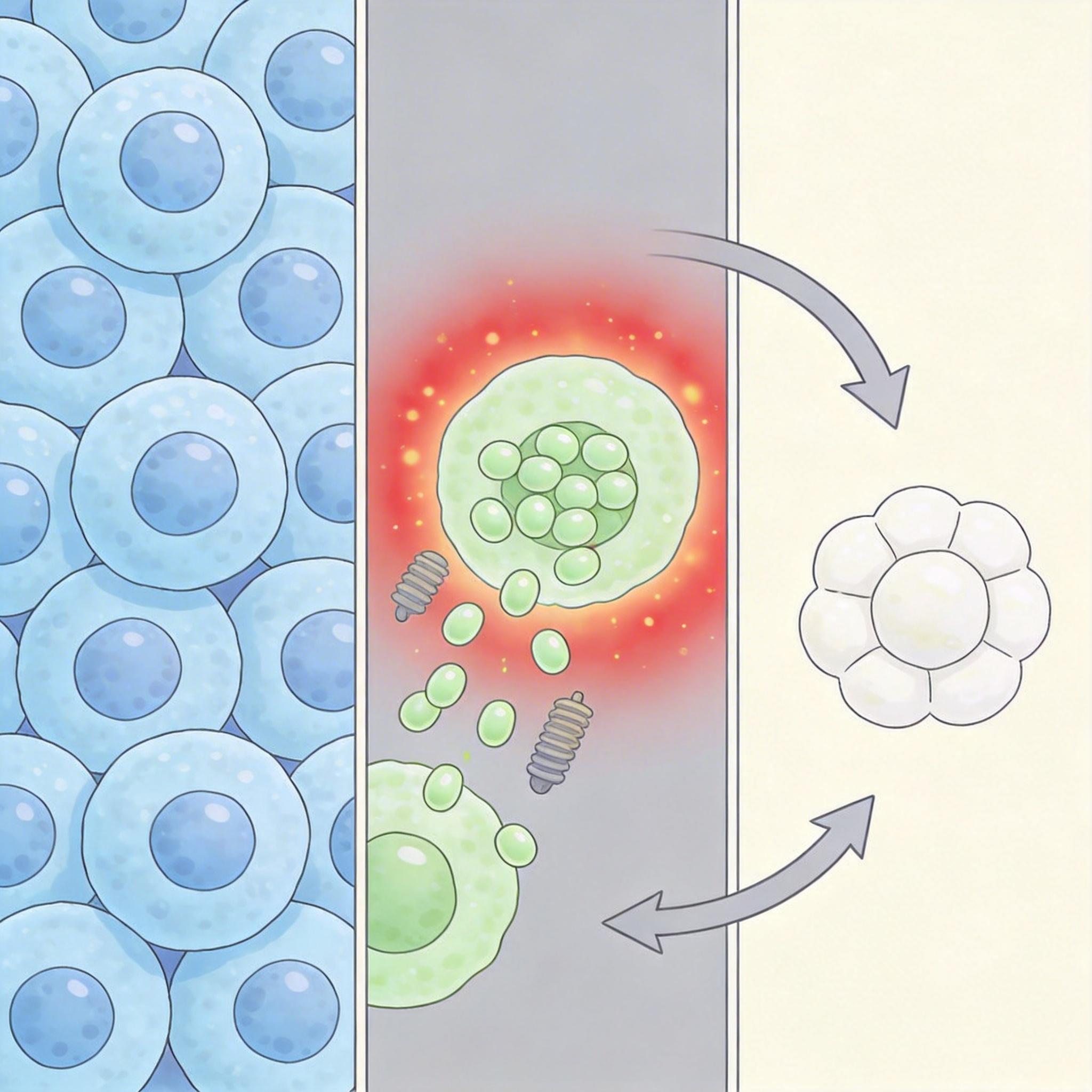
研究团队的解法直接又粗暴:用化学药物抑制锌转运蛋白ZnT8,不让锌跑到细胞里「添乱」。这个操作相当于给细胞装了个「自救开关」:
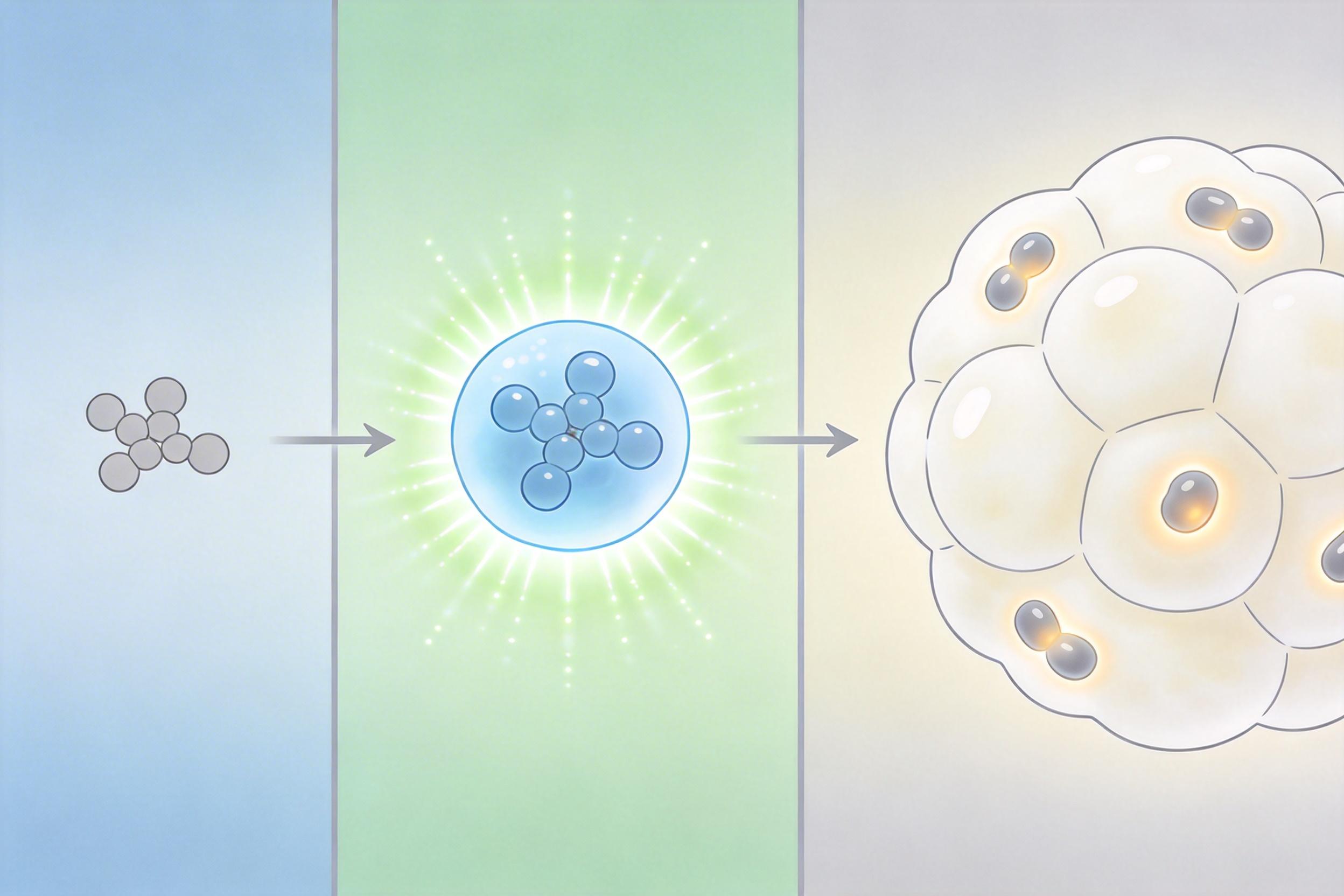
在糖尿病小鼠模型里,经过「断锌」预处理的类胰岛细胞,移植后血管生成速度快了3倍,血糖控制能力提升了40%,存活率从不到50%直接涨到了90%以上。更关键的是,这个方法对人类原代胰岛细胞同样有效——意味着它离临床应用又近了一步。
不过也得提一句,这可不是让糖尿病患者去吃锌补充剂或者锌抑制剂。细胞里的锌平衡就像走钢丝:少了会影响胰岛素储存,多了会害死细胞,必须精准调控移植前的细胞状态。
这个发现给干细胞治疗糖尿病打开了一扇新门,但要真正用到患者身上,还有三道关要过:
第一关是标准化:怎么把「断锌」的剂量和时间精确控制到每一批细胞里?毕竟多一点可能细胞活不了,少一点又没效果,工业化生产容不得半点误差。
第二关是安全性:长期抑制锌转运蛋白会不会有副作用?比如影响其他细胞的锌平衡?虽然动物实验里没发现问题,但人体的情况要复杂得多。
第三关是成本:目前干细胞类胰岛细胞的制备成本还很高,加上「断锌」的预处理步骤,会不会让治疗费用高到普通人用不起?不过好在这个方法用的是便宜的化学药物,不像基因编辑那样需要昂贵的设备,未来大规模生产后成本应该能降下来。
更值得关注的是,这个研究其实给了我们一个新的思路:有时候不用费劲改造细胞本身,只要调整细胞里的「微量元素平衡」,就能解决大问题。就像给一辆抛锚的车换个火花塞,不用换发动机就能重新跑起来。
当我们盯着干细胞分化的复杂步骤、盯着免疫排斥的难题时,却忽略了细胞里那些不起眼的微量元素——比如锌——居然是决定移植成败的关键。这就像我们总在找复杂的解决方案,却忘了问题的答案可能就在最基础的细胞代谢里。
「精准调控代谢,比改造基因更直接」,这句话不仅适用于胰岛移植,也适用于很多其他疾病的治疗。未来的再生医学,或许不是靠创造完美的细胞,而是靠理解细胞最本质的生存需求,给它们搭好活下去的台阶。
对于那5.89亿糖尿病患者来说,这可能不是终点,但至少是一个看得见希望的新起点。
点击催更,成为大圆镜下一个视频选题!