对抗知识焦虑,从看懂这条开始
App 下载
结节病新靶点:LGMN按下免疫炎症刹车
肺纤维化|泼尼松|巨噬细胞|LGMN分子|结节病|自身免疫疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
肺纤维化|泼尼松|巨噬细胞|LGMN分子|结节病|自身免疫疾病|医学健康
当你持续咳嗽、胸闷却查不出感染,淋巴结莫名肿大,可能正遭遇一种「会伪装的免疫病」——结节病。这种病因不明的肉芽肿性疾病,全球数百万患者受其困扰:三分之二能侥幸缓解,剩下三分之一却会发展为肺纤维化,最终因呼吸衰竭离世。目前唯一靠谱的一线药是泼尼松,可长期吃会引发糖尿病、骨质疏松,减药还容易复发。现在,中日友好医院和中国医学科学院的团队,找到了能给这种失控免疫反应「踩刹车」的关键分子——LGMN。
要理解LGMN的作用,得先认识结节病的「罪魁祸首」——巨噬细胞。这种免疫细胞像个「变形金刚」,能在两种状态间切换:M1型是「战斗狂」,会疯狂分泌促炎因子,引发免疫风暴;M2型是「和平派」,负责抗炎修复。
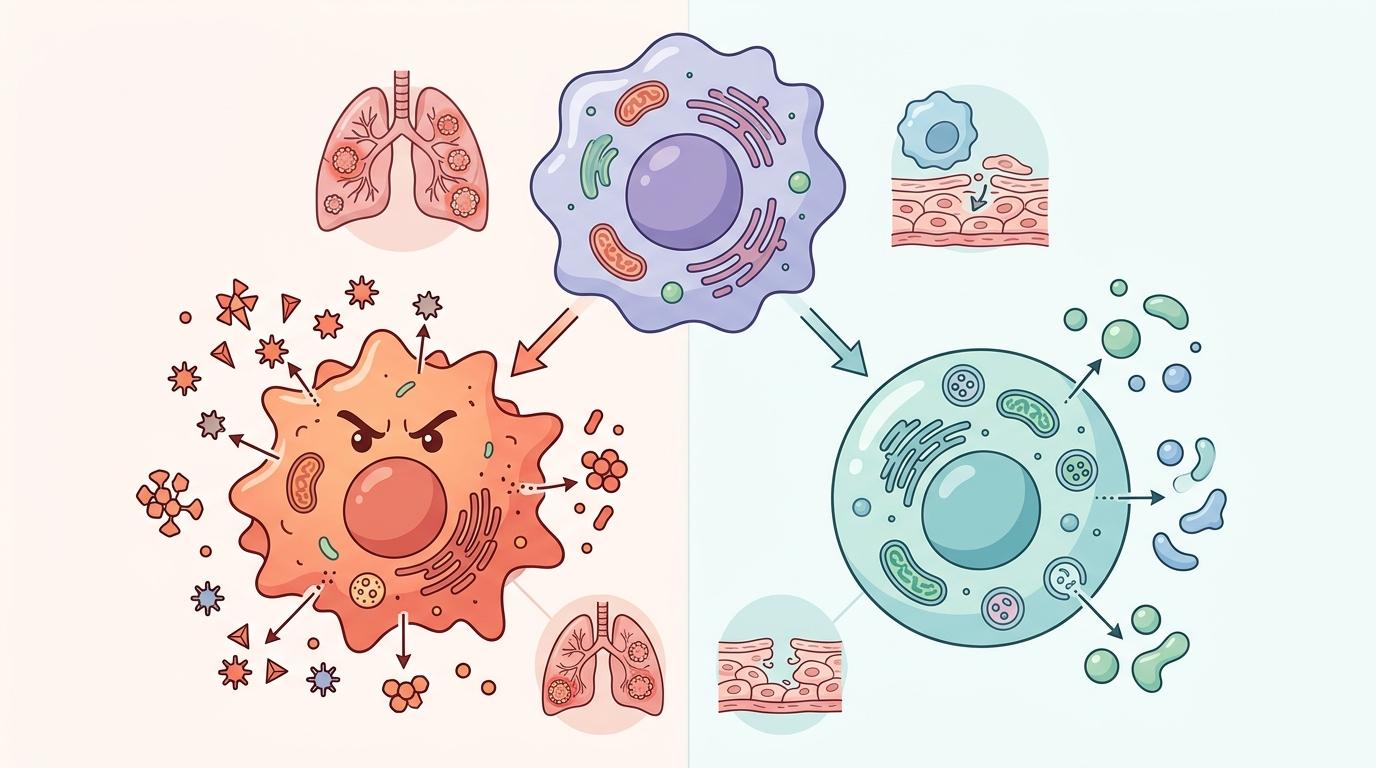
在结节病患者的肉芽肿里,M1型巨噬细胞占了上风,它们像失控的施工队,不断堆积炎症物质形成肉芽肿,啃噬肺部组织。而研究团队发现,患者肉芽肿里的LGMN蛋白含量明显升高——这不是巧合,更像是身体在本能地启动自我保护。
为了验证这个猜想,他们做了个「反向实验」:把小鼠的Lgmn基因敲除,再用痤疮丙酸杆菌诱导出结节病模型。结果不出所料,小鼠肺部的肉芽肿直接「疯长」,M1型巨噬细胞的数量比正常小鼠翻了好几倍,炎症因子浓度飙升。
LGMN到底是怎么给免疫反应踩刹车的?研究团队拆解出了完整的分子链条:
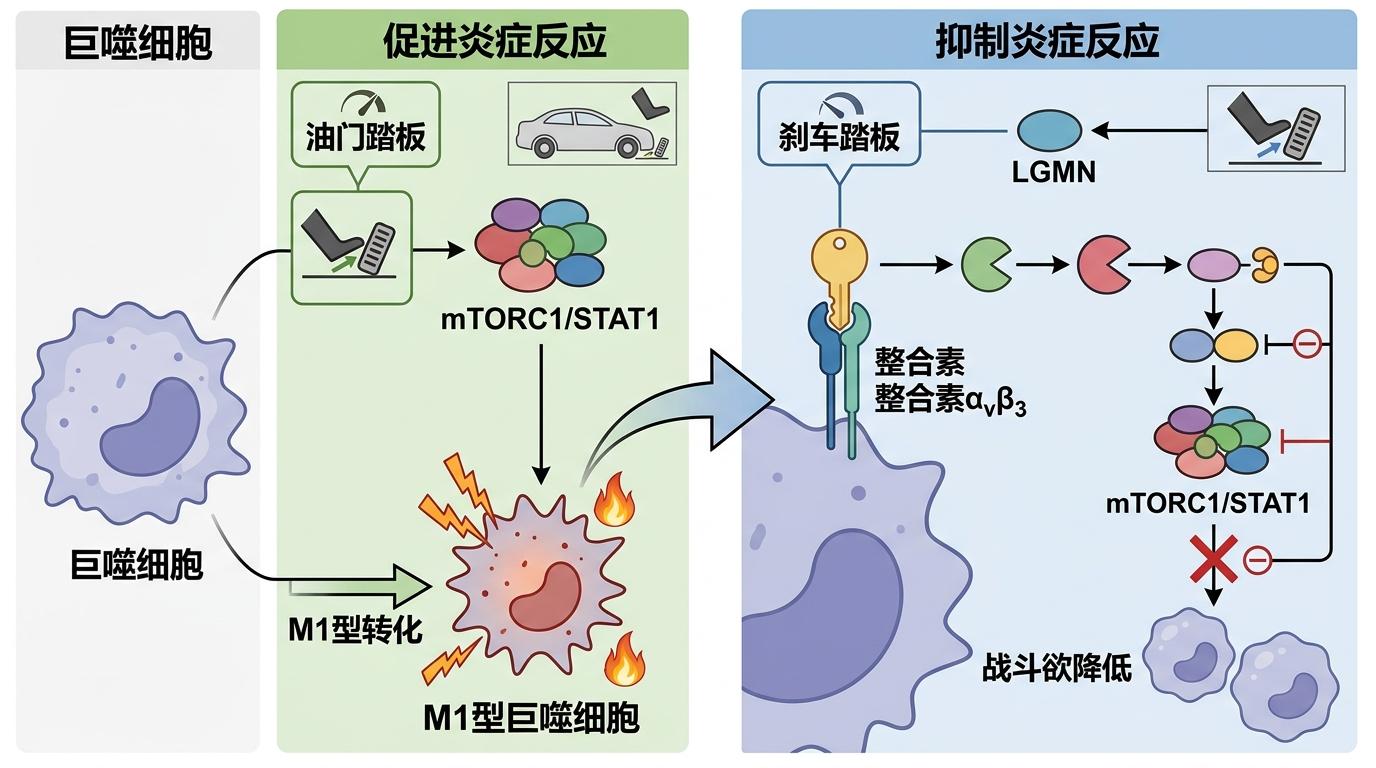
你可以把巨噬细胞的信号通路想象成一辆汽车,mTORC1/STAT1就是「油门踏板」——一旦被激活,就会驱动巨噬细胞向M1型转化,一路狂飙引发炎症。而LGMN会像个「刹车踏板」,它先结合巨噬细胞表面的整合素αvβ3,通过一系列分子反应,直接抑制mTORC1/STAT1通路的活性,让M1型巨噬细胞的「战斗欲」降下来。
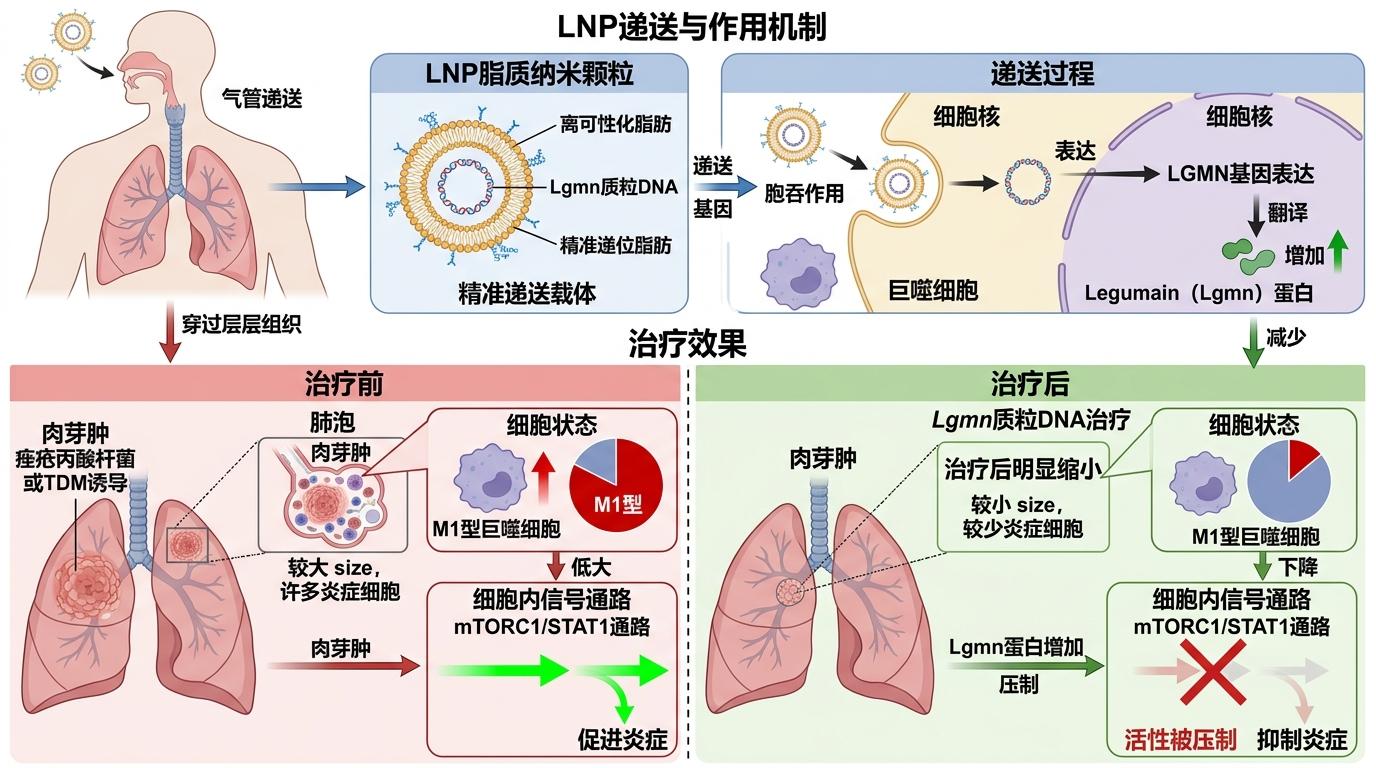
更关键的是,团队找到了把这个「刹车」送到病灶的方法:用脂质纳米颗粒(LNP)包裹Lgmn质粒DNA,通过气管递送到小鼠肺部。这种LNP就像精准快递,能穿过层层组织把LGMN基因送到巨噬细胞里。实验结果让人惊喜:无论是痤疮丙酸杆菌还是TDM诱导的肉芽肿,都被明显缩小,M1型巨噬细胞的比例大幅下降,mTORC1/STAT1通路的活性也被压制住了。
当然,这项研究也有局限:目前只在小鼠模型上验证了效果,人体临床试验还需要时间;LGMN在不同患者体内的表达差异,也会影响未来治疗的精准性。
有意思的是,LGMN在不同疾病里扮演的角色完全相反。在肿瘤里,它是「帮凶」——会促进巨噬细胞向M2型转化,形成免疫抑制环境,让癌细胞躲避免疫系统的追杀;但在结节病这类炎症性疾病里,它又变成了「救星」,专门抑制M1型巨噬细胞的促炎作用。
这种「双面性」恰恰说明,免疫调控是个精密的平衡游戏:多一分则炎症失控,少一分则免疫不足。LGMN就像这个平衡的「调节器」,不同的疾病状态下,它会通过不同的信号通路发挥作用。这也给未来的研究提了醒:针对LGMN的治疗,必须精准匹配疾病类型,不能一概而论。
从泼尼松的「一刀切」抗炎,到LGMN的「精准刹车」,结节病的治疗终于从「压制免疫」转向「调控免疫」。这不仅是一个分子靶点的发现,更代表着医学界对免疫疾病的理解,从「对抗炎症」升级到「恢复平衡」。
免疫是身体的铠甲,也是可能反噬的双刃剑。LGMN的发现,让我们看到了给这把剑装「保险栓」的希望。免疫的本质,是平衡而非对抗。未来,或许我们能找到更多这样的「分子开关」,让失控的免疫反应回归正轨。