对抗知识焦虑,从看懂这条开始
App 下载
细胞里的免疫快递,藏着治病的新钥匙
高尔基体|内质网|细胞器转运|SEC24C蛋白|STING蛋白|免疫学基础|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
高尔基体|内质网|细胞器转运|SEC24C蛋白|STING蛋白|免疫学基础|生命科学
当病毒悄悄溜进细胞,或者癌细胞在体内作乱,我们的免疫系统会立刻拉响警报。这个警报的关键传令兵,是一种叫STING的蛋白——它平时安安静静待在细胞的“后勤仓库”内质网里,一旦感知到危险信号,就必须迅速转移到“信号指挥中心”高尔基体,才能启动后续的免疫反击。
过去10年,科学家已经知道STING的这场迁移是免疫激活的关键,但始终没搞懂:它到底是怎么突破内质网的“门禁”,又是怎么保证自己不会乱跑导致免疫过度激活的?2026年2月,《Cell》杂志上的一篇论文,终于把这场细胞内的“秘密转移”拆解得明明白白。
要理解STING的迁移,得先把细胞里的细胞器比作一个公司:内质网是负责生产的仓库,高尔基体是分拣打包的物流中心,而COPII囊泡就是在两者之间跑运输的快递盒。每个快递盒都需要一个叫SEC24的“快递员”,专门识别要运送的货物。
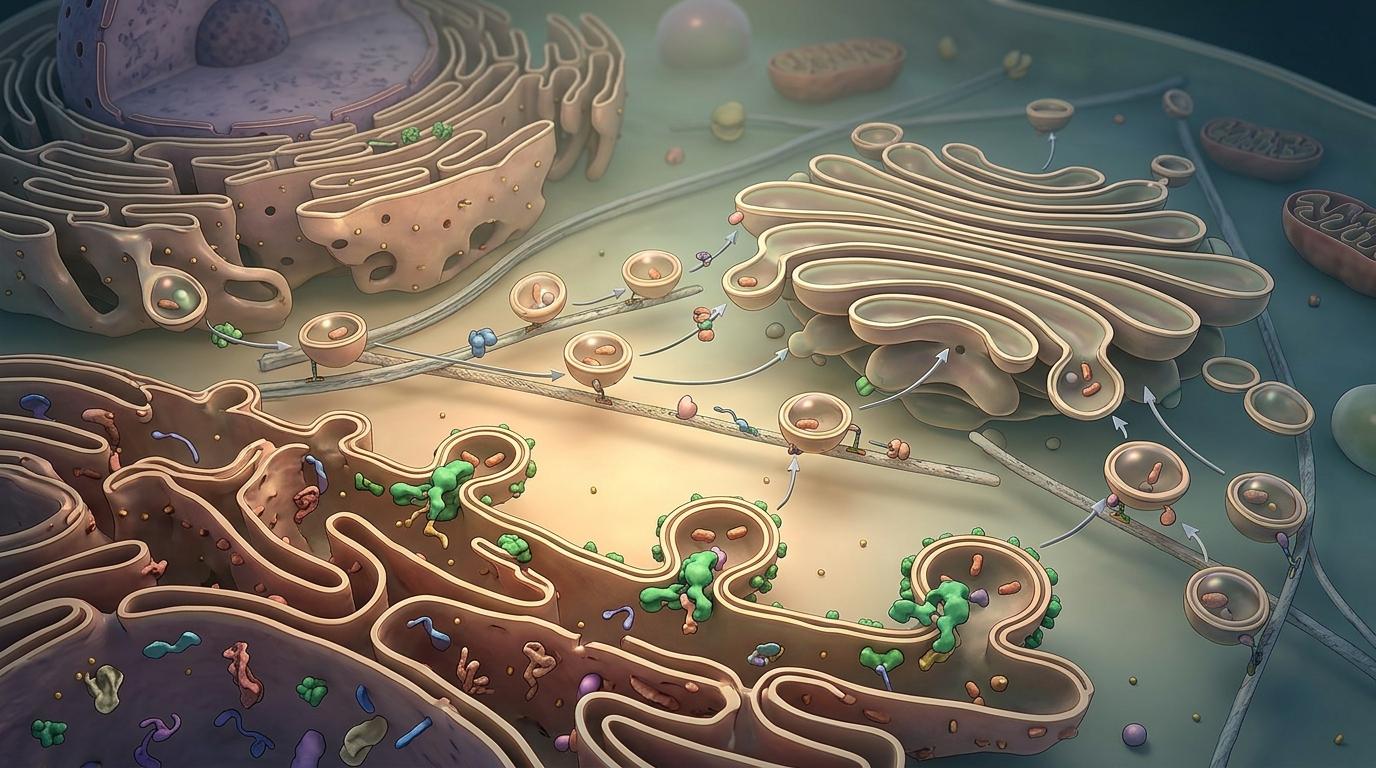
德克萨斯大学西南医学中心的研究团队发现,STING的“快递订单”只能由SEC24家族里的SEC24C来接。STING的C端有一段短短5个氨基酸的“快递地址”——339EEVTV343,这段序列刚好能卡进SEC24C的识别位点里。
但有意思的是,这段“地址”是个“半吊子”:它和SEC24C的结合力非常弱,单独一个STING分子根本抓不住快递员。这时候,STING必须先“组队”——和其他STING分子串联成链(也就是寡聚化),把几段弱结合的“地址”凑成一个强结合的“快递面单”,才能被SEC24C稳稳抓住,送进COPII囊泡里。
这个设计堪称精妙:如果单个STING就能随便溜出内质网,免疫系统可能会被风吹草动触发,导致自身免疫疾病;只有当足够多的STING同时激活,说明危险信号足够强,才会启动迁移。
当STING被SEC24C送进高尔基体,真正的免疫激活才刚刚开始。
研究人员用单分子成像技术观察到,STING进入高尔基体后,会在特定的脂质区域聚集——这个过程必须依赖一种叫“棕榈酰化”的化学修饰:高尔基体上的酶会把两个棕榈酸分子贴到STING的Cys88和Cys91位点上,就像给STING装了两个“锚”,让它能牢牢固定在高尔基体的脂筏区域。
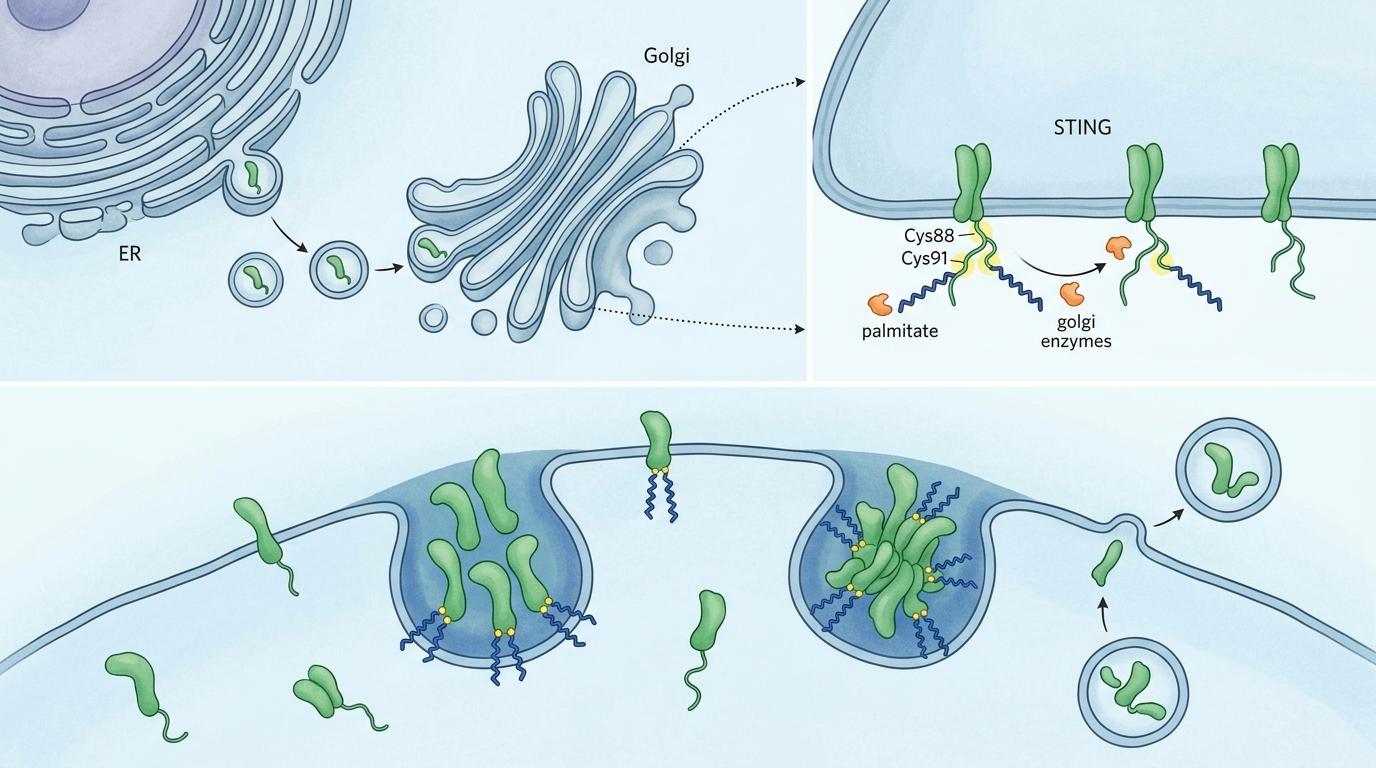
没有这两个“锚”,STING就算到了高尔基体也无法聚集,更没法招募下游的激酶TBK1。而TBK1正是启动免疫信号的关键:它会给STING和转录因子IRF3打上磷酸化的标记,激活的IRF3进入细胞核,就会下令生产干扰素和各种炎症因子,召唤免疫细胞来消灭入侵者。
更巧妙的是,细胞还留了“刹车”:当免疫反应足够强时,STING会被转运到溶酶体降解,及时终止信号,避免免疫过度损伤自身组织。
这场细胞内的“秘密转移”,给人类治病带来了全新的思路。
对于癌症患者来说,科学家可以通过改造STING的“快递地址”,让它更容易和SEC24C结合,或者直接用药物增强STING的寡聚化,让免疫信号更强——这样就能把“冷肿瘤”(免疫细胞浸润少的肿瘤)变成“热肿瘤”,帮助免疫检查点抑制剂更好地发挥作用。目前,基于这个思路的“超级STING”变体已经在动物实验中展现出了强大的抗肿瘤效果。
而对于自身免疫疾病患者,比如STING相关血管病(SAVI)和COPA综合征,问题恰恰出在STING的迁移失控:要么是STING的“地址”突变导致它随便就能溜出内质网,要么是逆向转运的“回程票”出了问题,导致STING在高尔基体持续激活。这时候,就可以用小分子药物阻断SEC24C和STING的结合,或者抑制棕榈酰化过程,给过度激活的免疫系统踩刹车。
不过,这条路还有不少坑要填:比如怎么把药物精准递送到病变细胞里,怎么避免全身给药带来的副作用,还有不同患者的STING基因多态性可能导致的疗效差异。但至少,我们终于摸到了调控免疫系统的“门把手”。
从2012年陈志坚博士发现cGAS-STING通路,到2015年Yan实验室发现STING的迁移现象,再到2026年揭开迁移的分子机制,科学家花了14年,才把细胞内这场几纳米尺度的“快递运输”搞清楚。
这正是生命科学最迷人的地方:我们身体里每一个看似简单的反应,背后都藏着亿万年进化出来的精妙调控。STING的这场“细胞内旅行”,不仅是免疫系统的防御密码,更是连接基础研究和临床治疗的桥梁。
精准调控免疫,才是治病的核心。未来,当我们能像控制开关一样控制STING的迁移和激活,也许就能真正实现“精准免疫治疗”——让该激活的免疫反应全力启动,让该沉默的免疫信号及时刹车。