
3 个月前

3 个月前
在每一个生命细胞构成的微观都市里,一套名为“自噬”(Autophagy)的系统,正像一支高效的资源回收与废物处理团队,夜以继日地工作。它拆解老旧损伤的细胞器和蛋白质,将其转化为能量和新生构件,维持着整座“城市”的清洁与活力。然而,如果这支团队的总指挥官,在发出“开工”信号的同时,又亲手为自己设下了路障,这听起来是否像一个难以理解的悖论?最近,一项突破性研究恰恰揭示了这样一个存在于细胞生命核心的精妙制衡机制。
就在不久前的2025年12月26日,国际权威期刊《自噬》(Autophagy)在线发表了中山大学李民教授团队的最新研究成果。这项研究的核心,直指自噬机器中的关键启动酶——ATG7。长期以来,科学家们都将ATG7视为自噬流水线的“发动机”或“第一推动力”。然而,李民团队发现,ATG7远不止于此,它还扮演着一个截然相反的角色:它既是启动一种特殊修饰过程(蛋白质ATG8化)的核心引擎,又是这个过程作用的关键“底物”,即被修饰的对象。
简单来说,ATG7在上游发号施令,驱动整个自噬流程;但同时,它又会给自己“贴上一个标签”,这个标签反而会阻碍它自己的工作效率。这一发现,揭示了自噬调控中一个前所未见的负反馈自我制动机制,彻底刷新了我们对ATG7功能的认知。
要理解这一发现的颠覆性,我们首先需要了解细胞自噬是如何运作的。可以将其想象成一个精确的分子接力赛:
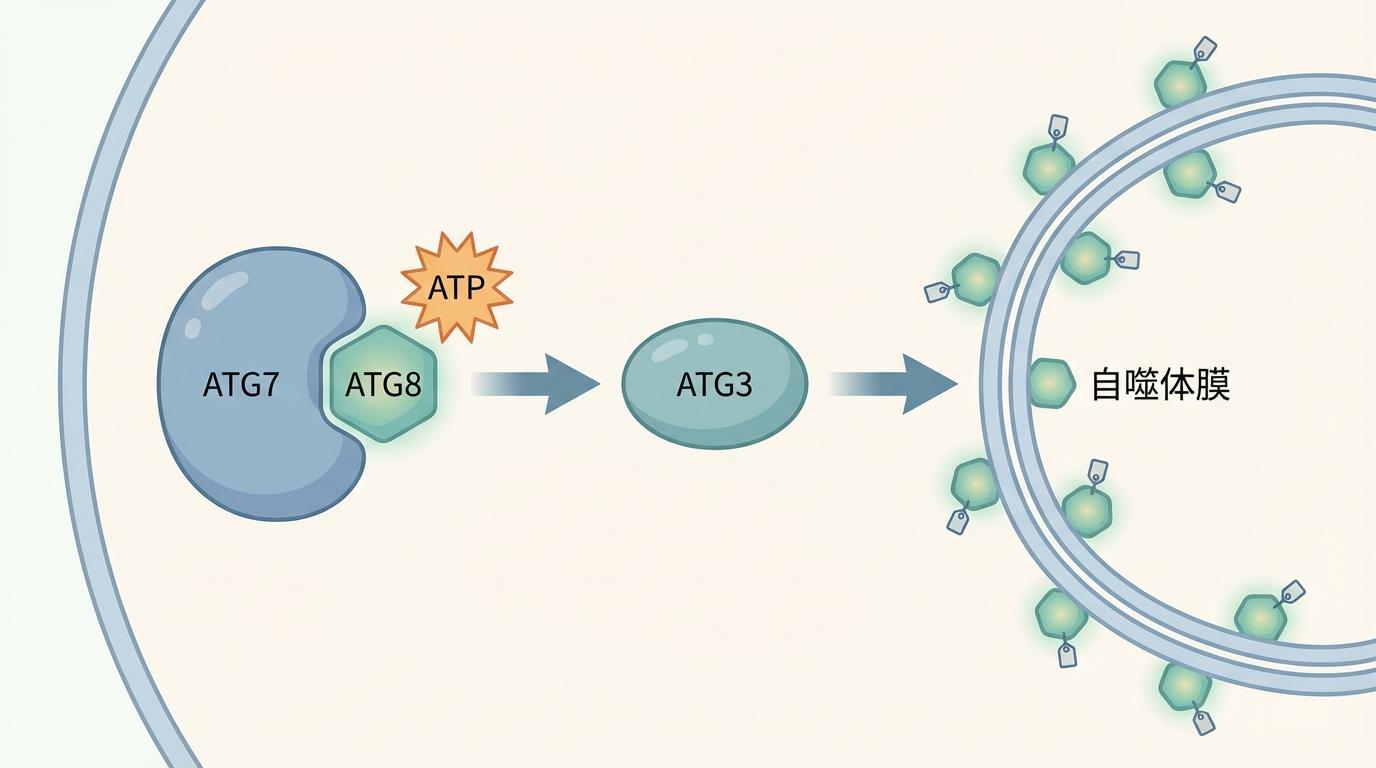
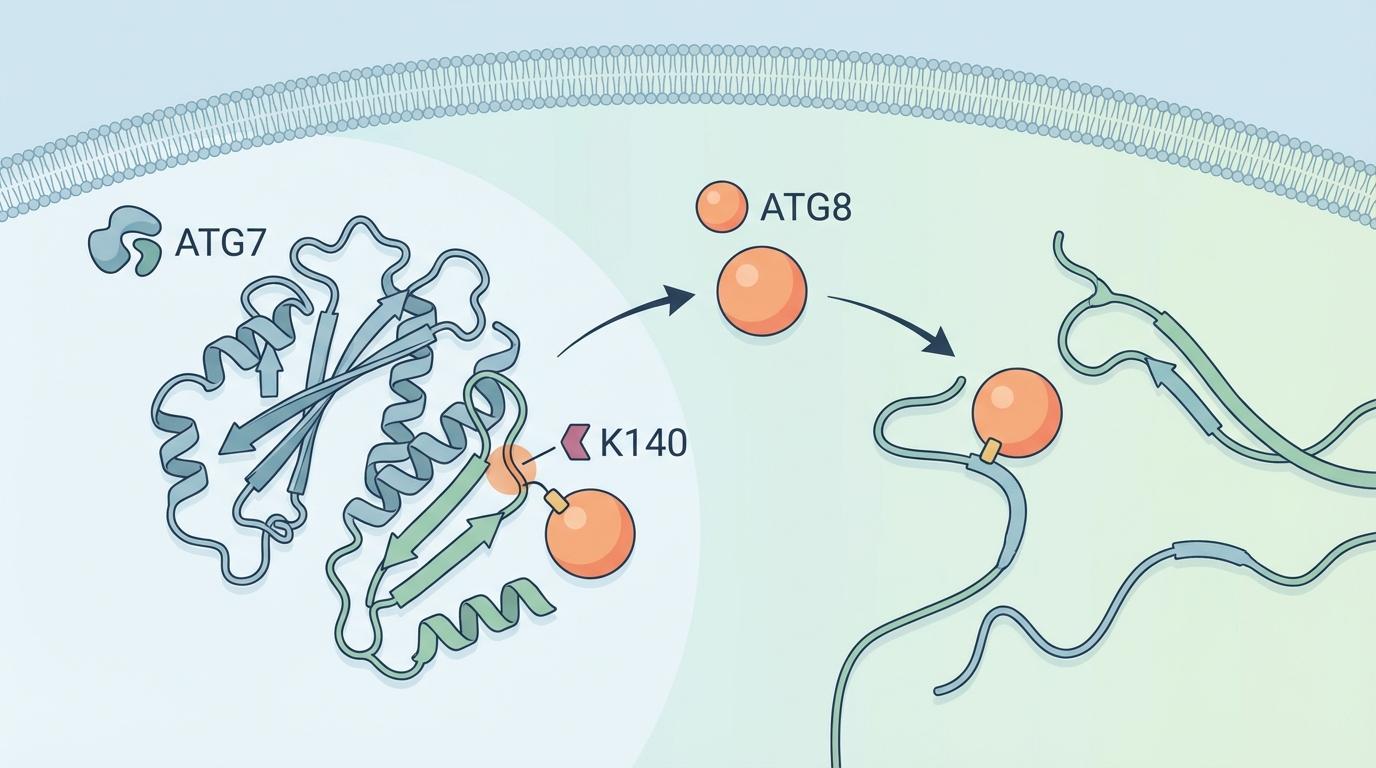
这个K140位点,恰好位于ATG7与它的下一棒队友ATG3相互作用的关键界面附近。一旦ATG8这个“挂件”被挂在了K140上,就会形成空间位阻,像一道屏障一样,阻碍了ATG7与ATG3的“握手”。接力棒无法顺利传递,整个自噬的流水线速度自然就慢了下来。这便是ATG7的自我制动——一个内置的、精巧的“刹车”系统。
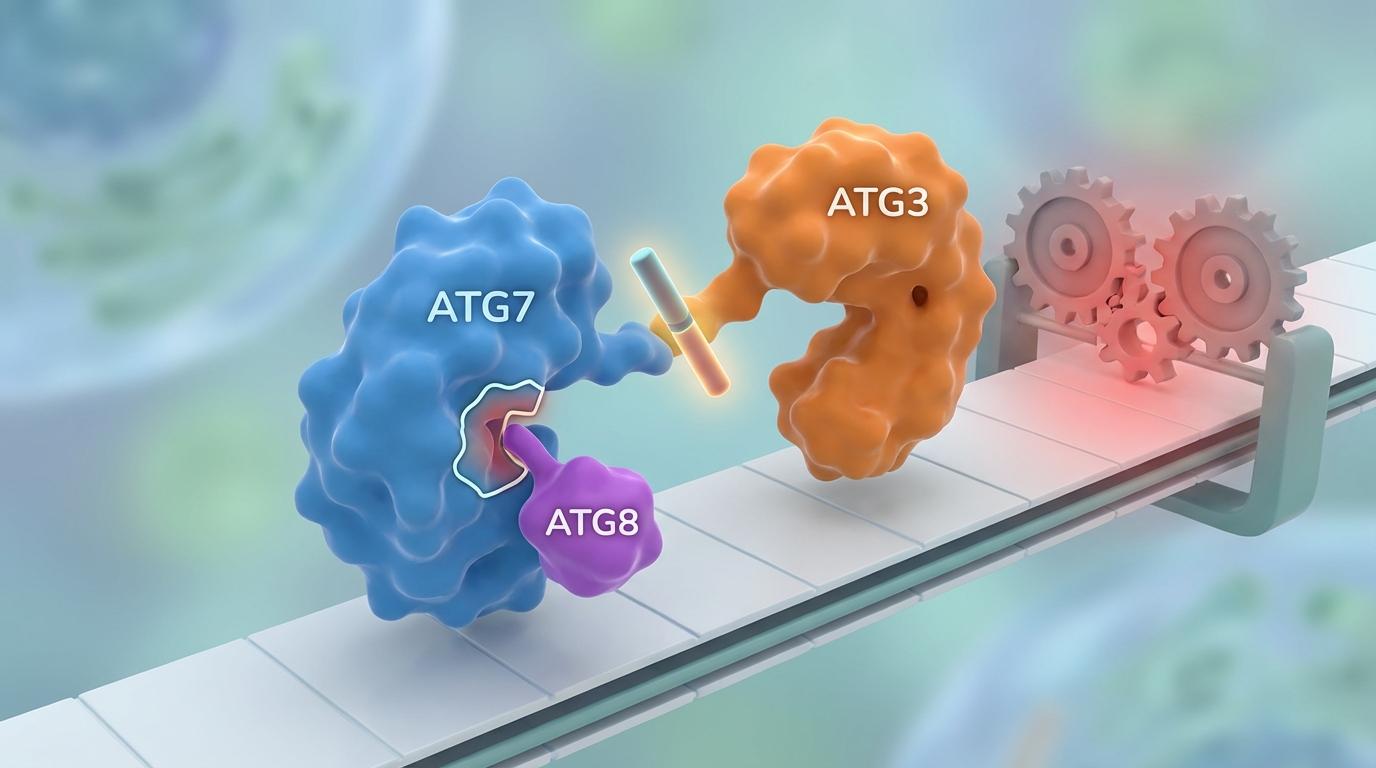
为了证实这一机制,研究团队展现了高超的实验设计。他们首先开发了特殊的分子工具——能够抵抗被切除的LC3B(ATG8家族的一员)突变体,使得追踪“蛋白质ATG8化”这一 elusive 的过程成为可能。
随后,他们通过系统的基因筛选和质谱分析,成功“抓获”了被修饰的ATG7,并精准定位到了K140这个关键刹车点。最令人信服的证据来自他们构建的细胞模型:当研究人员通过基因编辑技术,将内源的ATG7蛋白的K140位点进行突变,使其无法被ATG8修饰——相当于人为拆除了这个“刹车”——他们观察到,这些细胞的自噬活性显著增强了。这一结果无可辩驳地证明,ATG7的自我修饰确实是自噬过程的一个天然“减速带”。
这一发现的意义远不止于满足科学家的好奇心。自噬在人类健康与疾病中扮演着极其复杂的“双刃剑”角色。
在癌症(如白血病)中:一方面,正常的自噬可以清除受损细胞,抑制肿瘤的发生;但另一方面,一旦肿瘤形成,癌细胞会“劫持”自噬系统来抵抗化疗药物带来的压力,从而实现“苟延残喘”。因此,简单地“开启”或“关闭”自噬都不是理想的治疗策略。
在神经退行性疾病中:如阿尔茨海默病和帕金森病,自噬功能不足会导致有毒蛋白质的累积,损伤神经元。在这种情况下,适度增强自噬活性可能是有益的。
ATG7自我制动机制的发现,为我们提供了一个全新的调控靶点。它不再是一个简单的“开/关”,而更像一个**“调光器”**。未来,我们或许可以设计出精准的药物,去干预ATG7的K140位点修饰。比如,在癌症治疗中,通过“锁死刹车”来抑制自噬,增强癌细胞对化疗的敏感性;或者在神经退行性疾病中,通过“松开刹车”来提升自噬效率,帮助清除有毒蛋白。这种精细调节的可能性,为相关疾病的治疗打开了新的想象空间。
任何一项重大突破都会带来新的问题。李民团队的研究同样为我们留下了引人深思的悬念。例如,他们在体外原核系统中无法完整重建这一过程,这强烈暗示在哺乳动物细胞中,可能还存在一个尚未被发现的、负责识别底物的神秘E3连接酶,它像一个精准的“调度员”,决定着何时何地给ATG7“踩刹车”。
此外,细胞在何种生理或病理条件下会激活这一自我制动机制?它与其他已知的自噬调控网络(如mTOR信号通路)是如何协同工作的?这些都是未来研究亟待解答的关键问题。对“蛋白质ATG8化”这一新兴领域的探索,才刚刚拉开序幕。
从ATG7的双重身份中,我们窥见了生命演化令人惊叹的智慧。细胞内最强大的“分解”系统,其核心驱动者自身就携带者一个“安全阀”。这种内在的自我约束,确保了强大的力量不会失控,维持着动态而脆弱的生命平衡。这项发现不仅是自噬领域的一大步,更是对生命自我调控复杂性的一次深刻致敬。它提醒我们,在微观的细胞世界里,每一个角色都可能比我们想象的更加深邃,而对这些秘密的探索,终将照亮我们对抗疾病、理解生命的道路。
点击充电,成为大圆镜下一个视频选题!