
11 天前

11 天前
想象一下:你的心脏因为心梗坏死了一块肌肉,医生不用开胸,不用移植,只需要在你胸口打一针,就能让伤口附近的疤痕细胞「变身」成新的心肌细胞——既能填补缺损,又能避免纤维化。这不是科幻,是再生医学领域追了十几年的梦想。但现实是,这种「在体重编程」的效率一直卡在个位数,绝大多数疤痕细胞根本不搭理那些诱导信号。直到北京大学赵扬团队的新研究,终于揪出了藏在细胞里的「刹车」——钙网蛋白CALR,它正通过一套精密的钙信号机制,死死按住了疤痕细胞变身的开关。为什么心梗会激活这个刹车?关掉它真的能让心脏再生吗?
要找到阻碍再生的关键因子,传统方法只能一个个试,像在黑屋子里摸开关。赵扬团队换了个思路:给心梗后的心脏做一次「全基因组扰动扫描」——这就是他们改进的在体Perturb-seq技术。
你可以把这套技术想象成给140个候选基因各装一个「开关」,然后把这些带开关的疤痕细胞一起植入小鼠心梗区域,观察哪些开关一关掉,疤痕细胞就乖乖变身成心肌细胞。最终,钙网蛋白CALR的开关脱颖而出:只要敲低它的表达,小鼠体内的重编程效率直接提升了10倍,从不到2%跃升到10%-20%,体外实验更是接近70%。
更关键的是,这些新生成的心肌细胞不是「残次品」——它们能像天然心肌细胞一样同步跳动,产生规律的钙信号振荡,这意味着它们真的能承担泵血功能。
CALR到底是怎么卡住细胞变身的?答案藏在细胞内的钙离子平衡里。
你可以把细胞的内质网想象成一个「钙仓库」,CALR就是仓库管理员。心梗发生后,细胞启动应激反应,CALR的数量暴增,它会把仓库里的钙离子死死守住,不让它们流到细胞质里。而细胞质里的钙离子,正是激活心肌重编程关键因子MEF2C的「钥匙」——钙离子浓度不够,MEF2C就处于休眠状态,疤痕细胞自然变不成心肌细胞。
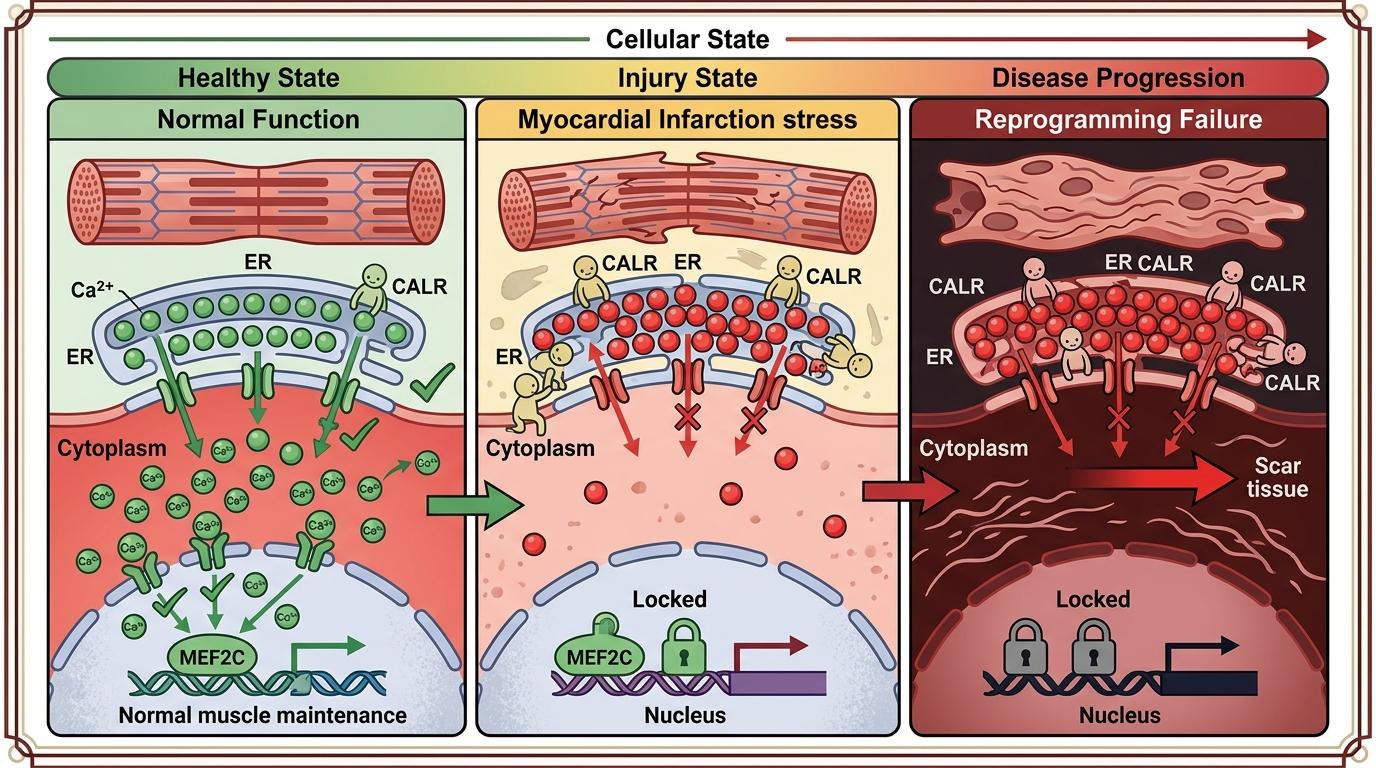
当研究人员敲低CALR后,仓库的门被打开,钙离子涌入细胞质,激活了下游的CaM/CaMKIIδ通路,MEF2C终于苏醒,开始指挥细胞合成心肌特有的蛋白质,完成命运的转变。甚至在某些情况下,激活钙信号的效果能直接替代外源MEF2C的作用——相当于用细胞自己的钥匙,打开了变身的开关。
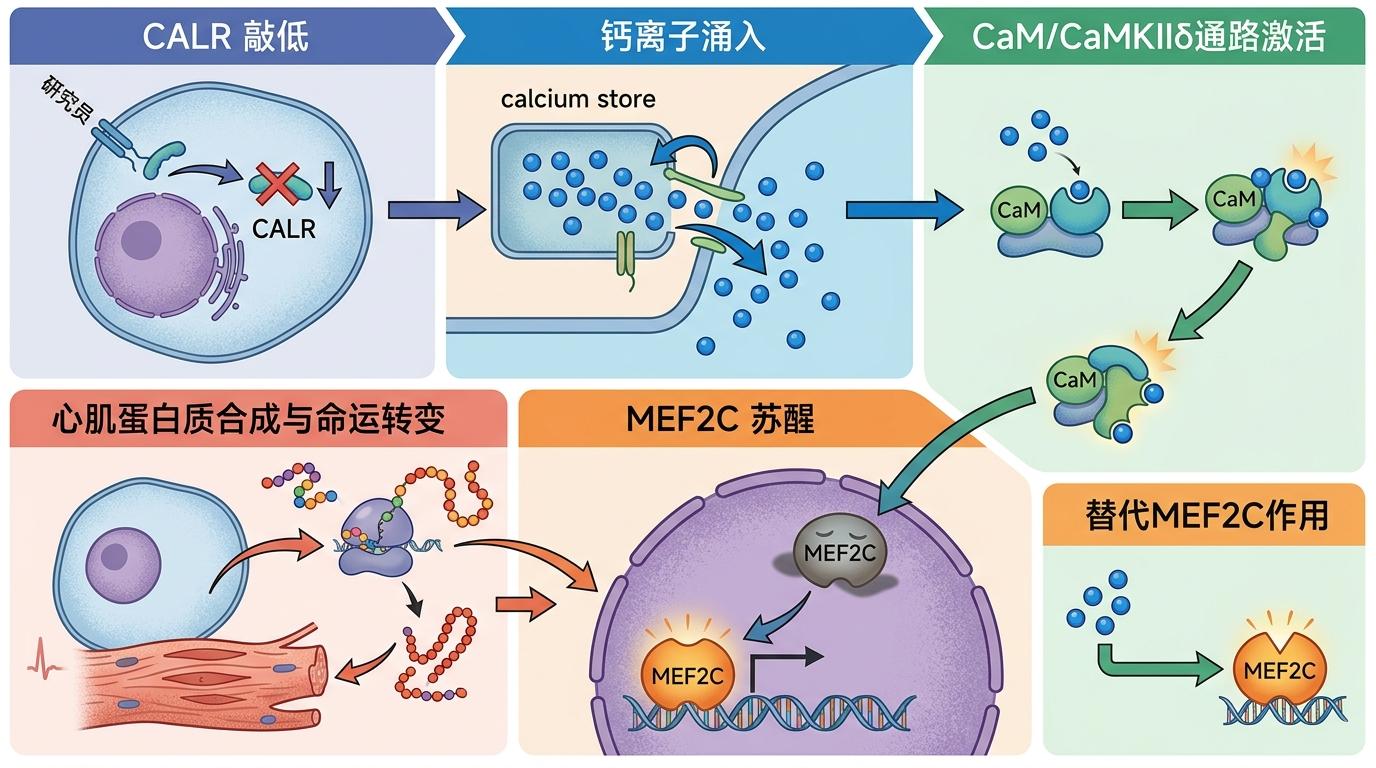
这个发现给心梗的再生治疗带来了新靶点,但距离真正应用到临床,还有几道坎要跨。
首先是递送问题:怎么精准地把CALR抑制剂或者钙信号激活剂送到心梗区域的疤痕细胞里?目前用的病毒载体虽然有效,但存在潜在的基因组整合风险,需要更安全的非病毒递送系统。其次是长期安全性:敲低CALR会不会影响细胞的正常钙稳态?会不会引发心律失常等副作用?这些都需要大动物模型和长期实验来验证。
更值得关注的是,CALR只是心梗微环境中的一个障碍因子,还有免疫反应、纤维化信号等其他「路障」存在。未来的再生治疗,很可能需要多靶点联合调控,才能让疤痕细胞高效、安全地变身成心肌细胞。
成年哺乳动物的心脏一直被认为是「不可再生」的器官,就像一台一旦零件损坏就无法修复的机器。但赵扬团队的研究,让我们看到了另一种可能:心脏其实自带「修复零件的图纸」,只是被病理环境中的「刹车」按住了。
解锁CALR介导的钙信号通路,相当于找到了启动这张图纸的钥匙。这不仅是心梗再生治疗的突破,更让我们意识到:很多时候,疾病不是身体失去了某种能力,而是这种能力被环境抑制了。
解铃还须系铃人,再生的钥匙就在细胞自己身上。
点击充电,成为大圆镜下一个视频选题!