
10 天前

10 天前
一位62岁的结直肠癌患者,术后接受了标准抗PD-1免疫治疗,肿瘤却仍在悄悄进展——这类“免疫治疗无效”的患者,占了结直肠癌总数的85%。医生曾以为是肿瘤本身的基因突变在作祟,直到复旦大学、中国医学科学院肿瘤医院等团队的研究揭开了另一个隐秘的凶手:患者血清中一种叫甘胆酸的代谢物,浓度比健康人高出数倍。它不是直接杀伤免疫细胞,而是通过一条隐藏的分子链条,给肿瘤细胞披上了“隐身衣”,让免疫治疗彻底失效。这条链条到底是什么?又该如何打断它?
你可以把肿瘤细胞的免疫逃逸想象成一场精心策划的伪装行动:甘胆酸就是那个发号施令的“幕后黑手”。
首先,它会抑制一种叫FXR的胆汁酸受体——这个受体原本像个“刹车”,死死按住转录因子SOX14的表达。当FXR被甘胆酸压制,SOX14就会“挣脱束缚”,开始大量合成棕榈酰转移酶DHHC9。
DHHC9的作用是给肿瘤细胞表面的PD-L1蛋白“做美容”:它会把棕榈酸分子连接到PD-L1上,这个过程叫棕榈酰化修饰。被修饰后的PD-L1稳定性大幅提升,能更长时间地停留在肿瘤细胞表面,就像给细胞贴上了“自己人”的标签,让负责杀伤肿瘤的CD8⁺T细胞彻底认不出目标。
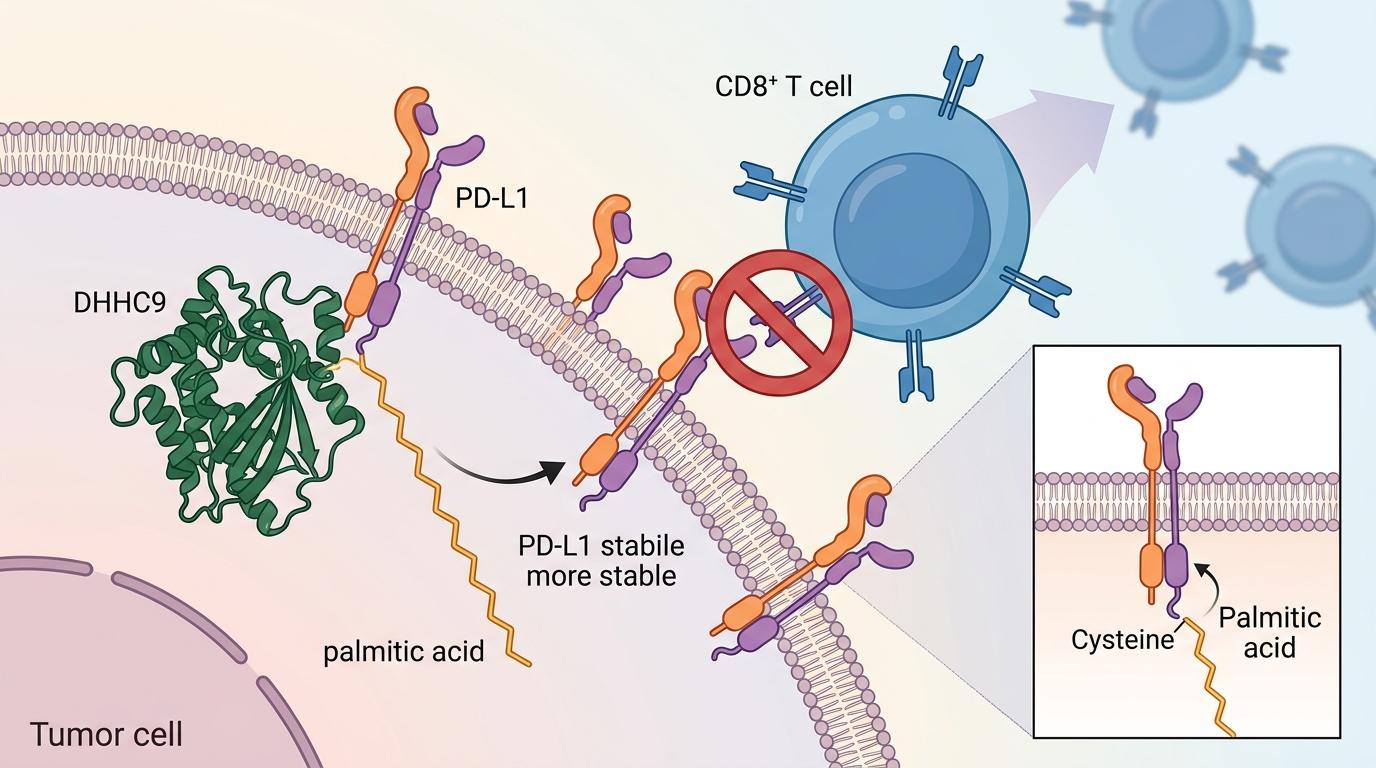
简单说就是:甘胆酸→抑制FXR→激活SOX14→增多DHHC9→稳定PD-L1→免疫细胞“失明”→肿瘤疯长。
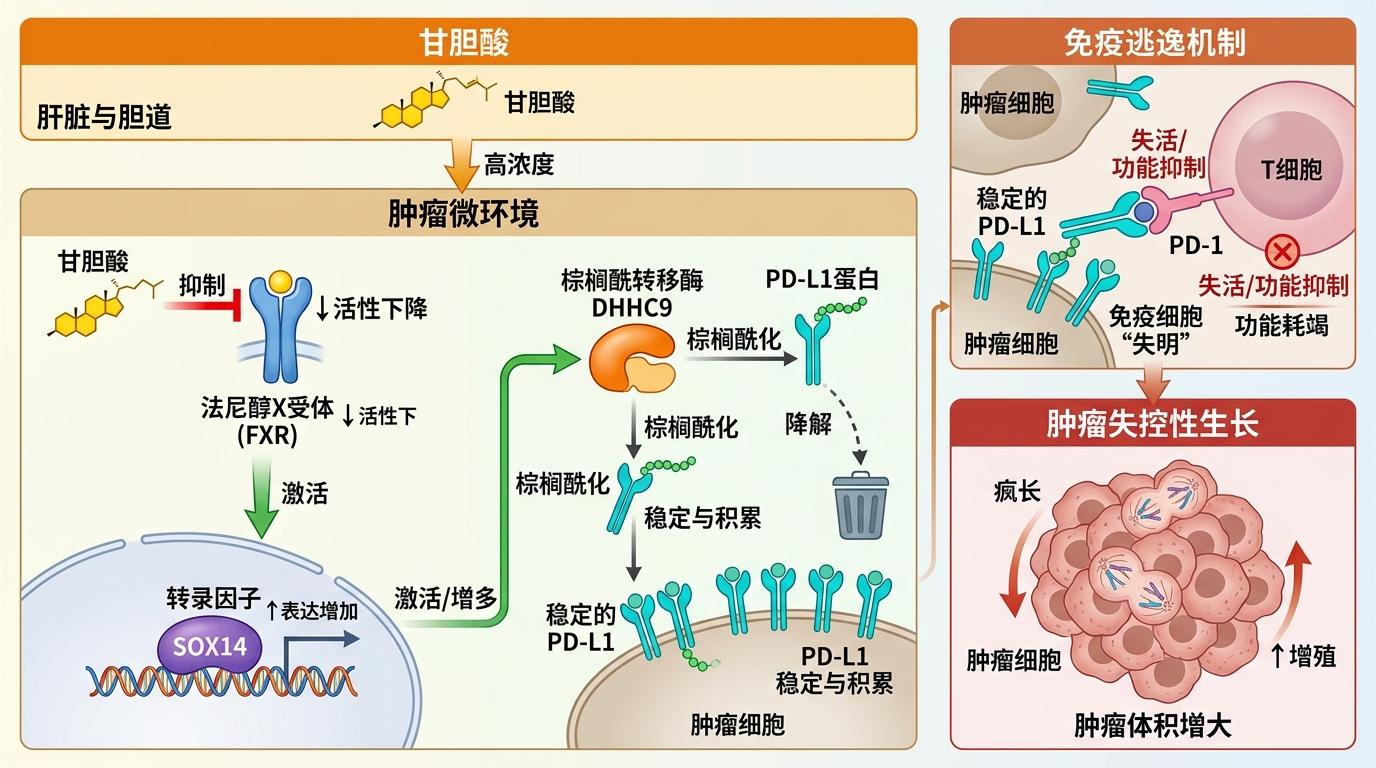
既然搞懂了甘胆酸的“作恶路径”,科学家们很快找到了破解方法。
在结直肠癌小鼠模型中,他们尝试了三种策略:一是用药物激活被抑制的FXR,重新按住SOX14的“嚣张气焰”;二是直接沉默SOX14或DHHC9的表达,掐断链条的中间环节;三是联合抗PD-1免疫治疗。结果令人振奋:三种策略都能显著降低肿瘤细胞表面的PD-L1水平,原本“沉睡”的CD8⁺T细胞重新被激活,肿瘤生长速度被大幅抑制,甚至有部分小鼠的肿瘤完全消退。
不过研究也留下了现实的局限:目前使用的FXR激动剂GW4064还存在组织非特异性问题,可能引发瘙痒、胃肠道反应等副作用,距离临床应用还需要优化。而且这条分子链条在其他癌种中是否同样有效,还需要更多研究验证。
这项研究最值得关注的,其实是它撕开了“代谢-免疫-肿瘤”网络的一角。
过去我们总把免疫治疗耐药归因于肿瘤细胞的基因突变,却忽略了代谢物的作用。甘胆酸原本只是参与脂肪消化的普通分子,却在肿瘤微环境中变成了免疫逃逸的“帮凶”——这说明肿瘤的代谢重编程,不止是为了给自己“供能”,还能通过改变代谢物的浓度,直接操控免疫微环境。
更有意思的是,甘胆酸的代谢还和肠道菌群密切相关:肠道菌群可以把初级胆汁酸转化为次级胆汁酸,而不同菌群组成会直接影响血清甘胆酸的水平。这意味着未来或许可以通过调节肠道菌群、干预胆汁酸代谢,从源头减少甘胆酸的产生,为免疫治疗“铺路”。
当我们把目光从肿瘤细胞的基因突变,转向那些在血液中流动的代谢物时,癌症治疗的边界正在被拓宽。对于那85%对免疫治疗无响应的结直肠癌患者来说,检测血清甘胆酸浓度,或许就能找到精准治疗的入口。
代谢微调,就能撬动免疫治疗的天平。这条被发现的FXR–SOX14–DHHC9–PD-L1通路,不仅是一个新的治疗靶点,更提醒我们:肿瘤从来不是孤立存在的,它和我们的代谢、肠道菌群、免疫系统紧密缠绕,而解开这些缠绕的钥匙,可能就藏在那些被我们忽略的“普通分子”里。
点击充电,成为大圆镜下一个视频选题!