
3 个月前

3 个月前
一位72岁的老人坐在窗边,手指无意识地摩挲着相册里褪色的照片——那是他大学毕业时的合影。如今,他叫不出照片中任何一个人的名字,包括他自己。阿尔茨海默病(AD)像一场浓雾,正吞噬着他六十年的记忆。2026年的今天,全球像他这样的患者已突破5500万,而传统药物治疗只能暂时缓解症状,无法阻挡疾病的侵蚀。免疫疗法曾带来曙光:靶向β-淀粉样蛋白(Aβ)的抗体能清除脑内致病斑块,但静脉注射后仅有0.1%的药物能穿越血脑屏障(BBB),更引发脑水肿和微出血(ARIA)等致命风险。这道由400英里长的脑血管筑成的“城墙”,成了治疗无法逾越的天堑。
2025年8月7日,《科学》杂志同时点亮了两束穿透迷雾的光。美国Denali治疗公司Y. Joy Yu Zuchero团队发表的研究,揭示了一种名为**ATVcisLALA的抗体运输载体:它将抗Aβ抗体与转铁蛋白受体(TfR)结合域融合,像特洛伊木马般骗过血脑屏障守卫。更精妙的是其不对称Fc突变设计**——一条抗体链保留清除斑块的功能,另一条则削弱了引发贫血的毒性。
同一期杂志上,温州医科大学宋伟宏团队的评述为这项技术落下关键注脚:在AD小鼠模型中,ATVcisLALA使抗体脑内浓度提升5-8倍,且均匀分布至深层脑组织。传统抗体因聚集在血管周围引发炎症(ARIA),而新技术几乎完全消除了这一风险。
血脑屏障的铜墙铁壁由毛细血管内皮细胞紧密连接而成,仅允许氧气和小分子脂质通过。但科学家发现,脑血管细胞表面的转铁蛋白受体(TfR1) 原是天然的“通关文牒”——它本负责将铁元素转运入脑。Denali团队设计的ATV抗体正是劫持了这一机制:
罗氏公司的Trontinemab双抗(同时靶向Aβ和TfR)临床数据佐证了这一路径的可行性:91%患者脑内斑块被清除,ARIA风险降至5%以下,剂量仅为传统疗法的五分之一。
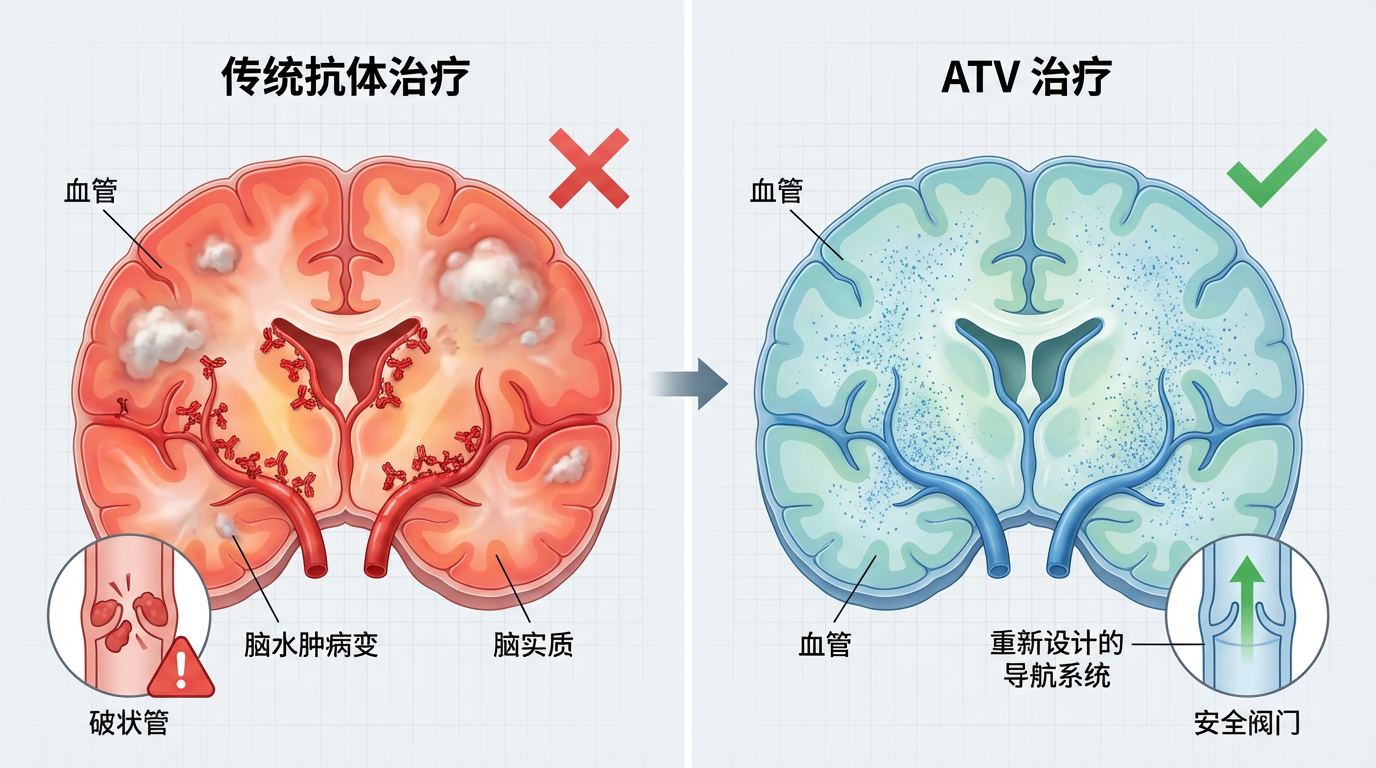
传统抗体的困局在于“双刃剑效应”:为增强疗效需增加剂量,却加剧了ARIA风险。ATVcisLALA的不对称Fc结构提供了破局之道。其一条链的LALA突变(Leu234Ala/Leu235Ala)阻断了与血细胞受体的结合,避免免疫系统误伤红细胞导致贫血;另一条链则保留完整功能,激活小胶质细胞吞噬斑块。
在模拟人类AD的5xFAD小鼠中,传统抗体治疗组80%出现脑水肿病变,而ATV组几乎完好无损。三维成像显示,新技术输送的抗体如细雨渗入土壤般均匀浸润脑实质,而非淤积在血管表面。“这相当于重新设计了抗体的‘导航系统’和‘安全阀门’。”一位研究者如此比喻。
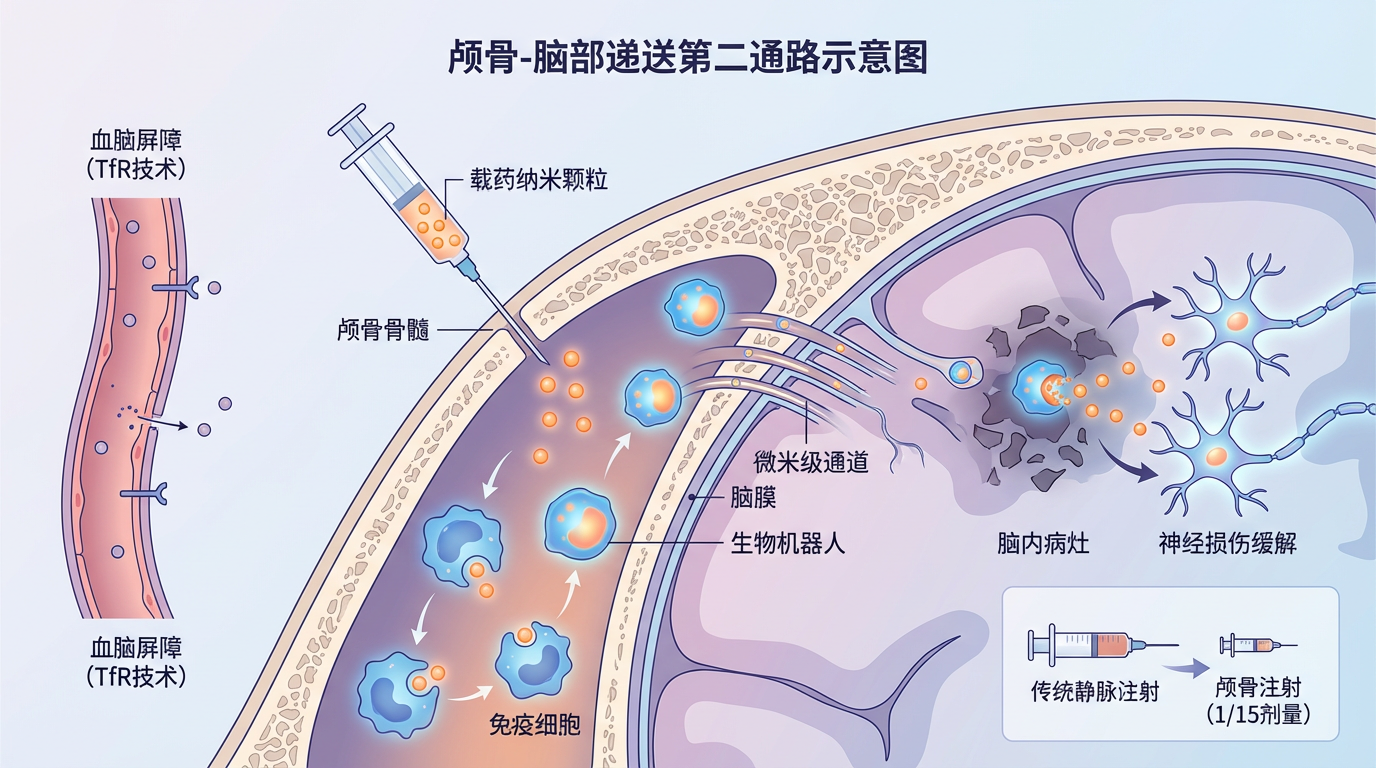
当TfR技术破解血脑屏障时,另一支“奇兵”正从颅骨骨髓中悄然出发。清华大学与北京天坛医院团队发现:颅骨与脑膜间存在微米级通道,免疫细胞可经此直达脑内病灶。他们将载药纳米颗粒注入颅骨骨髓,被免疫细胞吞噬后形成“生物机器人”,以传统静脉注射1/15的剂量成功缓解脑卒中小鼠的神经损伤。首个人体试验(SOLUTION试验)已显示安全性,为脑部递送开辟了第二条通路。
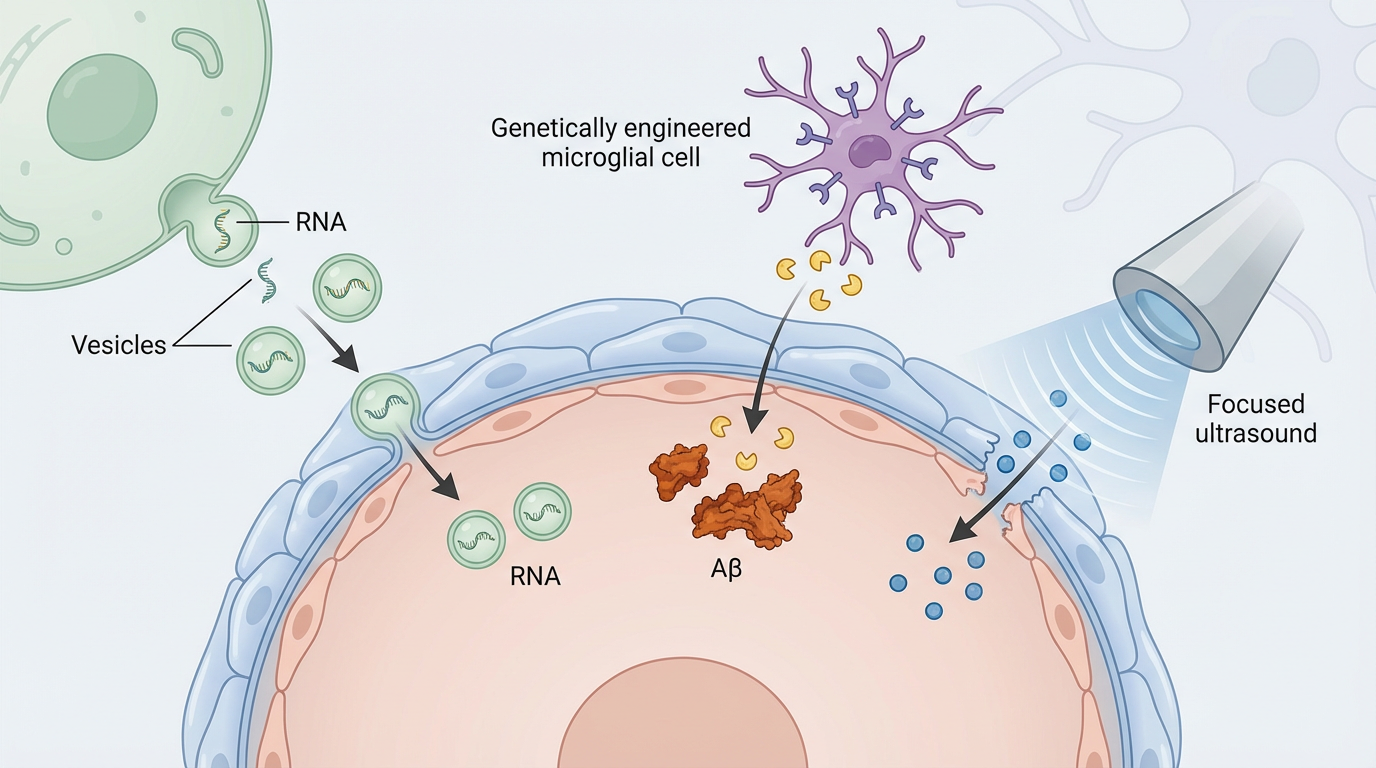
此外,外泌体作为天然纳米载体,可携带治疗性RNA穿越屏障;基因工程化小胶质细胞能持续分泌降解Aβ的酶;聚焦超声则短暂打开屏障促进药物渗透。这些技术如同多支探险队,正从不同方向攻克同一座堡垒。
“单一靶点治疗AD就像用一把钥匙开十把锁。”最新研究揭示了更复杂的病理网络:Aβ沉积触发tau蛋白缠结,小胶质细胞过度激活又加速神经元死亡。未来疗法必将走向多靶点协同:
在中国,华山医院率先开出仑卡奈单抗处方,社区早筛体系正建立“认知保护档案”。随着血液生物标志物检测获批(准确率超91%),未来患者或可通过年度体检实现早诊早治。
从1984年发现Aβ致病性到2025年递送技术突破,人类与阿尔茨海默病的抗争史布满荆棘。如今,转铁蛋白受体递送技术如同一座新灯塔,其光芒不仅照亮AD治疗之路,更为帕金森病、渐冻症等神经退行性疾病的攻克提供了范式。当科学家在微观世界操纵抗体的“导航密码”,在颅骨骨髓开辟“生物特快专递”,我们终将理解:对抗遗忘的战争,本质是一场对人类尊严最深刻的守护。
点击充电,成为大圆镜下一个视频选题!