对抗知识焦虑,从看懂这条开始
App 下载
神经退行性疾病新元凶:GSDM蛋白如何点燃大脑“焦亡”之火?
神经元死亡|帕金森病|阿尔茨海默病|细胞焦亡|GSDM蛋白|神经退行性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
神经元死亡|帕金森病|阿尔茨海默病|细胞焦亡|GSDM蛋白|神经退行性疾病|医学健康
在我们的大脑这座精密无比的城市里,数以百亿计的神经元如同市民,维系着记忆、情感与思考的运转。然而,在阿尔茨海默病、帕金森病等神经退行性疾病的阴影下,这座城市开始失序。长久以来,科学家们认为,致病的蛋白“垃圾”(如淀粉样斑块和α-突触核蛋白)是导致神经元死亡的直接杀手。但这好比说,垃圾堆积是城市衰败的唯一原因,却忽略了更深层的危机:当城市的“清洁工”——免疫细胞,不仅停止工作,反而开始四处“纵火”时,一场毁灭性的灾难便无可避免。近年来,一个名为“细胞焦亡”(Pyroptosis)的概念浮出水面,它描述的正是这样一种惨烈的场景:细胞并非安静地凋零,而是以一种“自燃”的方式壮烈死去,并释放出大量炎症信号,点燃周围的组织,形成一场燎原大火。这正是神经退行性疾病研究领域面临的一场认知革命。
这场革命的号角,由一系列突破性研究吹响。近期,由湖北工业大学赵震环团队、美国弗吉尼亚大学王少斌团队及福建医科大学赖忠盟团队联合发表在《Cell Death & Disease》上的一篇长篇综述,系统性地将聚光灯投向了这场“火灾”的幕后黑手——Gasdermin(GSDM)蛋白家族。这篇报告如同一份详尽的案情分析,首次全面梳理了GSDM介导的焦亡,是如何从一个原本在免疫抗感染领域被熟知的基础机制,演变为理解神经退行性疾病核心病理的关键。报告明确指出,GSDM蛋白介导的焦亡,不仅是神经元死亡的新通路,更是连接蛋白质异常聚集、神经炎症和细胞死亡三大病理特征的核心枢纽,为开发精准治疗药物提供了前所未有的突破口。
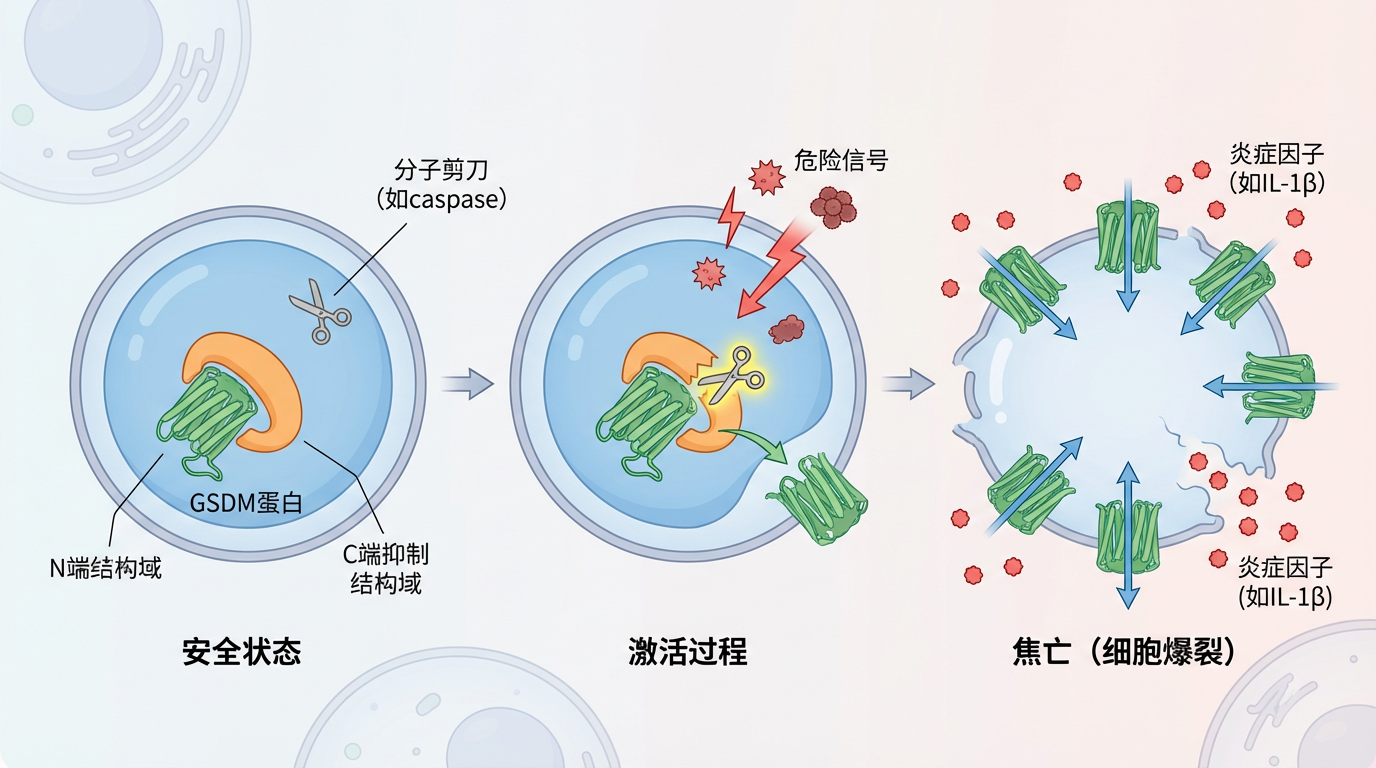
GSDM蛋白家族,堪称细胞内一个精密又危险的“自毁装置”。每个GSDM蛋白分子都由两部分构成:一个负责执行“爆破”任务的N端结构域,以及一个在平时将其牢牢锁住的C端抑制结构域。在正常情况下,这套装置处于安全关闭状态。然而,一旦细胞感知到危险信号——无论是病原体入侵,还是阿尔茨海默病中的β淀粉样蛋白聚集——特定的“分子剪刀”(如caspase蛋白酶)就会被激活,剪断连接N端和C端的锁链。被释放的N端结构域会迅速冲向细胞膜,像打桩机一样在膜上钻出巨大的孔洞。细胞内外平衡被打破,水分涌入,细胞急剧膨胀直至爆裂,同时将内部的炎症因子(如IL-1β)喷射而出,向周围的免疫系统发出最强烈的警报。这就是经典的焦亡过程。研究发现,这个家族中的两位关键成员在神经退行性疾病中扮演了不同角色:
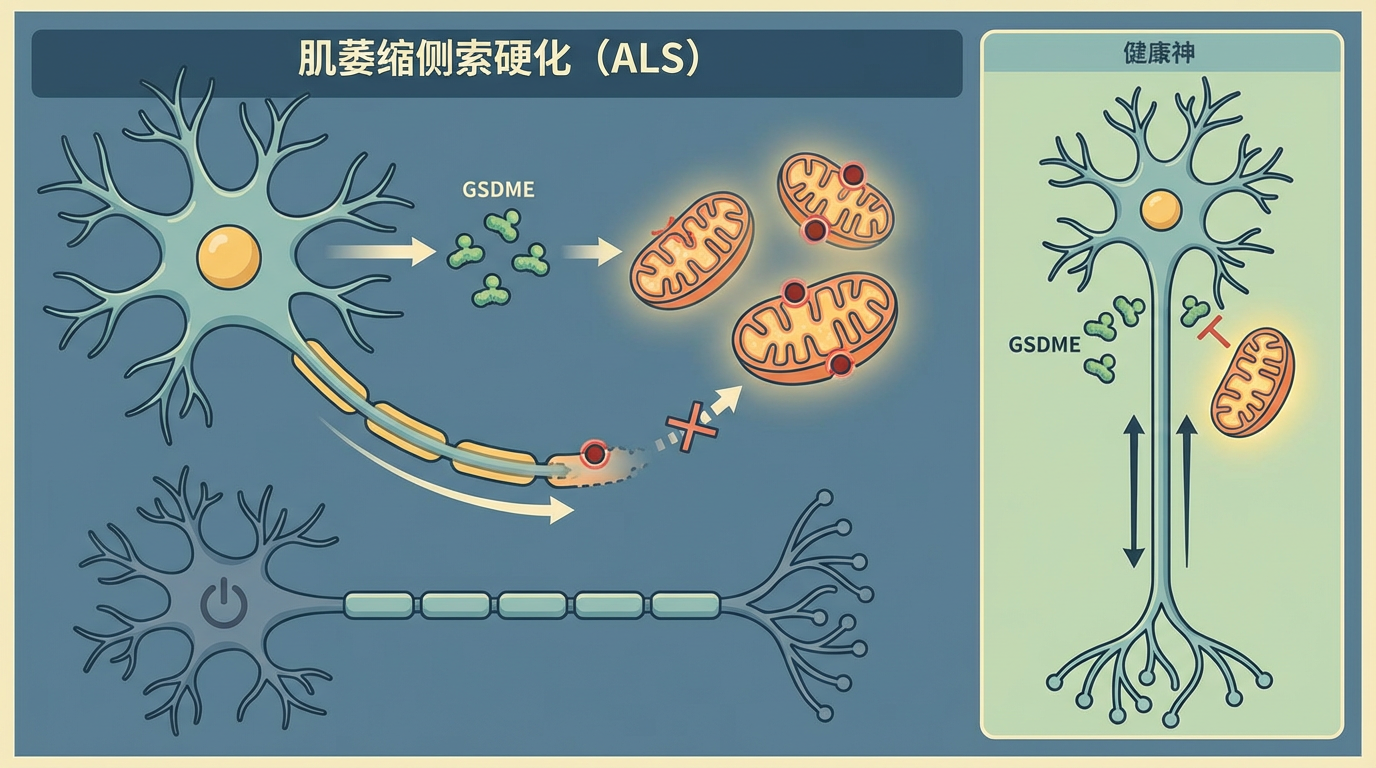
顺着GSDM这条线索,科学家们在多种神经退行性疾病的“犯罪现场”都找到了它的确凿证据:
既然找到了“纵火犯”,下一步自然是开发有效的“灭火器”。早期的策略集中于抑制上游的caspase蛋白酶,但这如同在火灾发生前阻止点火,一旦火势已起便无能为力。因此,直接靶向GSDM蛋白本身,阻止其在细胞膜上打孔,成为更具吸引力的策略。目前,研究人员已开发出多种策略:
SK56的强大之处在于其前所未有的精准性和多功能性。它不仅是一个“灭火器”,更像一个智能“修复机器人”。
尽管前景光明,但通往临床应用的道路依然充满挑战。焦亡本身是一把双刃剑,它既是驱动疾病的破坏力量,也是机体清除感染细胞、抵抗肿瘤的必要防御手段。如何设计出既能抑制神经系统中的过度焦亡,又不影响全身免疫监视功能的药物,是未来研究的核心难题。此外,大脑中不同细胞类型(神经元、小胶z质细胞、星形胶质细胞)对焦亡的反应各不相同,这意味着未来的治疗必须更加“个性化”,需要开发能靶向特定细胞的药物递送系统。我们需要一张更精细的“GSDM激活地图”,借助空间组学等前沿技术,来描绘在疾病不同阶段、不同脑区,GSDM是如何被激活和调控的。
从识别一种被忽视的细胞死亡模式,到揭示其在神经退行性疾病中的核心作用,再到利用AI设计出能够“亡羊补牢”的智能药物,我们对大脑“火灾”的理解和干预能力正在发生质的飞跃。GSDM介导的焦亡,不再仅仅是细胞生物学教科书上的一个名词,它已成为横亘在人类与神经退行性疾病之间的关键战场。在这片曾经被认为只能被动失守的“焦土”上,科学的智慧正点燃新的火种——那不是毁灭的火焰,而是重建与治愈的希望之光。