对抗知识焦虑,从看懂这条开始
App 下载
绘制身体的内在地形:能量景观如何揭示疾病的隐秘源头
小肠能量转化|肝脏代谢|器官功能分区|能量景观|分子细胞生物学|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
小肠能量转化|肝脏代谢|器官功能分区|能量景观|分子细胞生物学|生命科学
我们的身体,远非教科书上那些色彩均一的器官图谱。与其说它们是静态的组织块,不如将它们想象成一座座繁华而复杂的都市。肝脏是化学工业中枢,日夜不停地处理着营养物质与毒素;小肠则是一条精密的自动化生产线,从食物中汲取生命所需的能量。在这些“都市”内部,不同的街区承担着截然不同的功能,拥有独特的资源供给和能量消耗模式。长期以来,我们对这些内部“地理”的认知,如同只有一张粗略的行政区划图,无法看清其内在的能量流动与地形起伏。但如果我们能绘制一张精细到细胞级别的“能量地形图”,标示出哪里是能量充沛的高地,哪里是资源匮乏的洼地,我们是否就能找到疾病悄然萌芽的那个“原点”?
最近,普林斯顿大学的Joshua D. Rabinowitz实验室就扮演了这样一群“新世界制图师”的角色。他们在《自然》杂志上发表的研究,如同一颗深空探测器,首次为我们传回了肝脏与小肠内部详尽的“代谢地形图”。
他们使用的核心技术是高分辨率MALDI成像质谱,可以将其想象成一台“分子GPS”。这台设备能以极高的精度(在小肠中达到10微米,接近单个细胞的尺度)扫描组织切片,并“读取”出每一点上成百上千种代谢物的化学身份和丰度。然而,面对海量的数据点,如何将它们组织成一张有意义的地图,是巨大的挑战。
为此,团队开发了一种名为MET-MAP的无监督深度学习算法。这个聪明的AI无需预先告知组织结构,仅凭代谢物自身的空间分布特征,就能自主“重建”出组织的生理轴线,比如肝脏中从门静脉到中央静脉的路径,或是小肠中从隐窝到绒毛顶端的梯度。其工作原理,就如同地理学家通过分析各地的海拔数据,最终绘制出连绵的山脉与深邃的峡谷。
最终,一幅前所未见的画卷展开了:在肝脏和小肠中,超过九成的代谢物都存在着显著的空间梯度。这意味着,细胞的功能状态并非一成不变,而是与其所处的“地理位置”息息相关。代谢,不再是抽象的生化通路图,而成为了一幅可视、可量化的动态地貌。
这张“能量地形图”讲述了两个截然不同的故事。
肝脏:一座高压运转的化学工厂
肝脏的基本功能单元是肝小叶,血液从边缘的门静脉流入,汇向中心的中央静脉。这条路径天然形成了氧气和营养的浓度梯度,也造就了功能分区的“能量地貌”。
小肠:一条分工明确的生命流水线
小肠上皮细胞从隐窝的干细胞“工厂”诞生,沿着绒毛这条“传送带”向上迁移,最终在绒毛顶端完成使命并脱落。这一过程也形成了鲜明的代谢分工。
这张地图最激动人心的应用,在于它能实时追踪营养物质如何在体内“旅行”并改变“地形”。研究团队以常见的果糖为例,揭示了饮食如何引发局灶性的代谢风险。
当小鼠口服同位素标记的果糖后,仅仅90秒,信号就出现在小肠绒毛的底部,果糖在这里被迅速分解为果糖-1-磷酸(F1P)。然而,小肠的处理能力是有限的,部分未被分解的果糖会搭上门静脉的“快车”直达肝脏。
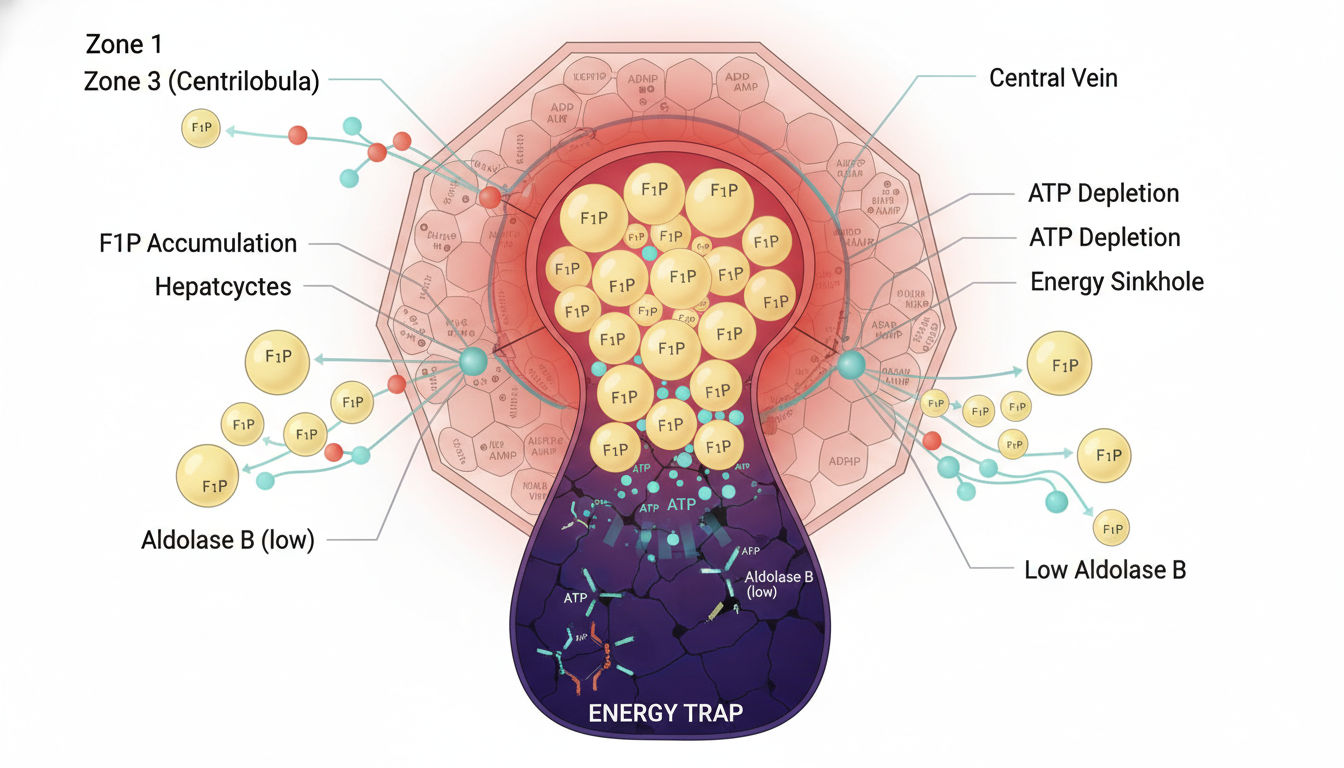
灾难性的变化发生在肝脏的中央静脉区(Zone 3)。F1P在这里大量积聚,形成一个“能量陷阱”。因为该区域负责清除F1P的醛缩酶B水平较低,导致F1P无法被有效处理。细胞为了磷酸化果糖,会疯狂消耗ATP,但后续能量再生的通路却被堵塞。最终,这片区域陷入了严重的局部能量耗竭,形成了一个危险的“能量洼地”。
这个发现意义重大。它首次在空间上清晰地指出了,高果糖负荷并非均匀地影响整个肝脏,而是精准地攻击了其代谢链条上的薄弱环节——中央静脉区。这为理解非酒精性脂肪肝等代谢疾病为何会从特定位置开始,提供了坚实的解剖学和代谢学基础。
这张“能量地形图”不仅描绘了健康状态,更以前所未有的清晰度揭示了疾病的潜在起点。一个区域的代谢特征,决定了它在面对外界压力时的脆弱性。
这一点在肝癌研究中得到了印证。德克萨斯大学西南医学中心的Hao Zhu教授团队发现,肝癌最容易起源于肝脏的Zone 3区域。这并非偶然。因为Zone 3的细胞长期处于低氧环境,进化出了一套独特的抗氧化能力,尤其对一种名为“铁死亡”的细胞死亡方式有更强的抵抗力。这种抵抗力在正常情况下是保护机制,但在基因突变发生时,却让癌变细胞获得了生存优势,使其更容易在这里“安营扎寨”,最终形成肿瘤。
结合Rabinowitz团队的研究,我们看到了一幅完整的图景:Zone 3不仅是高果糖负荷下的“能量洼地”,也是具备独特抗死亡能力的“避难所”。这种独特的代谢微环境,使其成为了多种肝脏疾病的空间起点。我们不再仅仅说“代谢紊乱导致了疾病”,而是可以精确地指出:“在肝脏中央静脉区,由于能量耗竭和对铁死亡的抵抗,为脂肪变性和癌症的发生提供了温床。”这为理解疾病的发生提供了精准的空间坐标系。
绘制出第一张地图仅仅是开始。未来的挑战与机遇在于如何整合更多维度的信息,创造一幅更加全面、动态的生命图景。
多组学融合:生命活动的复杂性远超单一层面。将揭示基因表达的空间转录组学、描绘蛋白质功能的空间蛋白质组学与空间代谢组学相结合,是必然趋势。然而,不同技术平台的数据如同语言不通的旅行者,如何让他们有效对话是一大难题。为此,浙江大学刘琬璐团队开发的SpatialMETA等人工智能算法应运而生,它们能够像一位“全能翻译”,融合不同模态、不同批次的数据,构建出统一、连贯的多维空间地图,揭示从基因到功能再到代谢的完整调控链条。
AI的角色演进:人工智能不仅是数据整合的工具,更是探索的引擎。未来,AI或能基于海量的组织病理图像,直接“预测”出其背后的代谢状态和基因表达谱,极大地降低科研和诊断成本。Owkin等公司正在构建的大规模空间组学数据库和多模态大模型,正是为了训练出能够洞察疾病本质的“AI病理学家”。
这一切最终将指向精准干预。当医生能够清晰地看到患者肝脏Zone 3区域出现了能量耗竭的早期信号,或许就可以通过靶向药物或精准营养干预,在病变形成之前就“填平”这个能量洼地。治疗将不再是全身性的模糊调节,而是针对特定空间节点的精准打击。
空间代谢组学及其与多组学的融合,正带领我们开启一场对自身内部世界的“地理大发现”。我们第一次能够如此真切地“看见”能量在组织内的流动、分配与消耗,看见生命在微米尺度上建立起的精妙秩序。这张“能量地形图”告诉我们,健康是一种动态的平衡,而疾病,往往始于这片复杂地形上某个最脆弱的节点。我们不再是自身健康的盲人摸象者,而是手持高清地图的探索者,正站在一个全新时代的入口,准备以前所未有的视角,去解读、守护和修复我们身体里这片广袤而神奇的星辰大海。