对抗知识焦虑,从看懂这条开始
App 下载
胰腺癌恶变有了明确拐点,早干预能拦下来
纪念斯隆凯特琳癌症中心|祖细胞样状态|KRAS突变|五年生存率|胰腺导管腺癌|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
纪念斯隆凯特琳癌症中心|祖细胞样状态|KRAS突变|五年生存率|胰腺导管腺癌|肿瘤学|医学健康
你可能没听过胰腺导管腺癌,但一定听过它的恐怖——五年生存率仅13%,超过80%的患者确诊时已是晚期。这种癌症像个潜伏的刺客,从最初的基因突变成型,要偷偷发展十几年,等你察觉腹痛、黄疸时,它早已站稳脚跟。
但2026年4月,美国纪念斯隆凯特琳癌症中心的研究团队,在《Cell》杂志上捅破了这层窗户纸:他们在小鼠模型里精准抓住了胰腺癌从良性转向恶性的那个“三岔路口”——祖细胞样状态。这个发现,第一次让我们有机会在它彻底失控前,伸手把人拉回来。
你可以把胰腺里的正常细胞想象成安分守己的上班族,KRAS突变就像有人在办公室里点燃了一根烟——一开始只是小骚动,细胞会立刻启动“灭火系统”:p53、CDKN2A这些抑癌基因会激活,迫使细胞进入“衰老状态”,相当于让冒烟的工位停工,防止火势蔓延。
但研究人员在小鼠体内发现了一群特殊的“纠结细胞”:它们一边被KRAS突变推着往癌变方向跑,高表达致癌基因程序;一边又被抑癌基因死死拽住,疯狂启动抑癌反应。这种矛盾的共激活状态,就是祖细胞样状态——它不是严格意义上的良性或恶性,而是两种力量的角斗场。
更关键的是,这些细胞不会乖乖待在原地角斗。它们会悄悄给周围环境“换血”:激活成纤维细胞制造致密的纤维瘢痕,吸引免疫抑制细胞形成“免疫特区”,甚至提前重构细胞外基质——这些变化在肿瘤还没成型时就已完成,相当于为癌变提前铺好了路。
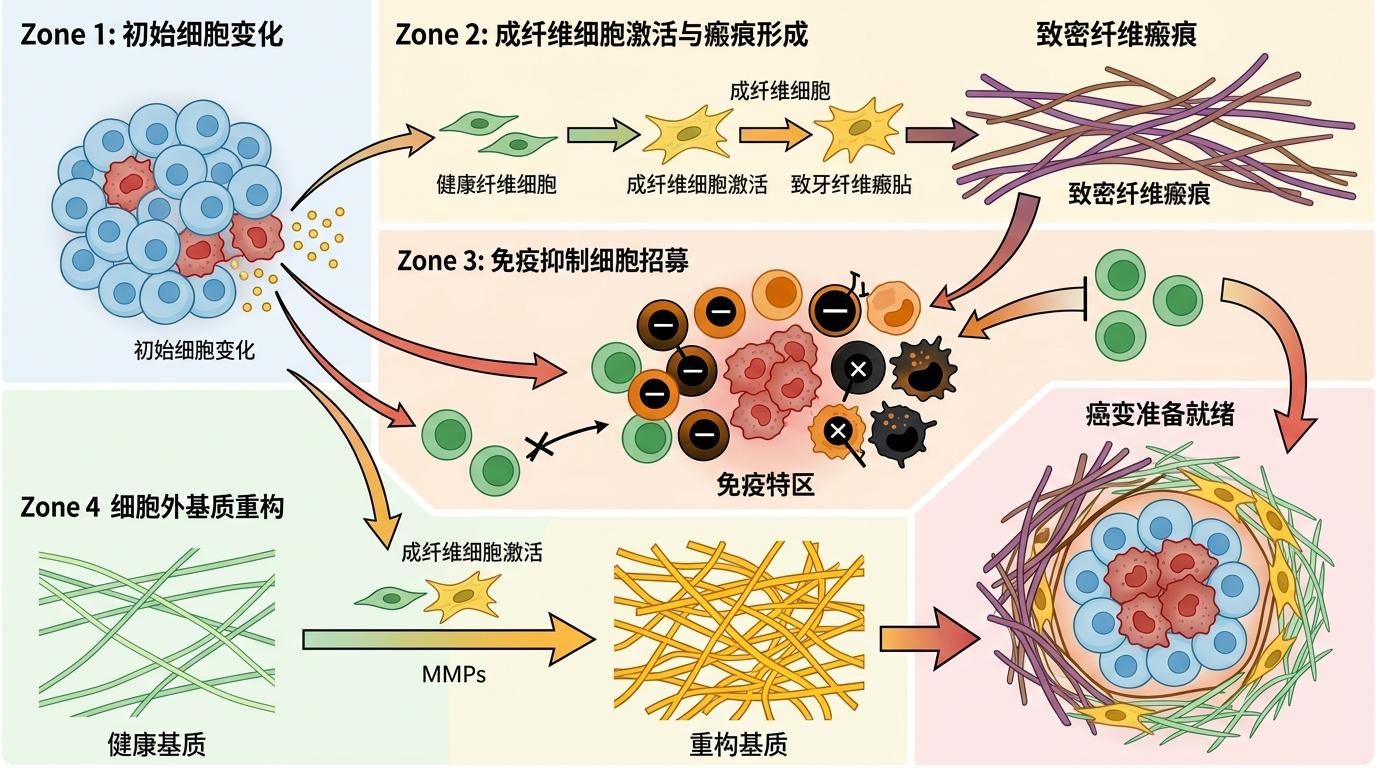
过去我们以为,癌症是基因突变一步步累积的结果,就像多米诺骨牌倒下,一旦启动就无法逆转。但这次的研究彻底打破了这个认知:祖细胞样状态是一个可逆的临界点。
研究者在小鼠模型里做了个实验:给处于癌前病变的小鼠短期使用KRAS抑制剂MRTX1133,仅仅3天,祖细胞样细胞就被清除了,它们辛辛苦苦构建的“恶变温床”也随之瓦解。后续观察发现,这些小鼠的癌症发生时间被大幅推迟——换算成人类时间,相当于延缓了好几年。
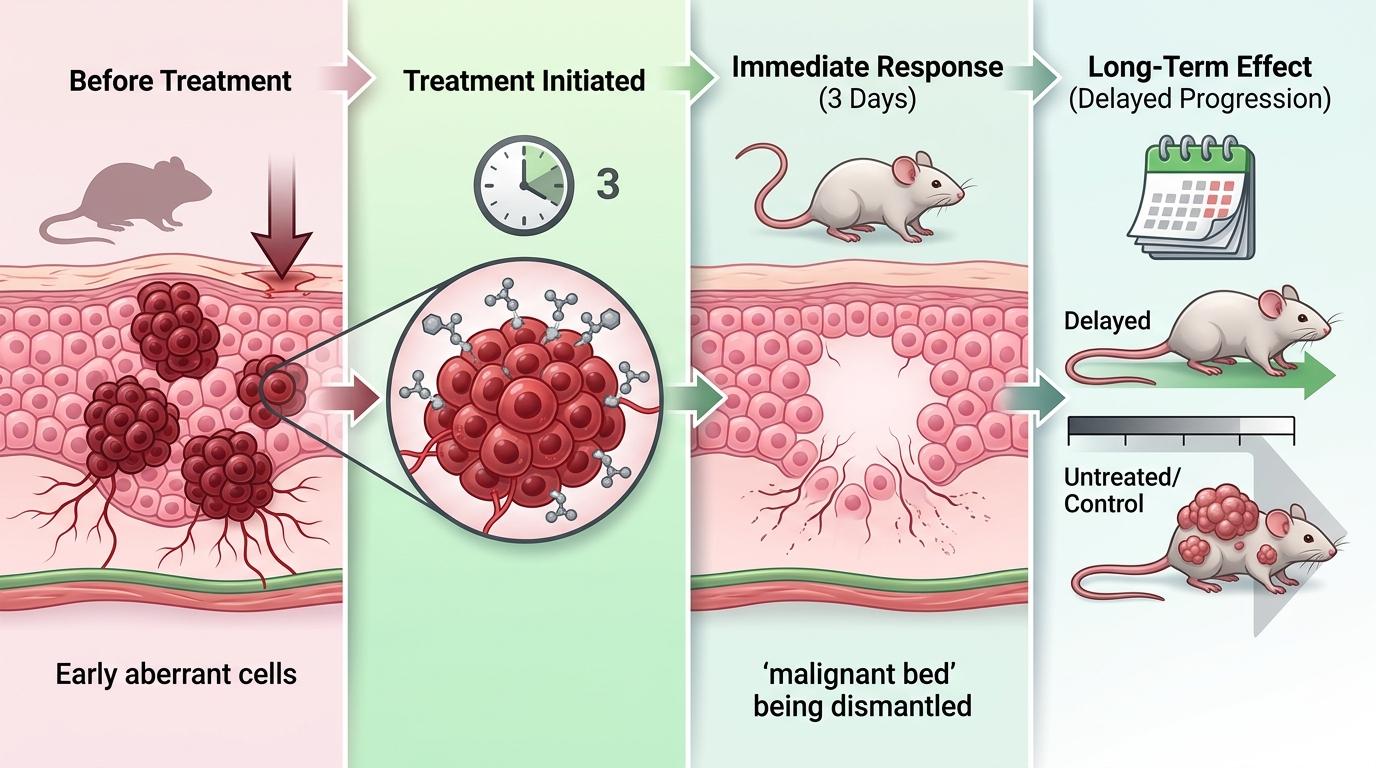
而p53基因在这里扮演着“裁判”的角色:如果p53功能正常,它会逼着祖细胞样细胞进入衰老,终止角斗;一旦p53失活,就像裁判离场,致癌力量立刻占据上风,细胞会启动上皮-间质转化,获得迁移和侵袭能力,疯狂加速恶变。这也解释了为什么约50%的胰腺癌患者会伴有p53失活突变——它们直接跳过了最关键的刹车环节。
更让人兴奋的是,这些干预手段并非遥不可及:KRAS G12D抑制剂MRTX1133已经进入临床试验,p53激活剂APR-246也在多种癌症的测试中显示出潜力。甚至针对微环境的药物,比如FAK抑制剂、CXCR2拮抗剂,都能通过破坏祖细胞样细胞的生存环境,阻断恶变进程。
当然,要抓住这个干预窗口,首先得找到处于祖细胞样状态的人。这也是胰腺癌早筛的最大难点:早期病变没有明显症状,传统的CT、MRI很难发现毫米级的异常,血液标志物CA19-9的特异性又太低。
但这次的研究给了我们新的方向:祖细胞样状态的细胞会表达特定的表面标记物,比如uPAR,它们还会向血液中释放独特的微环境蛋白。通过液体活检捕捉这些信号,再结合患者的KRAS突变情况、家族史等信息,就能精准筛选出高风险人群。
更值得关注的是,研究人员开发的空间转录组学技术,能在组织层面精准定位祖细胞样细胞的位置和周围微环境的变化——这意味着未来我们或许能在患者还没有任何症状时,就通过无创或微创的手段,找到那个即将“叛变”的细胞群体。
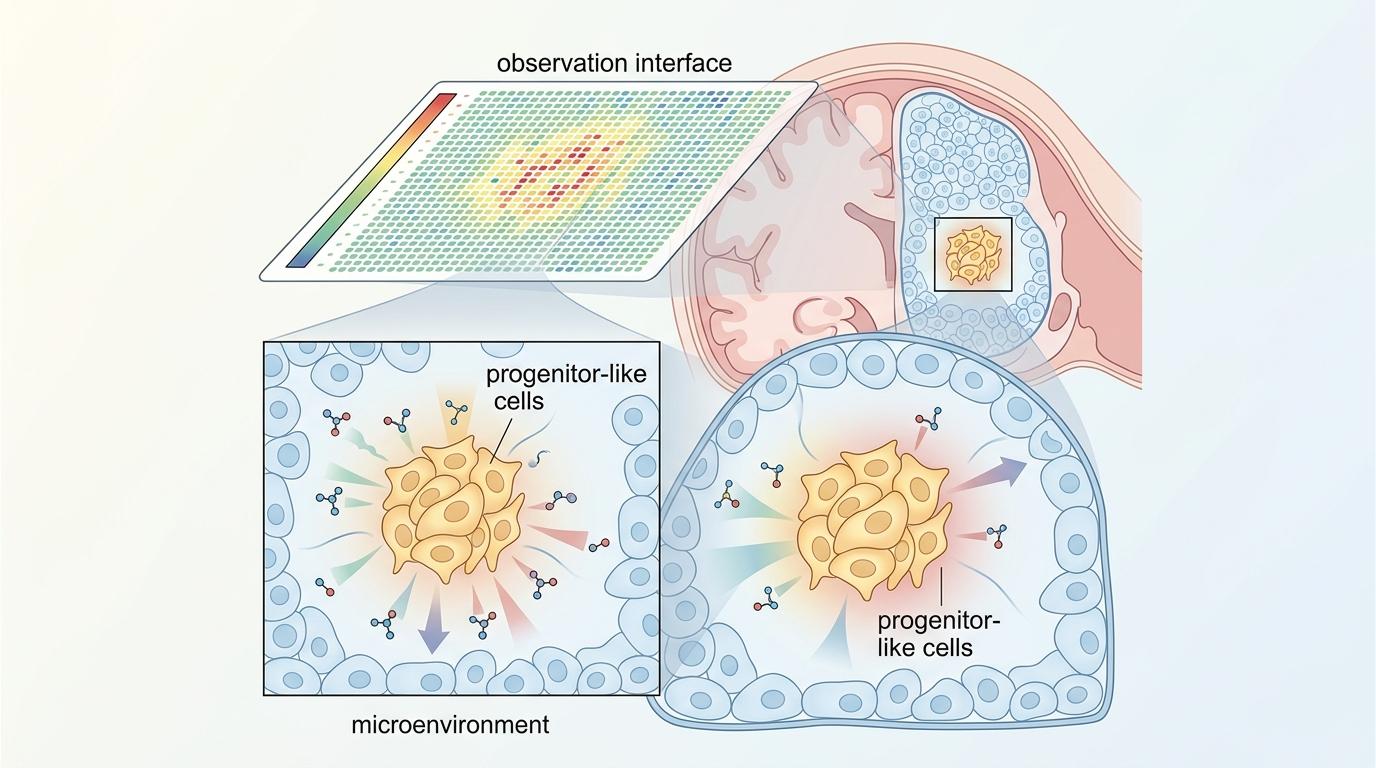
过去我们谈起胰腺癌,总是绕不开“绝症”“凶癌”这些词,仿佛一旦沾边就只能听天由命。但这次的研究,第一次把“主动权”交回了我们手里:原来它的恶变不是一场突如其来的海啸,而是一条有明确拐点的小路,我们完全可以在拐点处设卡,把它拦在良性的这一侧。
早发现不是终点,早干预才是希望。未来的胰腺癌防治,或许不再是等到肿瘤形成后再“杀敌一千自损八百”,而是在它还处于萌芽状态时,就用精准的药物掐断恶变的苗头。这不仅能大幅提升患者的生存率,更能让那些携带KRAS突变、有家族史的高风险人群,不用再活在对癌症的恐惧里。