
6 天前

6 天前
亚马逊雨林的黄昏里,一只Anopheles darlingi蚊落在伐木工的小臂上——它是南美50万疟疾感染者的“递刀人”。过去十年,美洲疟疾病例数纹丝不动,眼看就要消除疟疾的国家接连折戟,人们把账算在疟原虫抗药性头上,却忽略了这只蚊子的本事:它能把喷在蚊帐上的杀虫剂像代谢酒精一样分解掉。哈佛医学院的团队测序了1094只这种蚊子的全基因组,终于揭开了它躲过人命防线的核心秘密——这和非洲疟蚊的抗药路数,完全不是一回事。
研究人员从法属圭亚那到秘鲁的6个国家抓回蚊子,测序结果一出来就推翻了之前的猜测:这些看起来一模一样的蚊子,其实是遗传差异极大的8个地理种群,就像分布在南美大陆的8支独立部队,彼此间的遗传分化程度,甚至超过非洲两种疟蚊的物种差异。
安第斯山脉、流域边界是天然的隔离带,让它们几乎不交换基因——这意味着某个种群练出的抗药本事,很难扩散到其他区域,但反过来,每个种群都可能独立进化出自己的抗药技能。更意外的是,之前担心的“隐存种”根本不存在,所有蚊子都是同一个物种,只是在不同的环境里,硬生生演化出了迥异的生存策略。
最显眼的是13个大型染色体倒位——你可以把它想象成一段DNA被剪下来、翻转后再粘回去。这些倒位就像打包好的“生存工具箱”,里面装着适应不同环境的基因组合:有的帮蚊子在干旱地区活下来,有的专门对付杀虫剂。在农业密集区,某个倒位里的基因频率特别高,那里的蚊子,正靠着这套工具箱分解农药。
非洲疟蚊抗杀虫剂,通常是靠“靶点突变”——就像把杀虫剂的“锁孔”给堵上,让杀虫剂找不到地方发挥作用。但南美这只疟蚊,走了条完全不同的路:它靠的是“代谢解毒”。
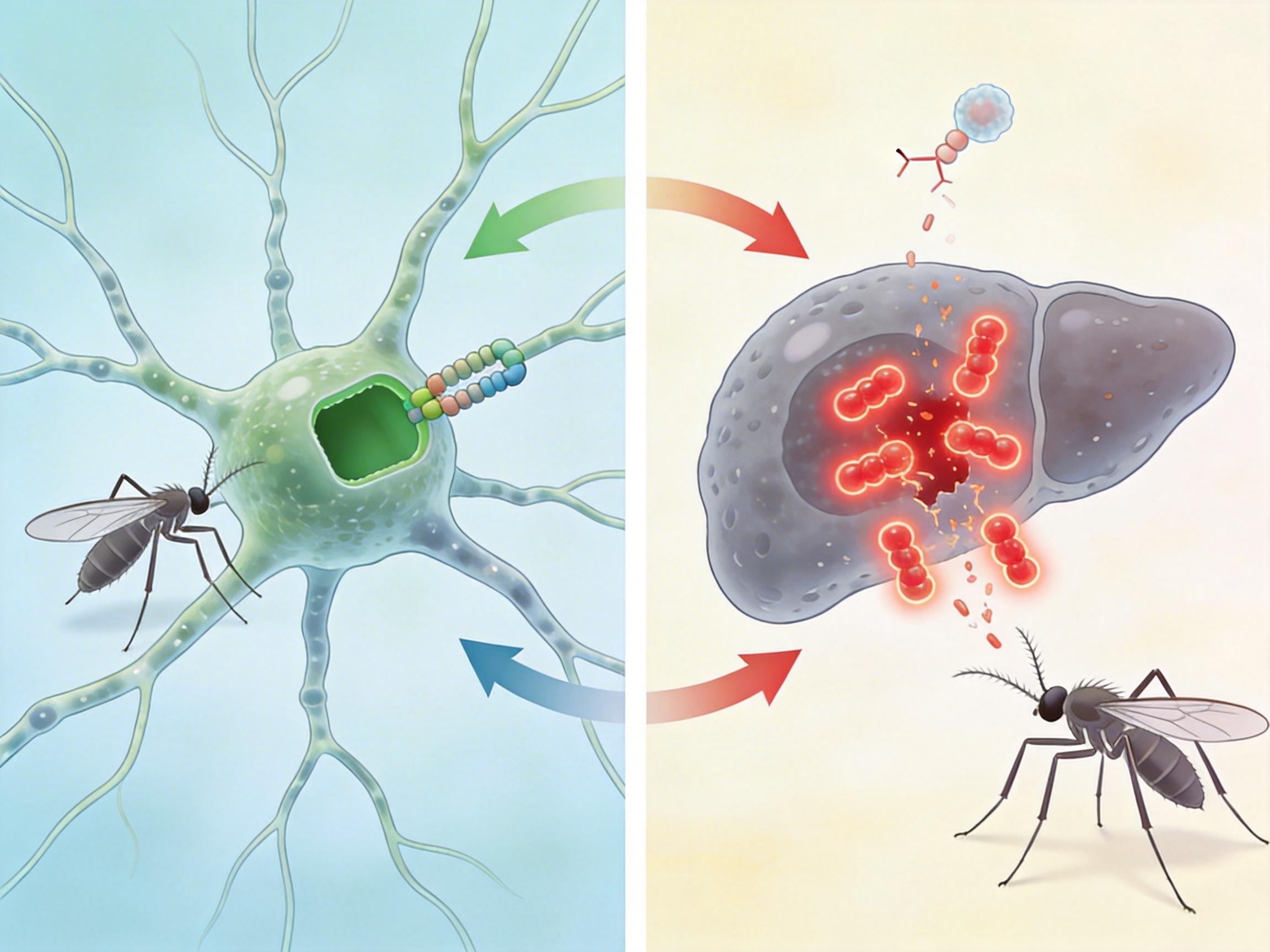
你可以把蚊子的细胞色素P450基因想象成一个“解毒酶工厂”。当杀虫剂进入蚊子体内,这个工厂就开足马力生产酶,把杀虫剂分解成无毒的物质排出体外。研究人员在多个种群里都发现了P450基因的强烈选择信号,尤其是CYP6AA1基因,只要它带上一个特定的突变,蚊子对拟除虫菊酯类杀虫剂的耐受性就会显著提升。
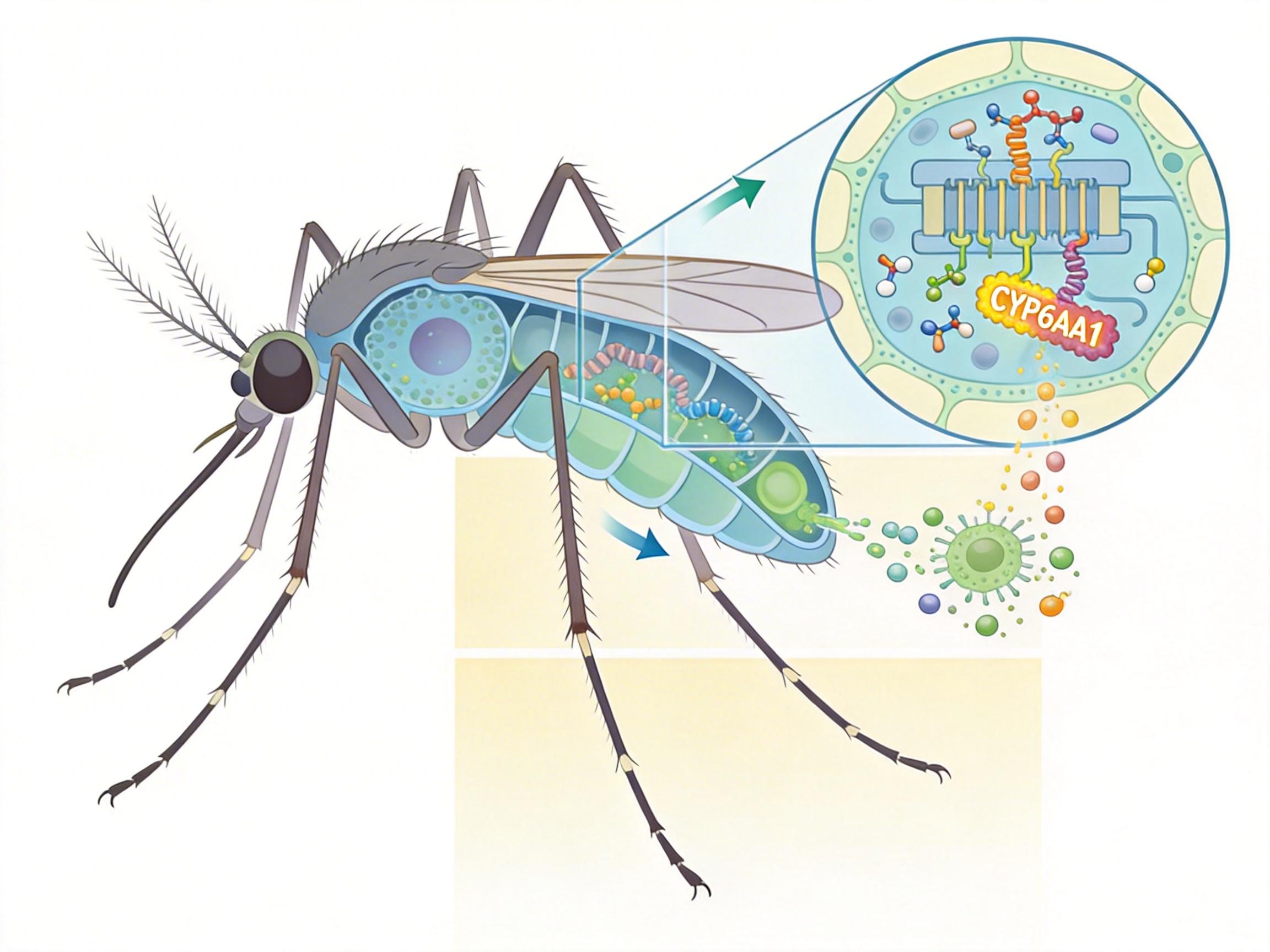
更麻烦的是,这个“工厂”的启动开关,可能被农业杀虫剂给按亮了。南美农田里大量使用的农药,和防控疟疾的杀虫剂是同一类,蚊子在农田边的水体里产卵,幼虫从小就接触低剂量农药,相当于一直在“锻炼”解毒能力。等到它们长大,再遇到蚊帐上的杀虫剂,自然轻松应对。
过去的防控策略,就像用同一把枪打不同的靶子——在南美大陆通用的杀虫剂,到了某个种群面前可能完全失效。现在有了基因组数据,终于可以精准狙击了。
比如,针对依赖P450解毒的种群,可以在杀虫剂里加入P450抑制剂,就像给解毒工厂断了电,让杀虫剂重新发挥作用。而针对不同地理种群的遗传差异,基因驱动技术的使用也得调整:因为种群间基因流动少,不能指望一个驱动基因传遍整个大陆,得在不同区域分别释放适配当地种群的基因驱动蚊子。
但挑战也摆在眼前:代谢抗药性不像靶点突变那样有明确的分子标记,很难用简单的方法监测;农业和公共卫生杀虫剂的交叉污染,更是给蚊子提供了持续的“锻炼”机会。如果不把农业用药和疟疾防控整合起来,再精准的技术,也赶不上蚊子进化的速度。
当我们把蚊子钉在显微镜下测序时,它们正跟着人类的足迹,在森林边缘、农田和矿区之间扩散。南美疟蚊的抗药之路,本质上是人类活动刻在它们基因里的印记:我们砍倒森林、喷洒农药,给它们创造了进化的温床,最后又要花更大的力气,去堵上自己留下的漏洞。
比蚊子更难对付的,是人类自己的惯性。 要消除疟疾,我们不仅要读懂蚊子的基因,更要改变和自然相处的方式——毕竟,蚊子的进化速度,永远快于我们单一的防控手段。
点击充电,成为大圆镜下一个视频选题!