对抗知识焦虑,从看懂这条开始
App 下载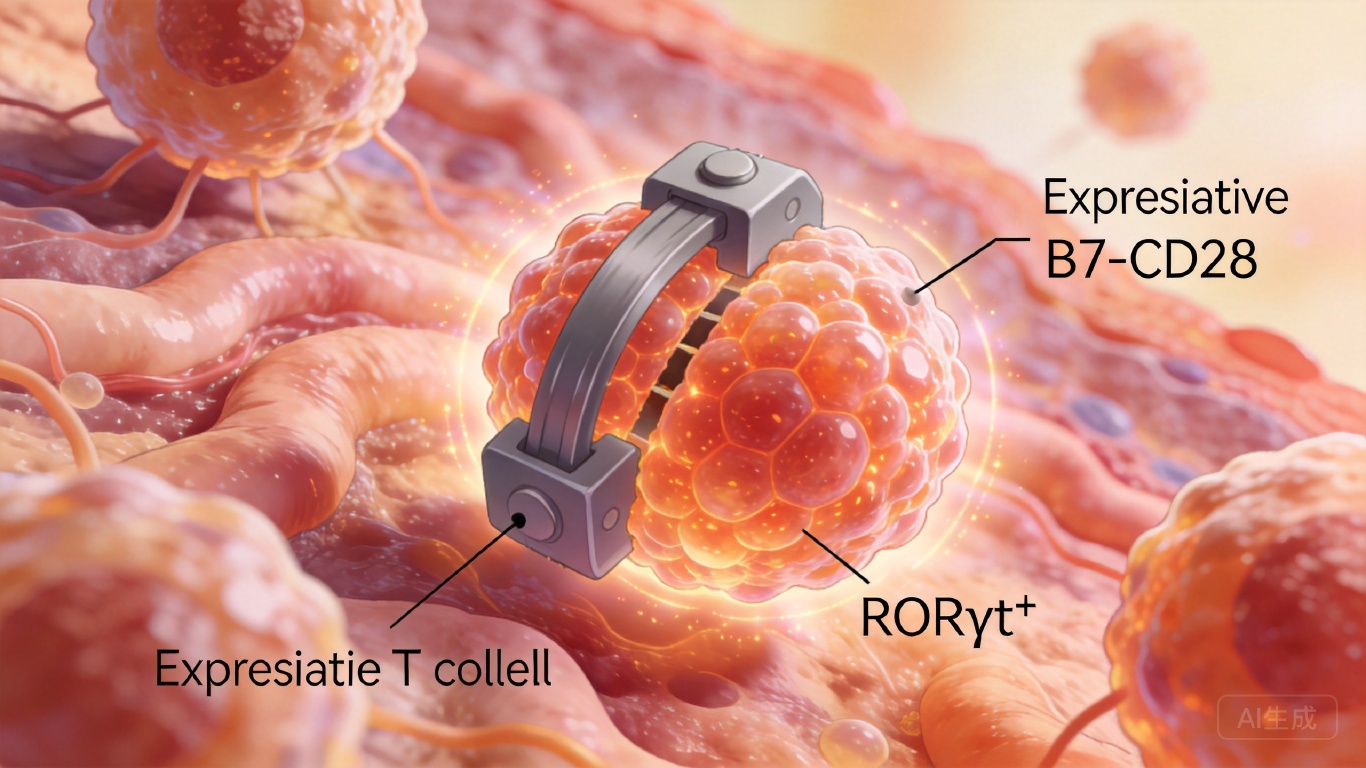
肠道免疫的刹车:共刺激信号竟抑制耐受细胞
威尔康奈尔医学院|吕梦泽|共刺激信号|肠道耐受|RORγt⁺ Treg细胞|免疫学基础|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
威尔康奈尔医学院|吕梦泽|共刺激信号|肠道耐受|RORγt⁺ Treg细胞|免疫学基础|生命科学
当你吞下一口食物,肠道里正在上演一场精密的谈判:免疫系统要放过共生的万亿细菌和无害的食物蛋白,同时揪出致命的致病菌。这场平衡的关键,是一群叫RORγt⁺ Treg的免疫细胞——它们像肠道的“维和部队”,专门阻止免疫系统“误伤友军”。2025年,这类细胞的研究拿下诺贝尔生理或医学奖,可科学家一直没搞懂:这些“维和部队”到底听谁指挥?直到2026年,威尔康奈尔医学院吕梦泽博士的团队给出了答案,这个答案直接推翻了免疫学沿用数十年的经典理论。
过去十年,免疫学课本里写着:肠道里的“维和部队”RORγt⁺ Treg,是由树突状细胞这类传统抗原递呈细胞“训练”出来的。但2022年吕梦泽团队在《自然》的研究率先捅破了这个误区:真正指挥“维和部队”的,是一群叫RORγt⁺ APC的特殊细胞——它们像肠道里的“外交官”,专门负责把细菌和食物蛋白的“身份信息”递交给免疫细胞,诱导出针对性的RORγt⁺ Treg。
你可以把这个过程想象成:树突状细胞是街头巡逻的警察,遇到可疑分子就直接亮警灯;而RORγt⁺ APC是社区调解员,手里攥着居民花名册,能精准认出“自己人”,再专门训练一批维和队员盯着这些熟人。实验数据更直白:如果把小鼠体内的RORγt⁺ APC去掉,肠道里的RORγt⁺ Treg会直接减少80%,小鼠很快就会患上严重的结肠炎。
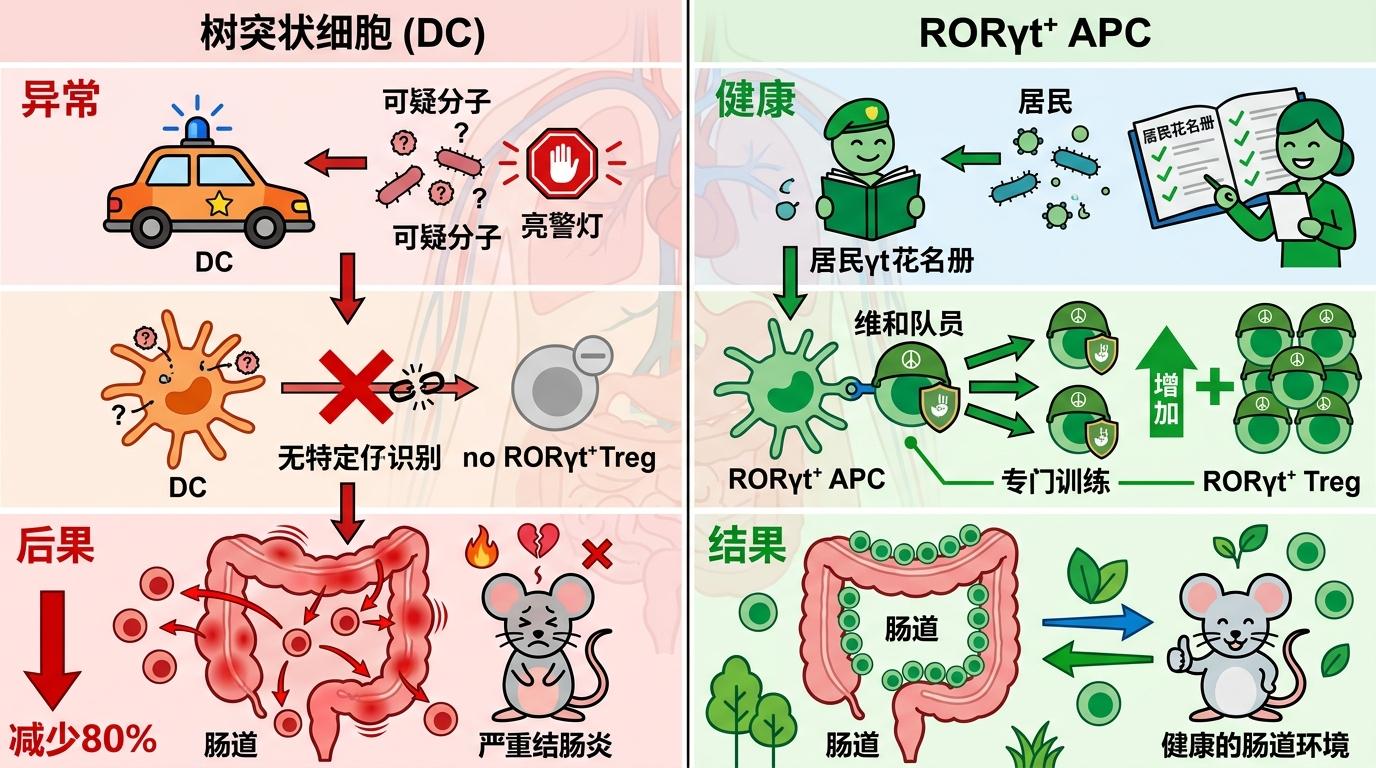
但当时的研究还留下一个漏洞:这些“外交官”除了递身份信息,还会不会给“维和部队”发别的指令?
经典免疫学有个铁律:T细胞的激活需要两个信号——第一个是抗原递呈(“身份识别”),第二个是共刺激信号(“出发指令”),后者就像踩油门,推着细胞快速增殖。但吕梦泽团队2026年发表在《实验医学杂志》的研究显示,在肠道的RORγt⁺ Treg这里,这个油门变成了刹车。
他们做了三组实验:第一组用抗体阻断共刺激信号的关键分子B7,结果肠道里的RORγt⁺ Treg直接翻倍;第二组给小鼠敲除B7基因,RORγt⁺ Treg的增殖速度比正常小鼠快3倍;第三组先去掉RORγt⁺ APC,再阻断B7信号,RORγt⁺ Treg却毫无变化。
答案清晰了:只有在RORγt⁺ APC完成“身份识别”(信号一)的前提下,阻断“出发指令”(信号二),才能让RORγt⁺ Treg大量增殖,建立肠道耐受。简单说就是:先认人,再按住油门,维和部队才能安心干活。
这也解释了一个临床难题:治疗自身免疫病的药物CTLA4-Ig,能阻断B7信号,却在炎症性肠病(IBD)患者身上收效甚微——因为这些患者的肠道里,RORγt⁺ APC已经被炎症破坏,没了“身份识别”,再怎么踩刹车也没用。
这个新范式虽然解决了旧问题,却也抛出了更多问号。比如,RORγt⁺ APC本身是个大家族,包括ILC3细胞、Thetis细胞等多个亚群,到底哪个亚群才是诱导RORγt⁺ Treg的主力?不同年龄段的RORγt⁺ APC功能会不会变化?婴儿肠道里的“外交官”是不是比成年人更活跃?
更关键的是临床转化:怎么才能精准恢复IBD患者肠道里的RORγt⁺ APC?是直接补充细胞,还是用药物激活它们?吕梦泽团队已经在小鼠实验里验证了联合策略的有效性:先给小鼠补充RORγt⁺ APC,再用CTLA4-Ig阻断B7信号,结肠炎的缓解率能从30%提升到85%。但这套方案要用到人身上,还需要解决细胞来源、免疫排斥等一系列问题。
还有一个容易被忽略的细节:肠道菌群对RORγt⁺ APC的影响极大。无菌小鼠的肠道里,RORγt⁺ APC的数量只有正常小鼠的三分之一;而补充短链脂肪酸这类细菌代谢产物,能让RORγt⁺ APC的活性提高2倍。这意味着,未来的治疗可能要把细胞疗法、药物和益生菌结合起来,才能真正稳住肠道的免疫平衡。
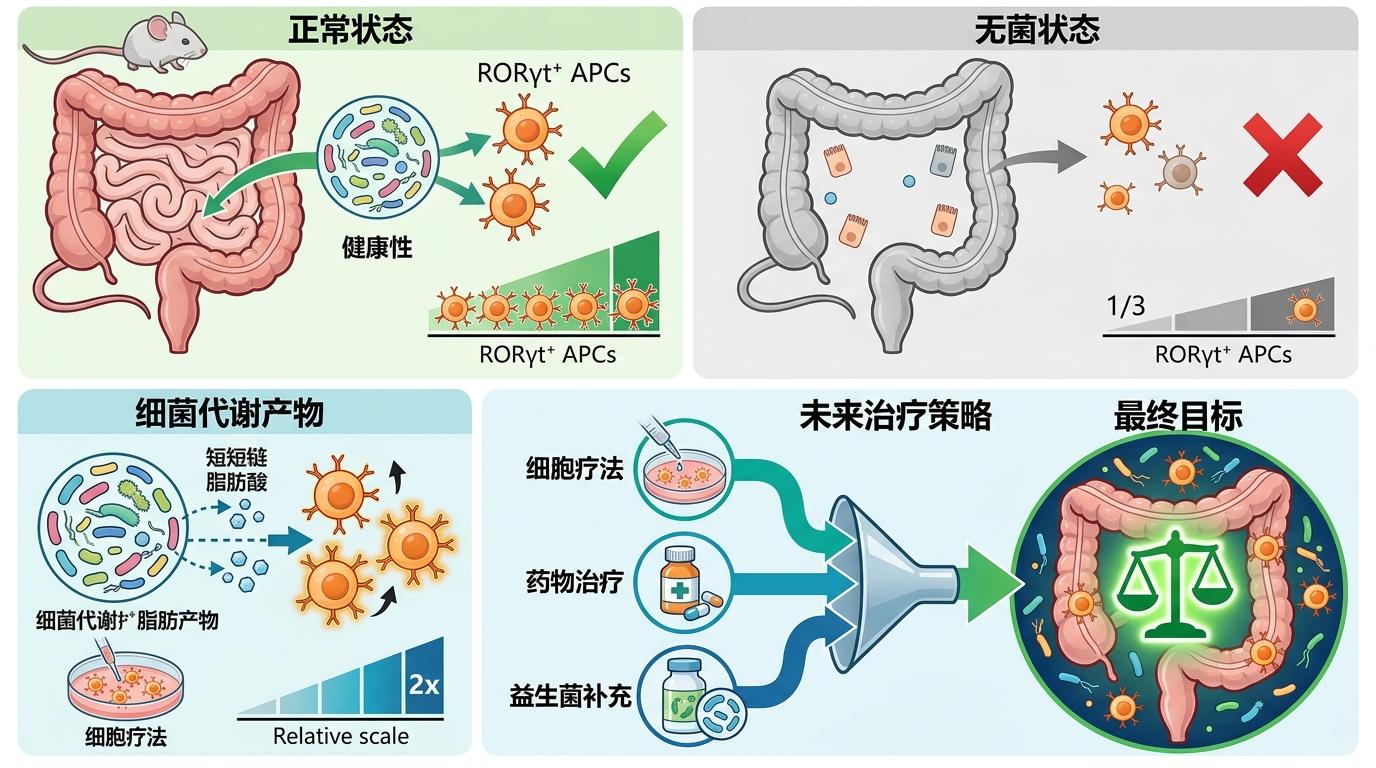
当我们谈论免疫系统时,总爱用“战争”来比喻:免疫细胞是战士,病原体是敌人,炎症是战场。但肠道的免疫耐受告诉我们,免疫系统的本质从来不是消灭,而是平衡。
吕梦泽团队的研究,就像在这场“战争”里发现了一套全新的指挥系统——原来真正的和平,不是靠不断增兵,而是先搞清楚“自己人”是谁,再按住冲动的扳机。免疫的最高智慧,是懂得何时停止攻击。
未来的某一天,当医生给IBD患者开的药方里,既有免疫药物,也有益生菌,甚至还有定制的RORγt⁺ APC时,我们会想起这场关于“刹车”的发现——它不仅改写了免疫学课本,更让我们离真正的精准医疗,又近了一步。