对抗知识焦虑,从看懂这条开始
App 下载
百万分之一的骨病,藏着人体的平衡密码
全身骨骼异常|多学科协作|基因失控|视神经受压|骨干皮质增厚|罕见遗传病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
全身骨骼异常|多学科协作|基因失控|视神经受压|骨干皮质增厚|罕见遗传病|医学健康
26岁的姑娘带着一双突出的眼睛走进诊室时,没人能立刻把她的症状串起来:15年的四肢骨痛、越来越差的听力,还有被外院诊断的甲状腺和性腺功能低下。眼科检查发现她的视神经正在被挤压,眼眶CT显示骨壁像被无形的手反复压实,连视神经管都窄成了一条缝。更奇怪的是,全身X光片里,她的每根长骨都像被裹了一层厚厚的水泥——对称性的骨干皮质增厚,从大腿到手臂无一幸免。这不是单一器官的故障,而是一场全身骨骼的「异常增生风暴」。医生们很快意识到,他们面对的是一种百万分之一的罕见病,而解开谜题的钥匙,藏在基因和多学科协作的交叉点上。
你可以把骨骼想象成一座不断翻新的房子:成骨细胞负责添砖加瓦,破骨细胞负责拆旧翻新,而TGF-β1就是管着这两队工人的监工。它平时以「潜伏」状态存在于骨基质里,只有在骨需要修复时才被激活,精准调控新旧骨骼的替换节奏。
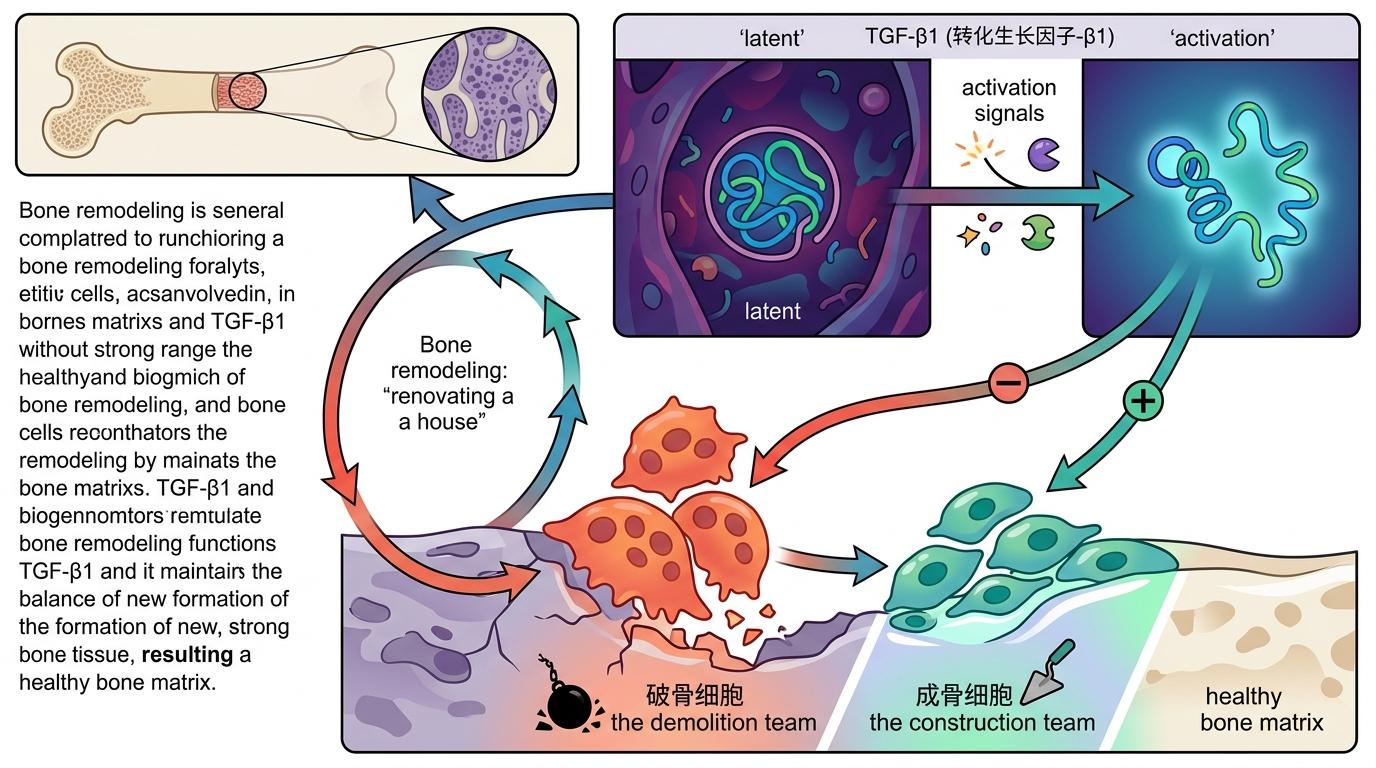
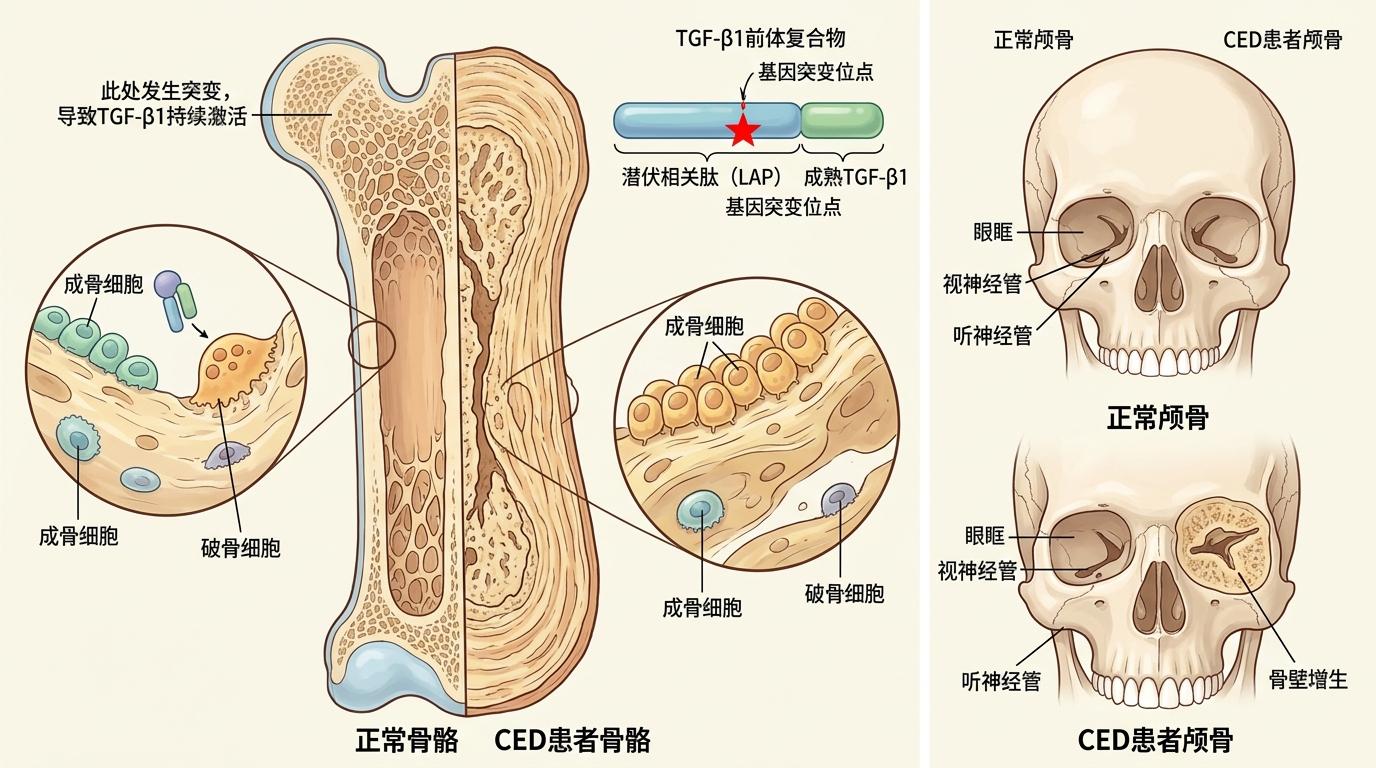
但Camurati-Engelmann病(CED)患者的TGFB1基因,偏偏在「监工的休眠开关」上出了错——突变集中在潜伏相关肽(LAP)区域,就像监工被拔掉了电源,24小时处于亢奋状态。过量激活的TGF-β1会疯狂指挥成骨细胞造骨,同时抑制破骨细胞拆旧,结果就是骨骼只长不消:长骨的骨干被越裹越厚,骨髓腔被挤得越来越窄;颅骨的骨壁不断增生,把眼眶、视神经管、听神经管都挤成了狭窄的通道。
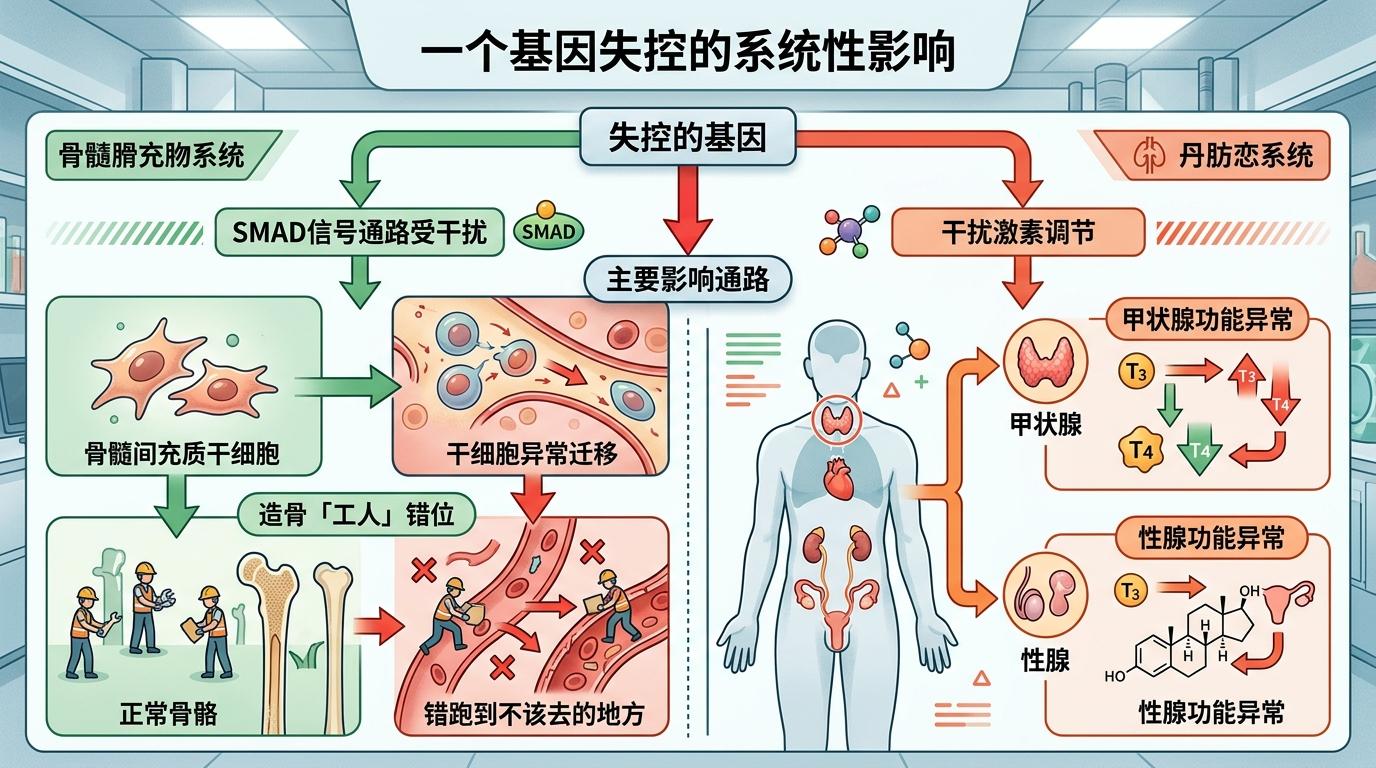
更关键的是,这个基因的失控不是单一维度的。它会通过SMAD信号通路影响骨髓间充质干细胞的迁移,让造骨的「工人」错跑到不该去的地方;还会干扰激素调节,这也是为什么患者会出现甲状腺、性腺功能异常。
最让医生困惑的,是这种病的「千人千面」。同样携带TGFB1的Arg218热点突变,有的孩子3岁就出现严重骨痛,连走路都困难;有的成年人只是体检时偶然发现骨骼增厚,几乎没有症状;还有的患者像这次的姑娘一样,以眼球突出为首发症状,差点被当成甲状腺疾病误诊。
这种表型异质性背后,藏着两个关键:一是基因的「不完全外显」——有的携带者虽然有突变,但身体的其他调控机制能勉强维持平衡,不会出现明显症状;二是「遗传期待」现象,家族里的后代往往发病更早、症状更重,就像失控的监工在代际传递中变得越来越亢奋。
更有意思的是,患者母亲在妊娠期间症状曾明显缓解。这提示激素水平可能是调控TGF-β1活性的另一把钥匙——雌激素或许能暂时按住失控的监工,只是这背后的具体机制,还需要更多研究去破解。
对于CED这类罕见病,单靠一个科室的力量几乎不可能确诊。这次的病例中,眼科发现眼球突出后,立刻召集了内分泌科、分子诊断科、骨科、影像科、耳鼻喉科的医生一起会诊——内分泌科排除了单纯的激素紊乱,骨科确认了全身骨骼的特征性改变,分子诊断科最终通过基因测序锁定了TGFB1的突变,影像科则精准定位了视神经受压的位置。
这种多学科协作不是简单的科室叠加,而是一场「精准拼图」:每个科室拿出自己的碎片,最终拼出完整的疾病画像。确诊后的治疗同样需要多学科配合:内分泌科调控激素水平,眼科监测视神经功能,骨科评估骨骼病变进展,一旦出现视力急剧下降,耳鼻喉科和眼科还需要联手做眼眶减压手术。
更值得关注的是,目前的治疗还只能停留在「缓解症状」层面:糖皮质激素能减轻炎症和骨痛,但长期使用会导致骨质疏松;洛沙坦能部分抑制TGF-β1信号,但疗效因人而异。真正的靶向治疗,还需要更深入地解析TGF-β1信号通路的调控网络。
当我们谈论罕见病时,我们谈论的不只是百万分之一的概率,更是人体这个复杂系统里最精密的平衡。一个基因的微小突变,就能引发全身骨骼的连锁反应;而解开这个谜题,需要的不只是先进的检测技术,更是打破科室壁垒的协作思维。
对于CED患者来说,确诊只是第一步,后续的长期管理、药物研发,还有更多未知等待探索。但这个病例也提醒我们:那些看似孤立的症状背后,可能藏着同一个根源;而医学的进步,往往就从关注这些「小众」的患者开始。
平衡一旦打破,全身都会买单。