对抗知识焦虑,从看懂这条开始
App 下载
肾癌耐药的幕后推手,竟是这种微环境细胞
肿瘤微环境|靶向药耐药|载脂蛋白E|癌症相关成纤维细胞|肾癌|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
肿瘤微环境|靶向药耐药|载脂蛋白E|癌症相关成纤维细胞|肾癌|肿瘤学|医学健康
晚期肾癌患者最害怕的场景,莫过于靶向药突然失效——原本被压制的肿瘤卷土重来,却再也找不到有效的武器。作为泌尿系统第三大恶性肿瘤,肾癌的靶向治疗已经卡了十年:以舒尼替尼为代表的一线药物,总会在半年到一年后遭遇耐药,患者五年生存率不足10%。
没人知道耐药的根源究竟藏在哪里,直到北大和安徽医科大学的团队把目光从肿瘤细胞本身,转向了它周围的「土壤」——肿瘤微环境。他们在肾癌患者的肿瘤组织里,揪出了一群伪装成「普通基质细胞」的帮凶:高表达载脂蛋白E(ApoE)的癌症相关成纤维细胞(CAF)。正是这群细胞,在暗中给肿瘤细胞「充电」,让它们变得更顽固、更耐药。
过去十年,科学家一直把CAF当成肿瘤微环境里的「路人甲」——一种只会给肿瘤细胞提供物理支撑的基质细胞。直到单细胞测序技术普及,人们才惊觉:CAF根本不是单一群体,而是一群分工明确的「帮凶团伙」。
你可以把肿瘤微环境想象成一个黑暗的工厂:肿瘤细胞是躲在里面的「老板」,而CAF就是负责跑腿、放风、提供原料的「员工」。其中,肌成纤维样CAF(myCAF)负责加固工厂围墙,让药物和免疫细胞进不来;炎症型CAF(iCAF)负责分泌免疫抑制因子,把巡逻的免疫细胞赶跑;而这次发现的ApoE高表达CAF,是专门给「老板」输送「营养液」的「后勤主管」。
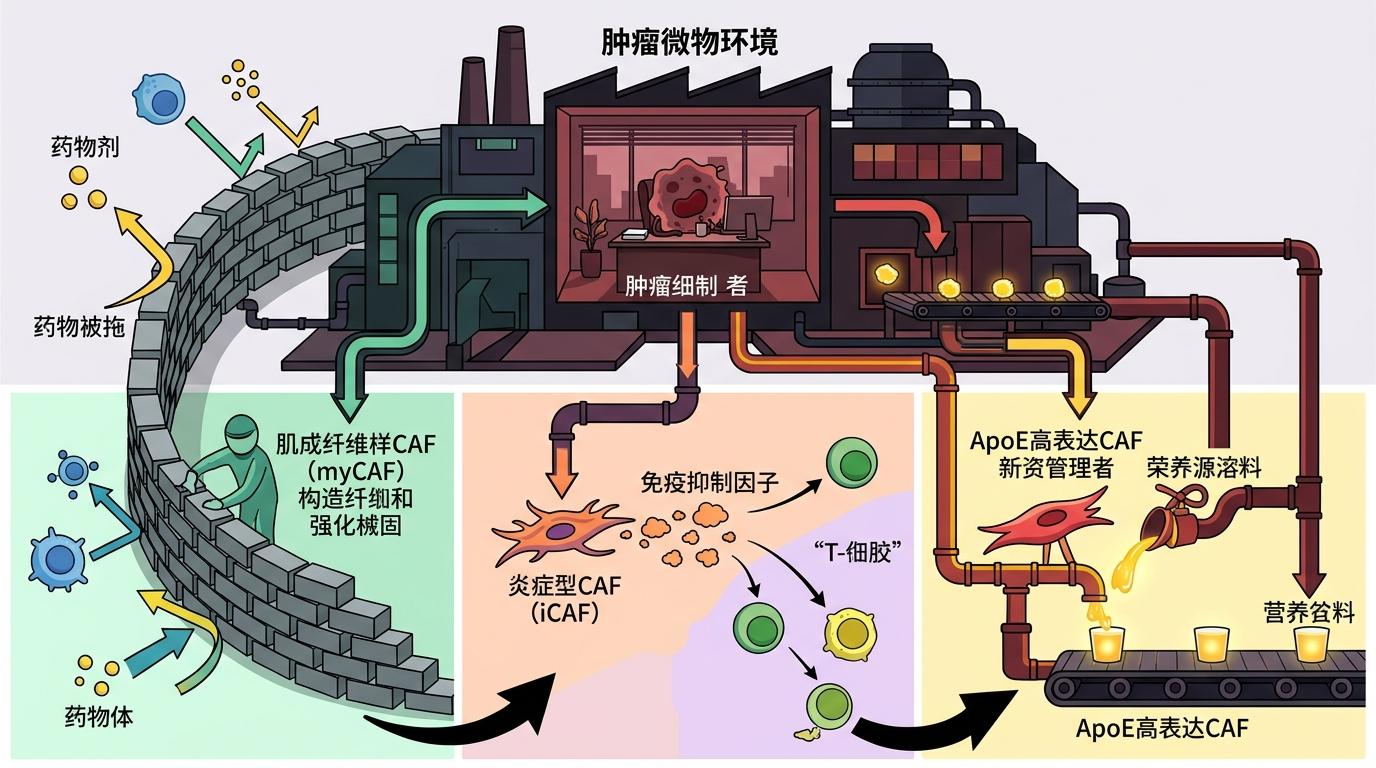
研究团队通过单细胞RNA测序和流式细胞术,从肾癌患者的肿瘤组织里精准分选出了这群ApoE高表达CAF。临床数据显示,肿瘤里这类细胞越多,患者的预后就越差:五年生存率比没有这类细胞的患者低了整整30%。更关键的是,它们和舒尼替尼的耐药性直接相关——这类细胞含量高的患者,靶向药的有效时间平均缩短了4个月。
ApoE高表达CAF到底是怎么给肿瘤细胞「充电」的?研究团队做了一个简单的实验:把这类细胞和肾癌肿瘤细胞放在同一个培养皿里,结果发现肿瘤细胞的「干性」突然增强了——它们像干细胞一样,能不断自我复制,还能分化成不同类型的肿瘤细胞,这正是耐药和复发的根源。
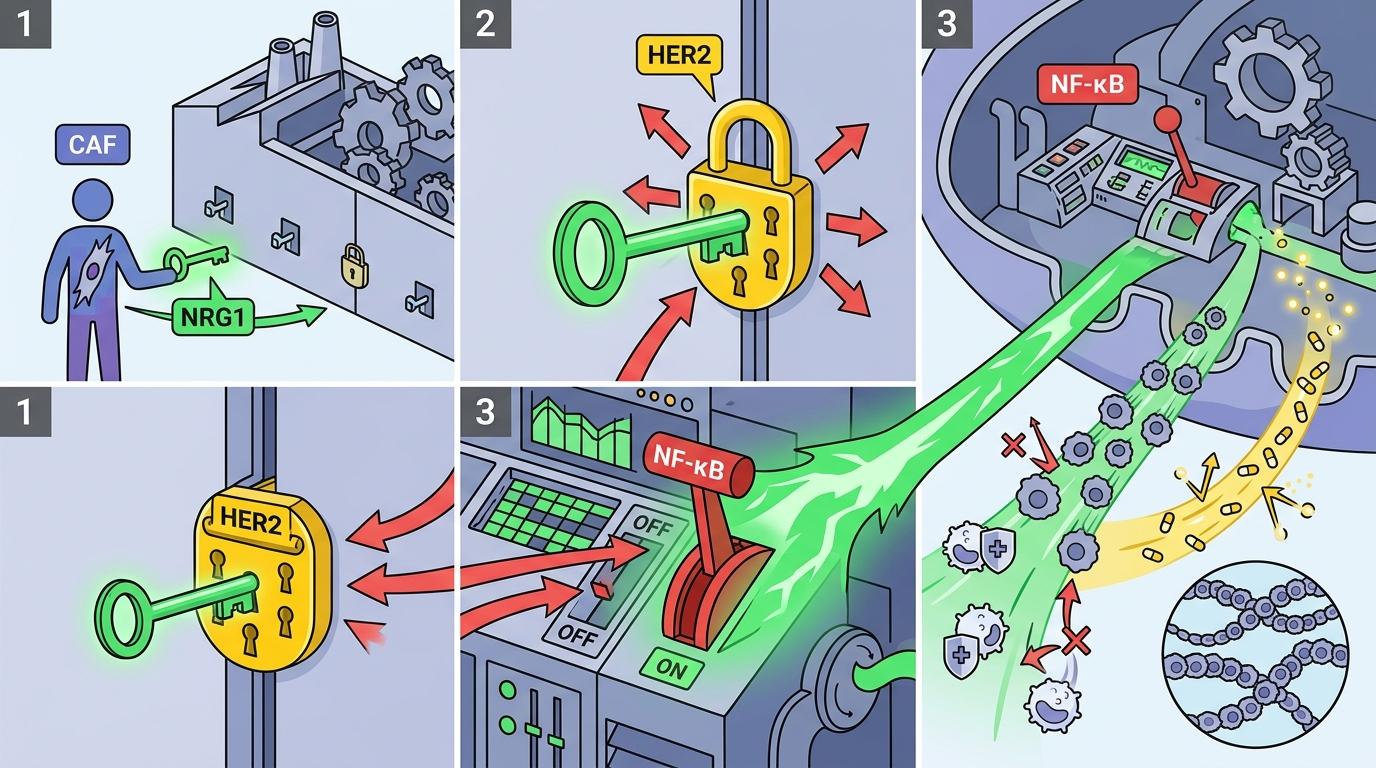
追踪下去,科学家找到了关键的「营养液」:神经调节蛋白1(NRG1)。ApoE高表达CAF会大量分泌这种蛋白,当它碰到肿瘤细胞表面的HER2受体时,就像按下了一个开关,激活了细胞内部的NF-κB信号通路。
你可以把这个过程想象成:CAF是站在工厂外的「送货员」,NRG1是它递进去的「钥匙」,HER2是肿瘤细胞门上的「锁孔」,而NF-κB就是打开「干性仓库」的「开关」。一旦开关被按下,肿瘤细胞就会源源不断地获得「永生能力」,不仅能躲避免疫细胞的攻击,还能对靶向药产生抗性。
更精准的实验数据验证了这个机制:当研究团队用RNA干扰技术敲低CAF里的NRG1,或者用抑制剂阻断NF-κB通路时,肿瘤细胞的干性特征立刻减弱了70%;在小鼠模型里,用抗体中和NRG1后,舒尼替尼的治疗效果提升了40%,肿瘤体积缩小了一半以上。
这个发现最有价值的地方,在于它给晚期肾癌的治疗提供了一个全新的思路:与其盯着肿瘤细胞本身,不如先改造它周围的「土壤」——精准清除ApoE高表达CAF,或者切断它给肿瘤细胞输送「营养液」的通路。
不过,这条路并不容易走。最大的挑战在于CAF的「伪装术」:它们和正常组织里的成纤维细胞长得太像了,现有的标志物(比如α-SMA、FAP)在正常细胞上也有表达,直接靶向很可能会误伤无辜。研究团队发现,ApoE高表达CAF的形成是由转录因子NRF1调控的,这或许是一个更精准的靶点——只需要阻断NRF1的活性,就能阻止普通CAF变成「帮凶」。
另一个挑战是通路的「交叉性」:NRG1/HER2/NF-κB通路不仅在肾癌里起作用,在乳腺癌、肺癌等其他肿瘤里也扮演着类似的角色,但具体的调控机制可能略有不同。比如在HER2阳性乳腺癌里,CAF分泌的NRG1会导致曲妥珠单抗耐药,机制和肾癌类似,但靶向的时机和剂量可能需要调整。
目前,针对NRG1的中和抗体已经进入了早期临床试验,而针对NRF1的抑制剂还在实验室阶段。不过,研究团队已经在小鼠模型里证明了联合治疗的潜力:把NRG1中和抗体和舒尼替尼一起使用,不仅能显著延缓耐药的出现,还能把小鼠的生存期延长一倍以上。
当我们把目光从肿瘤细胞本身移开,才发现肿瘤微环境里藏着太多被忽略的细节。这些看似无关紧要的基质细胞,其实是肿瘤最顽固的「盟友」——它们不仅给肿瘤细胞提供营养,还帮它们建立起对抗药物和免疫细胞的「防御工事」。
「改土优于除虫」,这句农业领域的老话,正在肿瘤治疗的领域里得到新的验证。未来的癌症治疗,或许不再是单纯地「杀死肿瘤细胞」,而是通过改造肿瘤微环境,让肿瘤细胞失去生存的「土壤」。对于晚期肾癌患者来说,这不仅意味着延长生存期,更意味着看到了治愈的希望。