对抗知识焦虑,从看懂这条开始
App 下载
人类大脑进化之谜:新神经干细胞揭示双引擎协同
抑制性神经元|人类大脑进化|脑室下区放射状胶质细胞|北京协和医院朱兰院士团队|清华大学米达团队|神经生物学|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
抑制性神经元|人类大脑进化|脑室下区放射状胶质细胞|北京协和医院朱兰院士团队|清华大学米达团队|神经生物学|生命科学
大脑,这个重约1.4公斤的宇宙级超级计算机,如何在数百万年间膨胀三倍,孕育出语言、艺术和科学?2026年初,一项研究揭开了谜底:人类认知王国的扩张,竟源于两类隐藏的“建筑师”——它们如同精密协同的引擎,推动神经元数量与多样性的爆发式增长。
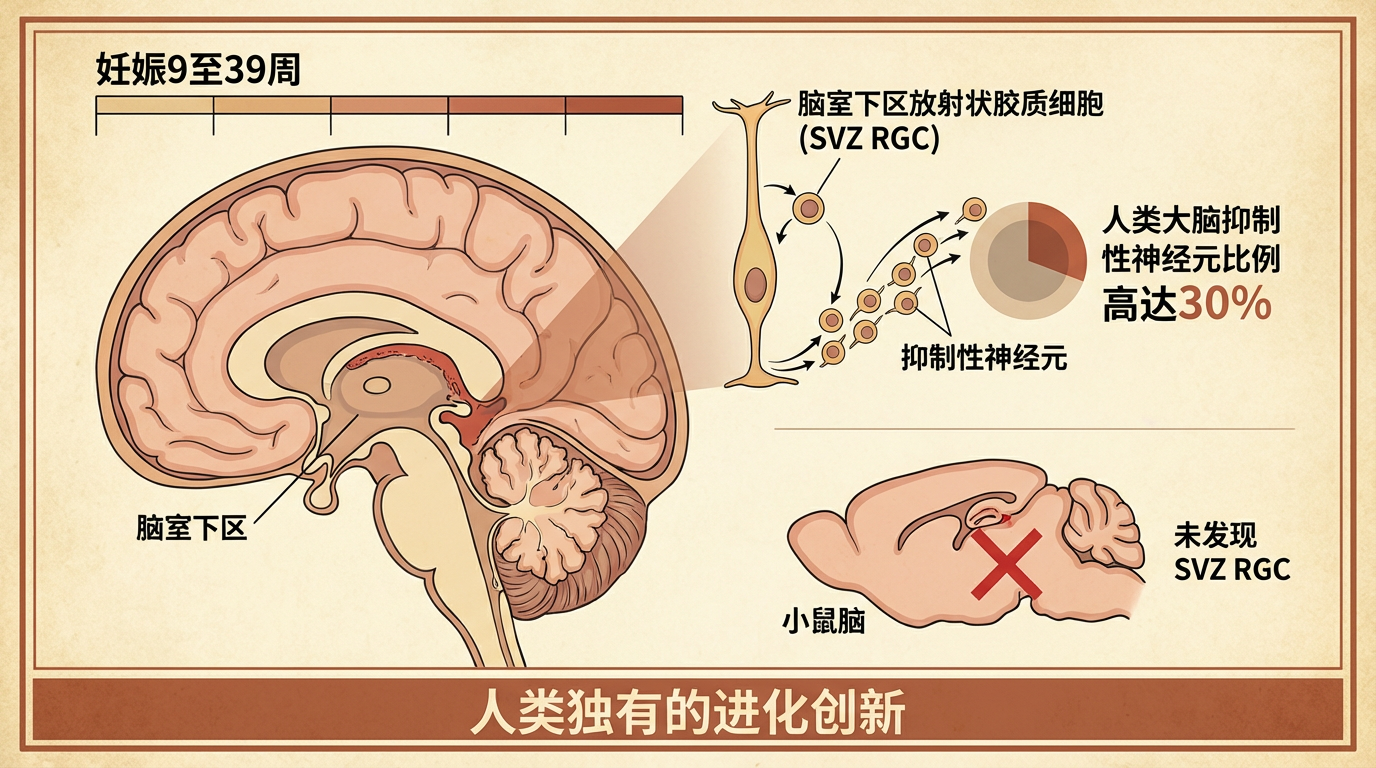
2026年1月16日,清华大学米达团队联合北京协和医院朱兰院士团队在《科学》期刊发表里程碑研究。通过分析妊娠9至39周的人类胎儿脑样本,他们首次发现一种仅存于灵长类大脑的神经干细胞——脑室下区放射状胶质细胞(SVZ RGC)。这种细胞在胚胎期持续分裂,源源不断产生抑制性神经元,使人类大脑抑制性神经元比例高达30%,远超其他哺乳动物。令人惊讶的是,小鼠脑中竟找不到它的“亲戚”,暗示这是人类独有的进化创新。
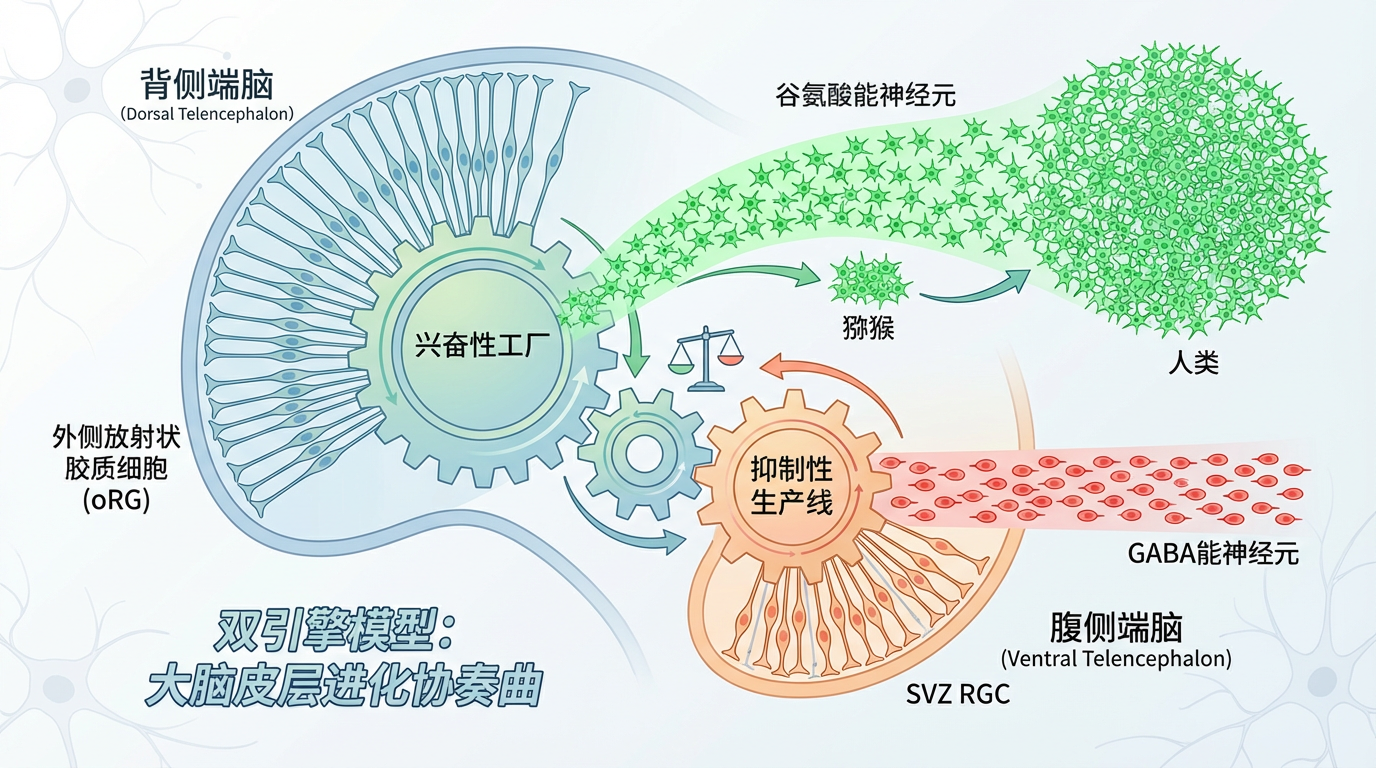
研究提出颠覆性的“双引擎模型”:背侧端脑中,外侧放射状胶质细胞(oRG)化身“兴奋性工厂”,批量制造谷氨酸能神经元;腹侧端脑里,新发现的SVZ RGC成为“抑制性生产线”,专门生产GABA能神经元。两者如同精密齿轮——oRG推动神经元数量从猕猴的17亿跃升至人类的160亿,SVZ RGC则确保抑制性神经元比例同步提升,避免神经网络陷入混乱。中国科学院院士时松海惊叹:“这不是简单的数量堆砌,而是两类干细胞在时空舞台上演绎的进化协奏曲。”
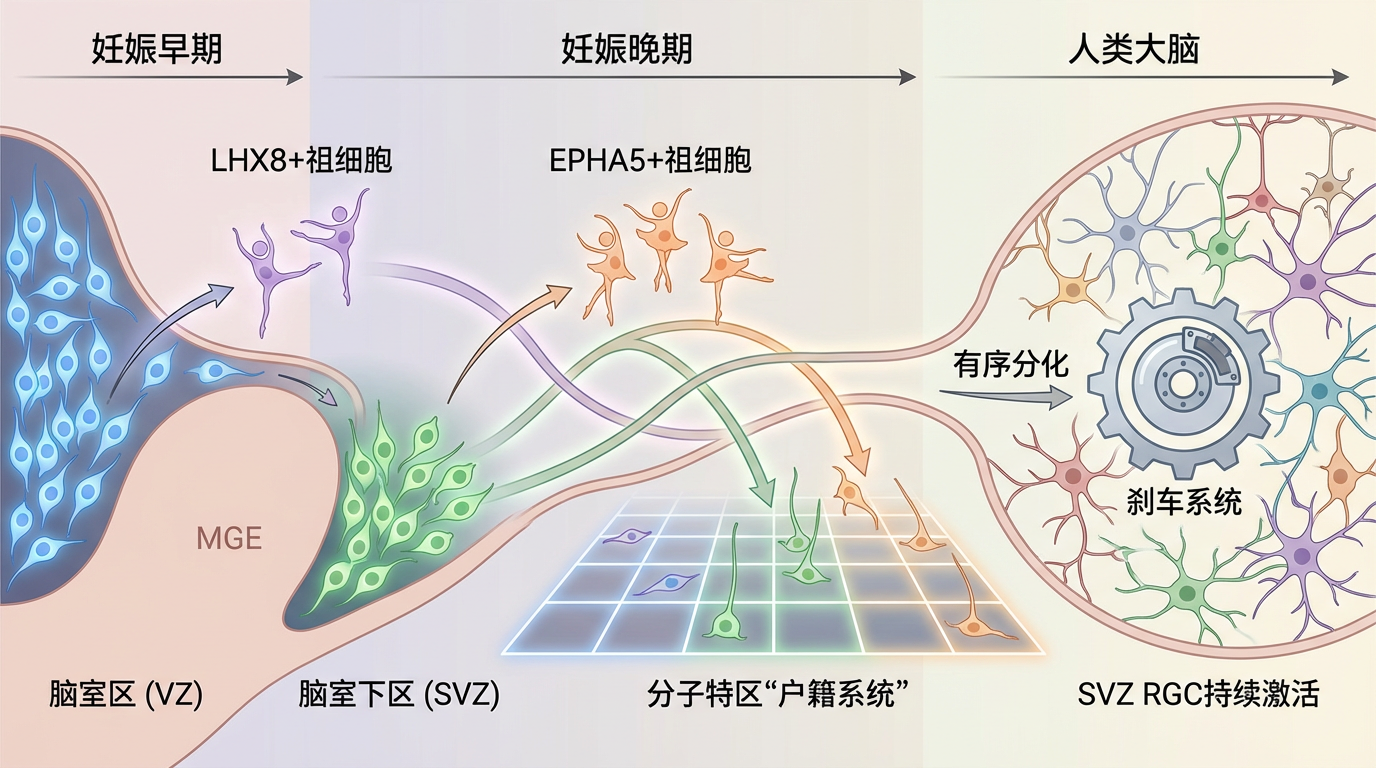
抑制性神经元的诞生竟像一场精心编排的芭蕾。内侧神经节隆起(MGE)脑区中,神经祖细胞域严格按“出生时间”和“出生地”决定细胞命运:妊娠早期,脑室区LHX8+祖细胞率先登场;妊娠晚期,脑室下区EPHA5+祖细胞接过接力棒。空间转录组图谱显示,这些区域如同分子特区的“户籍系统”,确保数百种抑制性神经元亚型有序分化——当SVZ RGC持续激活时,人类大脑才获得调控复杂思维的“刹车系统”。
幕后指挥这场进化盛宴的,是交织的信号网络。ERK和PKA通路如同“加速踏板”,维持oRG细胞的自我更新;YAP信号则像“转换器”,引导干细胞向胶质细胞分化。关键的是VCAM1分子——它在放射状胶质细胞中持续表达,像细胞命运的“锚点”,通过调控β-catenin信号决定干细胞该增殖还是休眠。一旦这些通路失调,大脑扩张的精密程序便会崩解。
抑制性神经元如同交响乐团的指挥棒,维持着神经网络的兴奋-抑制平衡。研究发现,锥体神经元膜电位的轻微波动,竟能通过轴突上的D-电流“放大器”,调节抑制性反馈强度。这种动态平衡一旦打破,便会引发癫痫或自闭症——正如自闭症患者脑中抑制性神经元功能缺损,导致神经信号如脱缰野马。上海生科院舒友生团队的电生理实验揭示:人脑的高效认知,正源于这种微秒级的电化学博弈。
这项发现正点燃医学革命的导火索。由于SVZ RGC的异常与癫痫、孤独症密切相关,科学家已着手设计靶向疗法:在类器官模型中移植改造后的SVZ RGC细胞,成功修复了异常的神经环路。更激动人心的是,瑞士团队用诱导干细胞衍生的神经前体治疗脑损伤小鼠,运动功能竟恢复近70%——人类首次窥见再生医学修复大脑的路径。但挑战犹存:如何精准控制移植细胞的分化方向?这个悬念将成为下阶段攻关焦点。
尽管双引擎模型照亮了进化迷宫的入口,深层谜题依然盘旋:神经干细胞如何感知进化压力调整增殖周期?抑制性神经元亚型的精细调控网络仍笼罩在迷雾中。正如张旭院士所言:“我们刚读懂进化写下的第一章。”当基因编辑技术CRISPR开始解锁神经元DNA修复密码,人类站在了认知新纪元的门槛——理解大脑不仅为了治愈疾病,更是回答“何以成为人类”的哲学叩问。这场探索终将证明,最宏大的宇宙图景,正藏匿于最微小的细胞协作中。