对抗知识焦虑,从看懂这条开始
App 下载
肠道缺血再灌注损伤,纳米平台实现双相精准治疗
肠道屏障|氧化风暴|重庆医科大学|纳米颗粒|肠缺血再灌注损伤|临床诊疗技术|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
肠道屏障|氧化风暴|重庆医科大学|纳米颗粒|肠缺血再灌注损伤|临床诊疗技术|医学健康
想象一场发生在肠道里的“二次伤害”:当缺血的肠道终于等来血流恢复,本该是生机重启,却先迎来一场由活性氧引爆的“氧化风暴”——细胞破裂、炎症扩散,紧接着是肠道屏障垮塌,细菌趁机攻入全身。这就是肠缺血再灌注损伤,一种让医生头疼的双相急症:前24小时要灭火,72小时后要补墙,传统治疗顾此失彼。重庆医科大学的团队却用一颗纳米颗粒,同时搞定了这两个阶段的难题——它能在6小时内掐灭炎症火苗,又能在4天后帮肠道重新建起“防护墙”。
肠缺血再灌注损伤的凶险,在于它是一场分时段的“连环灾”。
缺血期,肠道细胞因缺氧耗尽能量,像断电的工厂一样停摆;再灌注那一刻,氧气汹涌而入,却触发黄嘌呤氧化酶等“坏分子”大量产生活性氧(ROS)——这些分子像失控的自由基,击穿细胞膜、打碎DNA,还会激活NLRP3炎症小体,让巨噬细胞“自爆”(焦亡),释放出大量炎症因子,把局部炎症变成全身风暴,最快24小时就可能引发多器官衰竭。
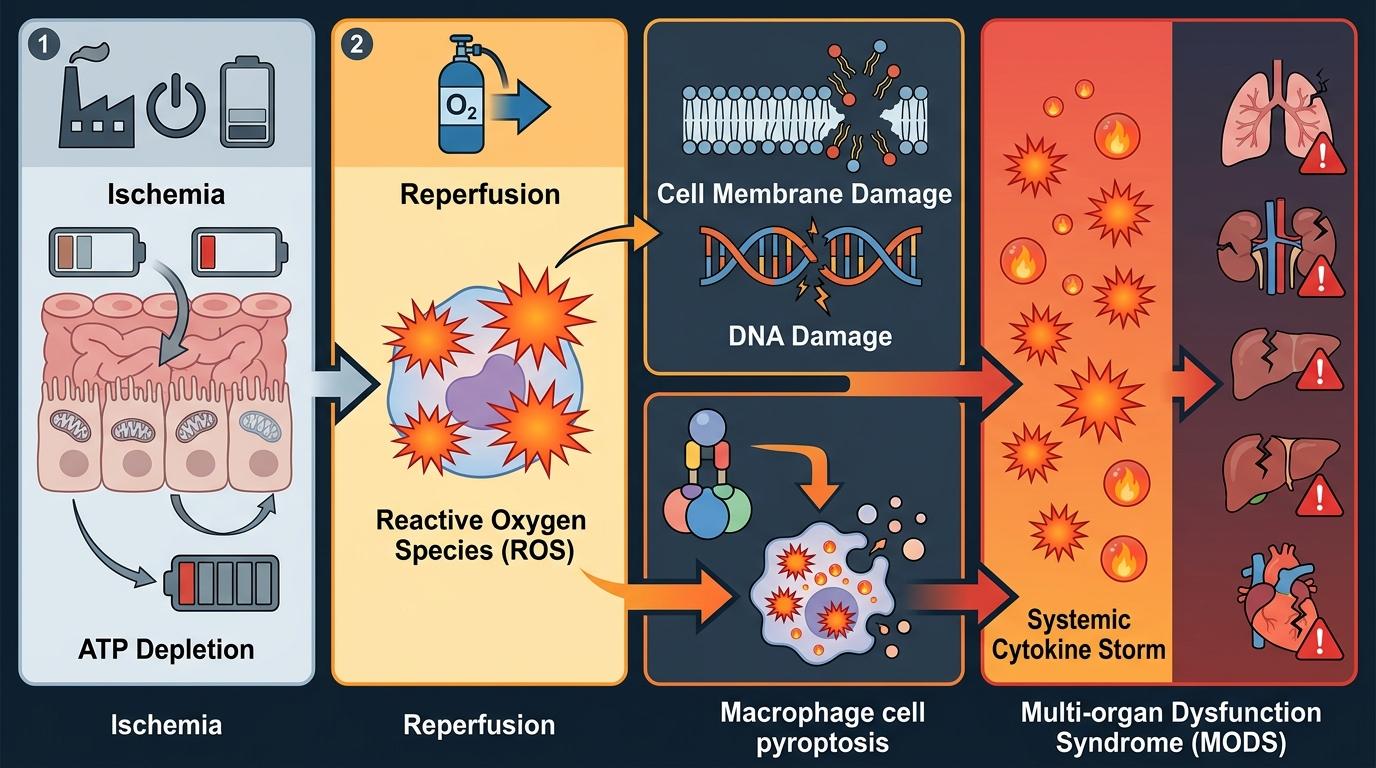
熬过急性期的患者,又会掉进第二个陷阱:肠道黏膜的紧密连接蛋白被破坏,原本像砖墙一样的肠壁出现缝隙,肠道里的细菌和毒素趁机钻进血液,引发继发性脓毒症。这时候,治疗的核心从“抗炎”转向“修复”——要补好肠壁,还要催生新血管给肠道供能。
传统治疗要么只盯着急性期抗氧化,要么只在恢复期促修复,始终跟不上疾病的“节奏切换”。
重庆医科大学团队打造的MPB@TA-Cu-Ma纳米颗粒,是专门为这场“双相战争”设计的“自适应武器”。
它的核心是普鲁士蓝(PB)纳米酶——这是唯一经FDA批准的抗氧化纳米材料,能同时模拟超氧化物歧化酶(SOD)和过氧化氢酶(CAT),像一个高效的“垃圾清运工”,把活性氧快速分解成水和氧气。但团队给它做了三重升级:用单宁酸(TA)刻蚀表面,让它的活性氧清除效率直接提升50.15%;把部分铁离子换成铜离子,不仅强化了抗氧化能力,还赋予了它促血管生成的本事;最后包裹上巨噬细胞消除素MaR1,给它装上了“智能开关”。
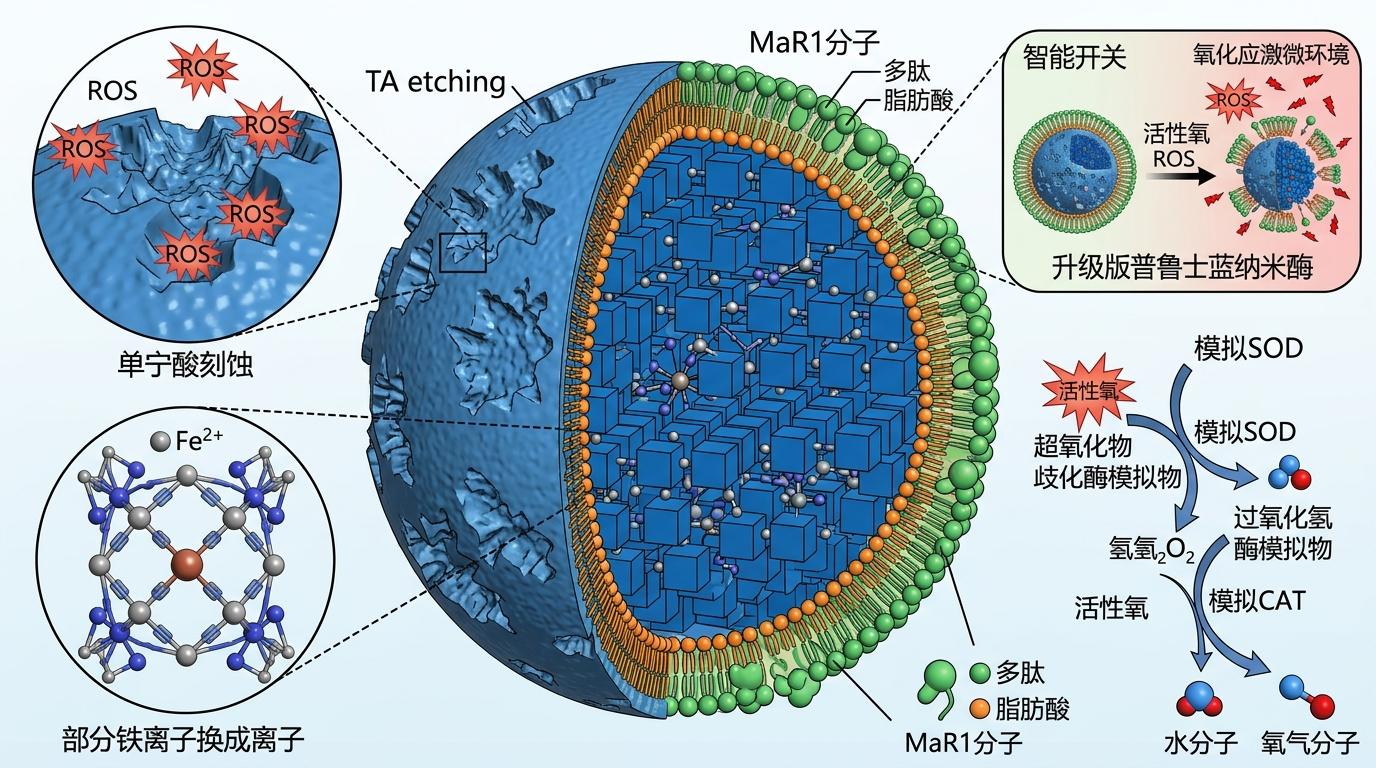
在急性期(损伤后6小时内),纳米颗粒先释放MaR1,死死按住NLRP3/caspase-1通路,不让巨噬细胞“自爆”,同时快速清除活性氧,把炎症因子的水平压下来。到了恢复期(损伤后96小时),它又转而上调α-防御素1和桥粒芯糖蛋白1,像给肠壁“抹水泥”一样修复紧密连接;还能促进血管内皮生长因子(VEGF)表达,催生新的血管给肠道“供血供氧”。
简单说,它会根据肠道的“病情阶段”自动切换功能:先当“消防员”,再当“建筑工”。
这颗纳米颗粒的厉害之处,在于它不是“头痛医头”的单一治疗,而是从根源上阻断了“氧化应激-炎症-屏障损伤”的恶性循环。转录组学分析证实,它同时调控了三条关键通路:抑制焦亡、修复上皮、催生血管,把原本割裂的两个治疗阶段拧成了闭环。
但从实验室到临床,还有几道坎要跨。首先是生物安全性:纳米颗粒在体内的代谢路径、长期蓄积的毒性,还需要更系统的评估;其次是靶向性:如何让它精准聚集在肠道损伤部位,而不是在全身乱跑;最后是规模化生产:要保证每一批纳米颗粒的大小、载药量都完全一致,才能满足临床需求。
更重要的是,动物模型和人类的肠道环境还有差异——小鼠的肠道菌群、免疫反应和人类不同,这颗纳米颗粒在人体内能不能复刻实验室里的效果,还需要更多临床试验验证。
当我们把目光从这颗纳米颗粒拉远,会发现它代表的是一种新的治疗思路:不再是用单一药物对抗复杂疾病,而是让药物“适应”疾病的节奏。
肠缺血再灌注损伤的双相病理,其实是很多复杂疾病的缩影——癌症、自身免疫病、神经退行性疾病,都不是单一靶点的问题,而是多阶段、多通路的紊乱。这颗纳米颗粒的意义,不仅在于解决了一个临床难题,更在于它证明了:我们可以设计出“会思考”的药物,跟着疾病的节奏走,而不是让患者去适应药物的节奏。
好的治疗,是和疾病同频共振。