对抗知识焦虑,从看懂这条开始
App 下载
癌细胞“B计划”遭破解?新药欲破抗癌耐药僵局
癌细胞B计划|抗癌耐药|基因突变|DNA损伤修复|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
癌细胞B计划|抗癌耐药|基因突变|DNA损伤修复|肿瘤学|医学健康
在人体每个细胞的微观世界里,一场永不停歇的战争正在上演。我们的生命蓝图——DNA,每时每刻都面临着来自内外敌人的攻击:紫外线、化学物质、甚至细胞自身复制时的小差错,都可能导致DNA链条断裂。一旦损伤无法修复,基因突变便会累积,为癌症的发生埋下伏笔。
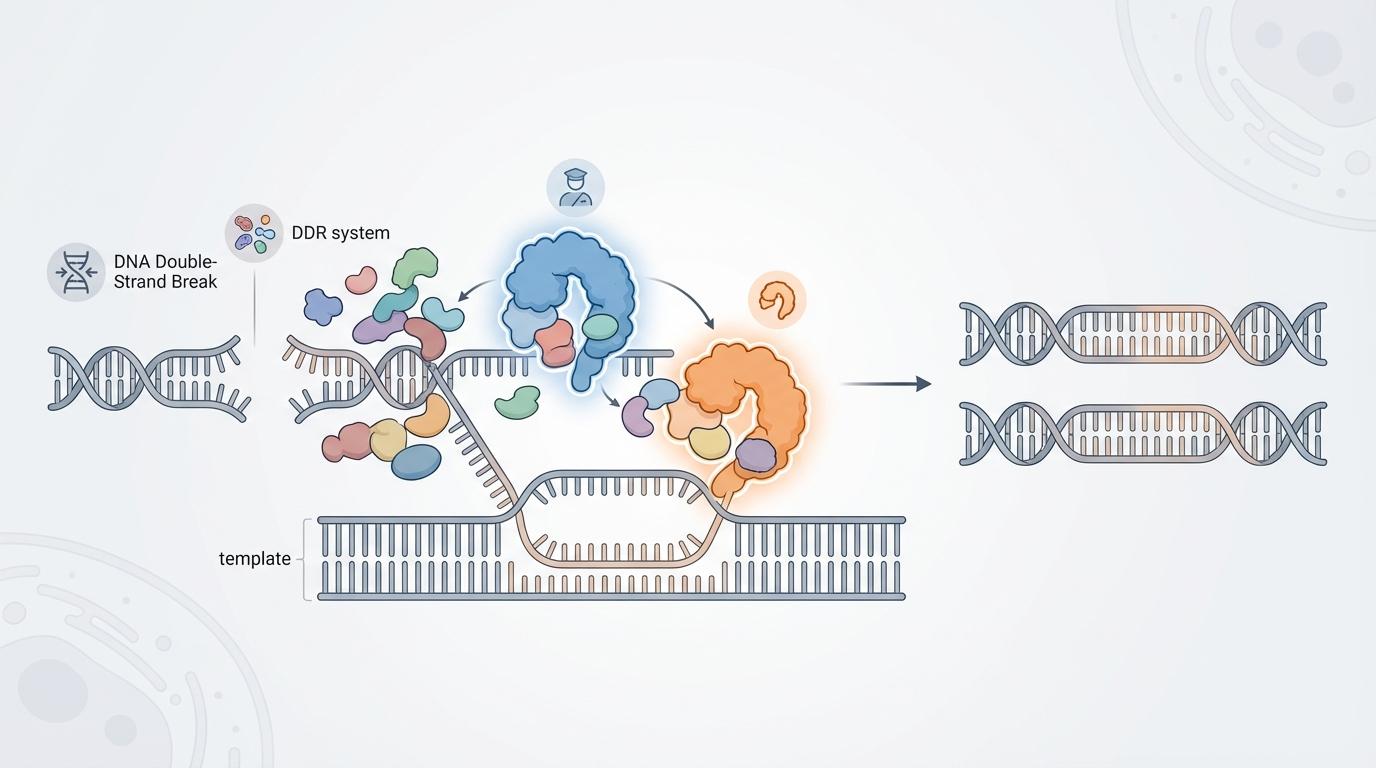
幸运的是,细胞演化出了一套精密的“国防系统”——DNA损伤修复(DDR)通路。其中,对于最凶险的DNA双链断裂,同源重组(Homologous Recombination, HR)修复机制扮演着“王牌部队”的角色。它以未受损的DNA为模板,进行完美无瑕的修复,确保遗传信息的稳定。而BRCA1和BRCA2基因,正是这支王牌部队的关键指挥官。
然而,癌细胞,尤其是部分乳腺癌、卵巢癌、前列腺癌和胰腺癌细胞,却常常自断臂膀。它们的BRCA基因发生突变,导致HR这支精锐部队瘫痪。这个看似致命的缺陷,反而被科学家们敏锐地捕捉到,成为了精准打击癌症的“阿喀琉斯之踵”。
一个世纪前,生物学家在果蝇身上发现了一个奇特现象:两个特定基因单独失活,果蝇安然无恙;但若同时失活,则会导致死亡。这一概念,在近百年后被命名为**“合成致死”(Synthetic Lethality)**,并成为抗癌药物设计的黄金法则。
对于那些BRCA突变、HR修复功能瘫痪的癌细胞,它们被迫依赖另一条较为原始的修复通路来苟延残喘。这条通路的核心是PARP酶。科学家们设想:如果用药物抑制PARP酶,相当于切断了癌细胞最后的救命稻草。正常细胞因为拥有完备的HR修复系统,不受影响;而癌细胞则会因为两条关键修复通路同时失灵,在DNA损伤的重压下走向崩溃。
2014年,基于这一天才构想,首款PARP抑制剂奥拉帕尼(Olaparib)获批上市,精准打击携带BRCA突变的癌细胞,开启了“合成致死”疗法的时代。这无疑是精准医疗史上的一座里程碑,它将癌细胞的“缺陷”变成了“靶点”,实现了前所未有的精准杀伤。
然而,这场攻防战的复杂性,很快超出了最初的预期。
胜利的喜悦并未持续太久。临床数据显示,PARP抑制剂并非万能神药,仅对约60%的患者有效,且许多患者在治疗后不可避免地出现了耐药性。癌细胞,这个进化了亿万年的微观对手,再次展现了其惊人的狡猾与韧性。
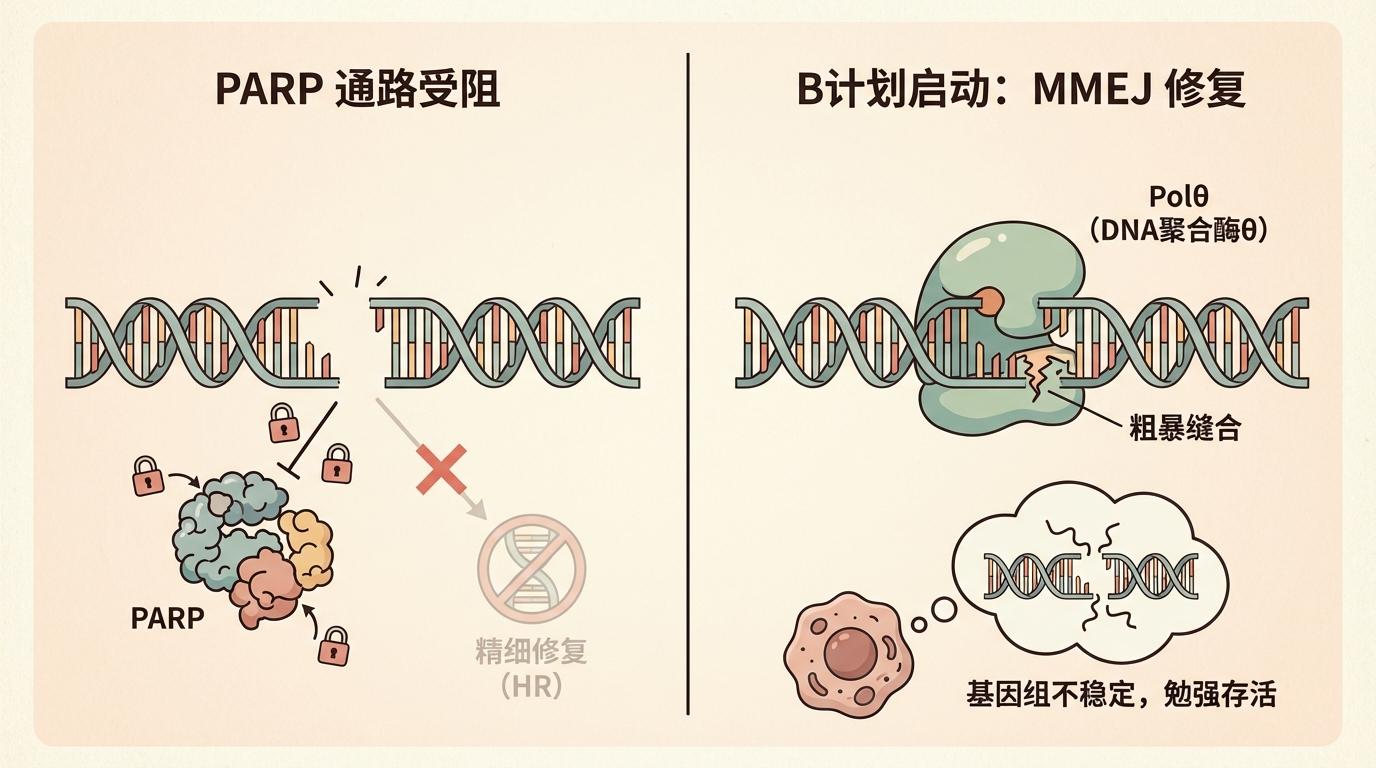
研究人员发现,在PARP通路被封锁后,一部分癌细胞启动了一套被长期忽视的备用修复方案——“B计划”。这个计划的核心,是一种名为**DNA聚合酶θ(Polθ)**的特殊酶。Polθ引导的是一种名为“微同源介导的末端连接”(MMEJ)的修复方式。与HR的精雕细琢不同,MMEJ修复更像是“粗暴缝合”,它修复过程错误频出,容易导致基因组进一步不稳定。但这对于挣扎求生的癌细胞来说,已经足够了。只要能勉强将断裂的DNA连接起来,它们就能活下去。
更棘手的是,Polθ在正常组织中几乎不表达,却在乳腺癌、卵巢癌等多种肿瘤中高表达,其过度活跃与患者的不良预后密切相关。它不仅是癌细胞的备用修复工具,更是其对抗PARP抑制剂、化疗和放疗的“万能挡箭牌”。癌细胞的生存逻辑清晰而残酷:只要Polθ还在,它们就总有翻盘的机会。
敌人的“B计划”已被识破,科学家的对策也随之升级——既然一次打击不够,那就来**“双重打击”**。如果能同时抑制PARP和Polθ,就能彻底摧毁癌细胞所有的DNA修复能力,让其在内外交困中无路可逃。
这一全新的“合成致死”组合策略,迅速点燃了全球新药研发的引擎。近十年来,Polθ已成为抗癌领域最炙手可热的新靶点之一。全球多家制药公司,包括Artios、GSK以及中国的先声药业、圣域生物等,纷纷投入这场攻坚战。
近期,一项研究报告了一款全新的Polθ聚合酶变构抑制剂的诞生,为这场战役带来了新的曙光。根据公布的数据,这款新型小分子抑制剂展现出优异的特性:
如今,以中国先声再明自主研发的SIM0508为代表的多款Polθ抑制剂已进入临床试验阶段,单药或与PARP抑制剂联合使用。2024年底,SIM0508已在中国实现全球首例患者给药,标志着这一“双重打击”策略正从实验室构想,一步步走向临床现实。
从发现BRCA基因的缺陷,到利用“合成致死”开发出PARP抑制剂,再到如今为克服耐药而靶向Polθ,抗癌策略的演进,就像一场精彩的攻防对决。每当癌细胞亮出一张底牌,科学界总能找到克敌制胜的新战术。
Polθ抑制剂的出现,无疑为精准抗癌打开了一扇新的大门。它不仅有望解决PARP抑制剂的耐药难题,更有可能将“合成致死”的理念推广到更广泛的肿瘤类型。未来,我们或许能看到更多基于DNA修复通路缺陷的“组合拳”疗法,例如Polθ抑制剂与化疗、放疗甚至抗体偶联药物(ADC)的联合,为患者提供更多、更有效的治疗选择。
然而,前路依然充满挑战。这些新药在人体内的安全性与有效性仍需大规模临床试验的严格验证。癌细胞的适应性极强,它是否会演化出“C计划”来规避“双重打击”?如何筛选出最适合这类疗法的患者?这些都是摆在科学家和医生面前的开放性问题。
这场围绕生命蓝图的战争远未结束。但每一次对癌细胞生存机制的深刻洞察,都让我们手中的武器库变得更加丰富和强大。Polθ抑制剂的故事告诉我们,在与癌症的漫长博弈中,智慧、坚韧与创新,永远是人类走向最终胜利的最强底牌。