对抗知识焦虑,从看懂这条开始
App 下载
PCOS流产元凶锁定:高雄激素如何让胎盘细胞“生锈”?
浙江大学|细胞铁死亡|胎盘细胞|高雄激素|多囊卵巢综合征|代谢内分泌疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
浙江大学|细胞铁死亡|胎盘细胞|高雄激素|多囊卵巢综合征|代谢内分泌疾病|医学健康
对于全球数百万患有多囊卵巢综合征(PCOS)的女性而言,怀孕之路往往布满荆棘。这是一种育龄期女性最常见的内分泌疾病,其标签不仅是月经不调或代谢紊乱,更深层的痛苦,是反复经历的早期妊娠丢失。这种无声的失去,像一个无法挣脱的循环,长期以来,其背后的生物学机制如同一团迷雾,让患者和医生都深感无力。为何在这些女性体内,新生命的火花总是那么容易熄灭?
就在2025年12月16日,一束光照进了这个长久以来的黑暗角落。浙江大学的张银丽、张松英及Zhu Haiyan教授团队在国际顶尖期刊《Advanced Science》上发表了一项突破性研究,为这个难题提供了全新的答案。他们的研究首次精准地描绘出,PCOS患者体内过高的雄激素(即高雄激素血症),会启动一种名为“铁死亡”(Ferroptosis)的细胞自毁程序,直接攻击胎盘中至关重要的滋养层细胞,最终导致胚胎的“断供”与丢失。
这项发现如同一位侦探,终于在复杂的犯罪现场找到了关键的作案手法,将高雄激素、铁死亡与早期妊娠丢失这三个看似孤立的线索,串成了一条完整的证据链。
要理解这场发生在微观世界里的悲剧,我们需要认识几个关键角色:
滋养层细胞:它们是胎盘的构建者和守护者,是连接母体与胎儿的生命桥梁,负责输送营养、交换气体。它们的健康与否,直接决定了胚胎的命运。
铁死亡(Ferroptosis):这是一种独特的细胞死亡方式,不同于我们熟知的细胞凋亡。你可以把它想象成细胞内部的“生锈”。当细胞内可自由活动的铁离子过多,就会引发一系列失控的氧化反应,破坏细胞膜,最终导致细胞崩解死亡。
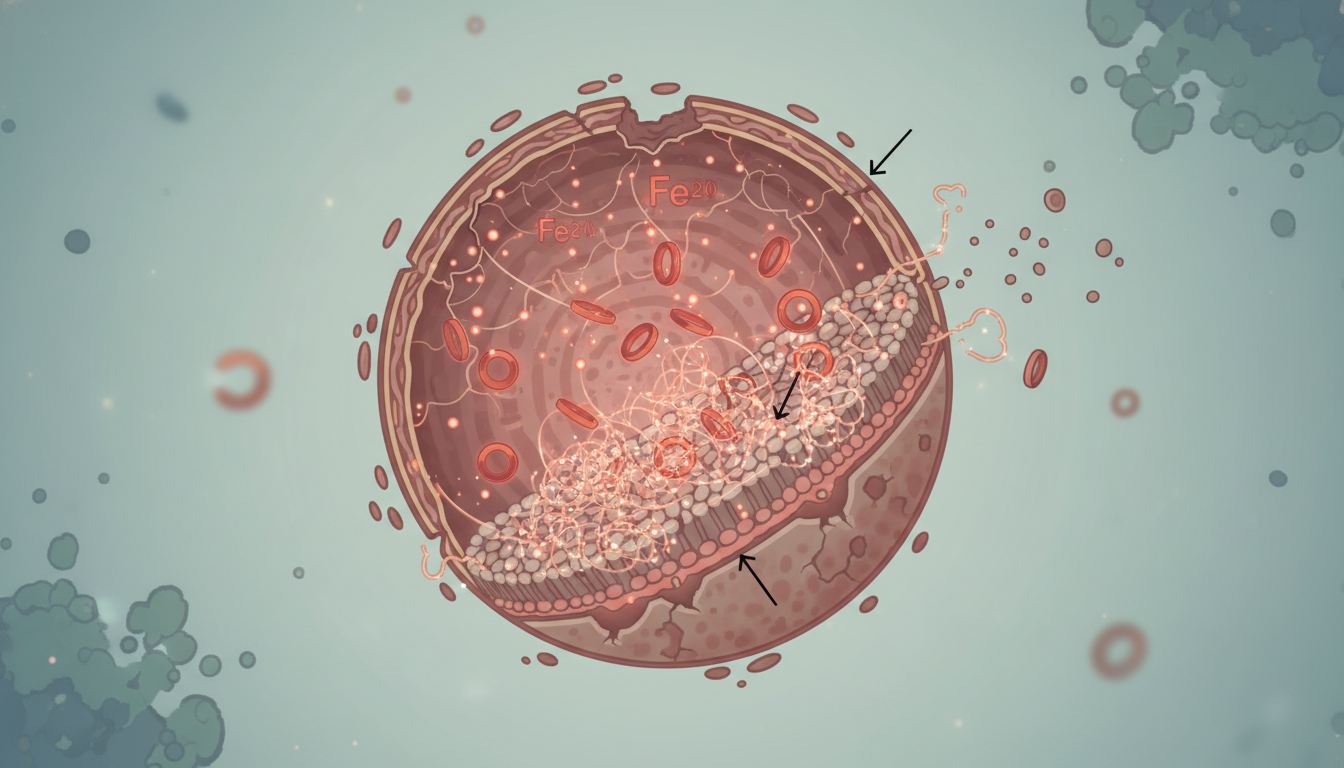
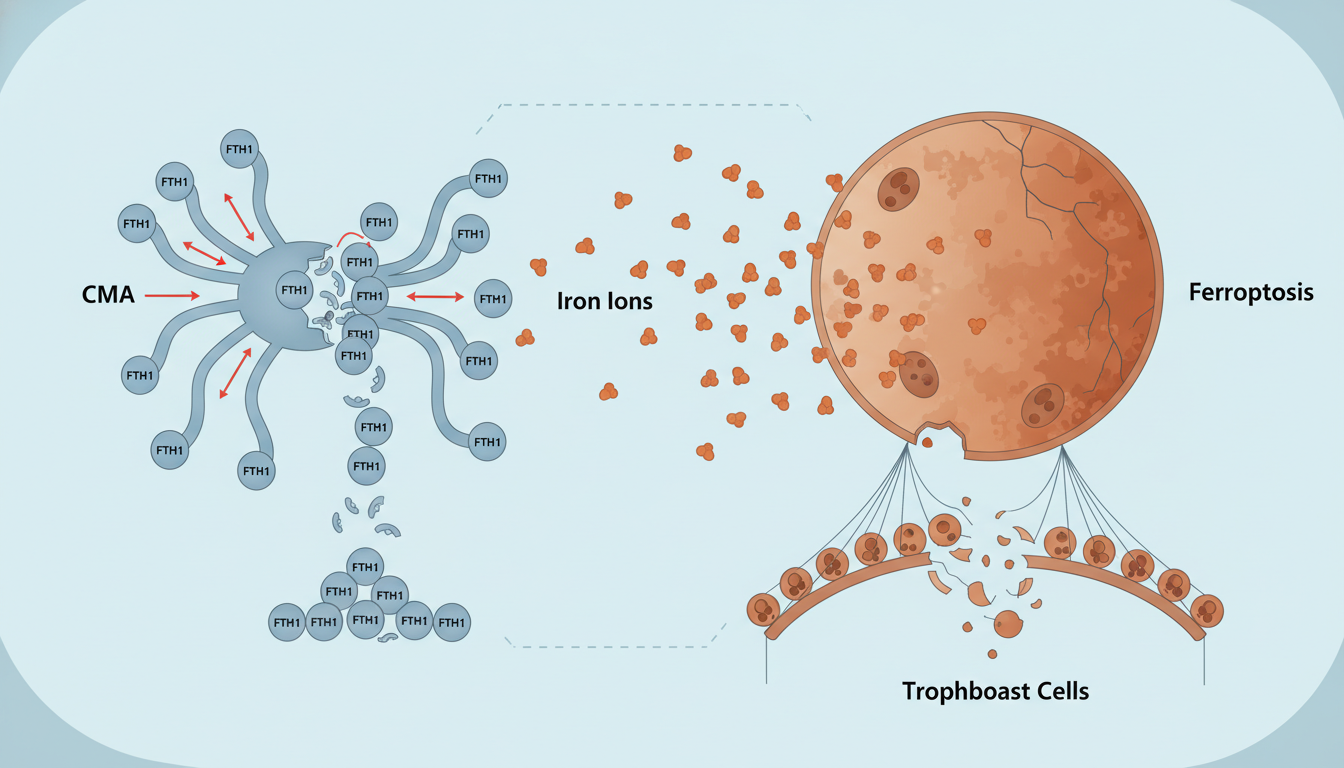
浙江大学团队的研究揭示了一场由高雄激素导演的细胞内“权力的游戏”。正常情况下,雄激素会通过其受体(AR)适度地“命令”细胞生产更多的“铁管家”FTH1。然而,在PCOS患者体内,过量的雄激素变得像一个反复无常的暴君。它一方面下令增产FTH1,另一方面却又激活了一个更强大的破坏机制——伴侣蛋白介导的自噬(CMA)。
CMA就像一个被过度激活的“内部纪律部门”,它会疯狂地降解FTH1蛋白。这场“生产”与“破坏”的竞赛,最终以后者的压倒性胜利告终。当“铁管家”FTH1被大量清除后,细胞内的铁离子失去束缚,四处流窜,最终引发了滋养层细胞的“生锈”——铁死亡。生命之桥,由此开始崩塌。
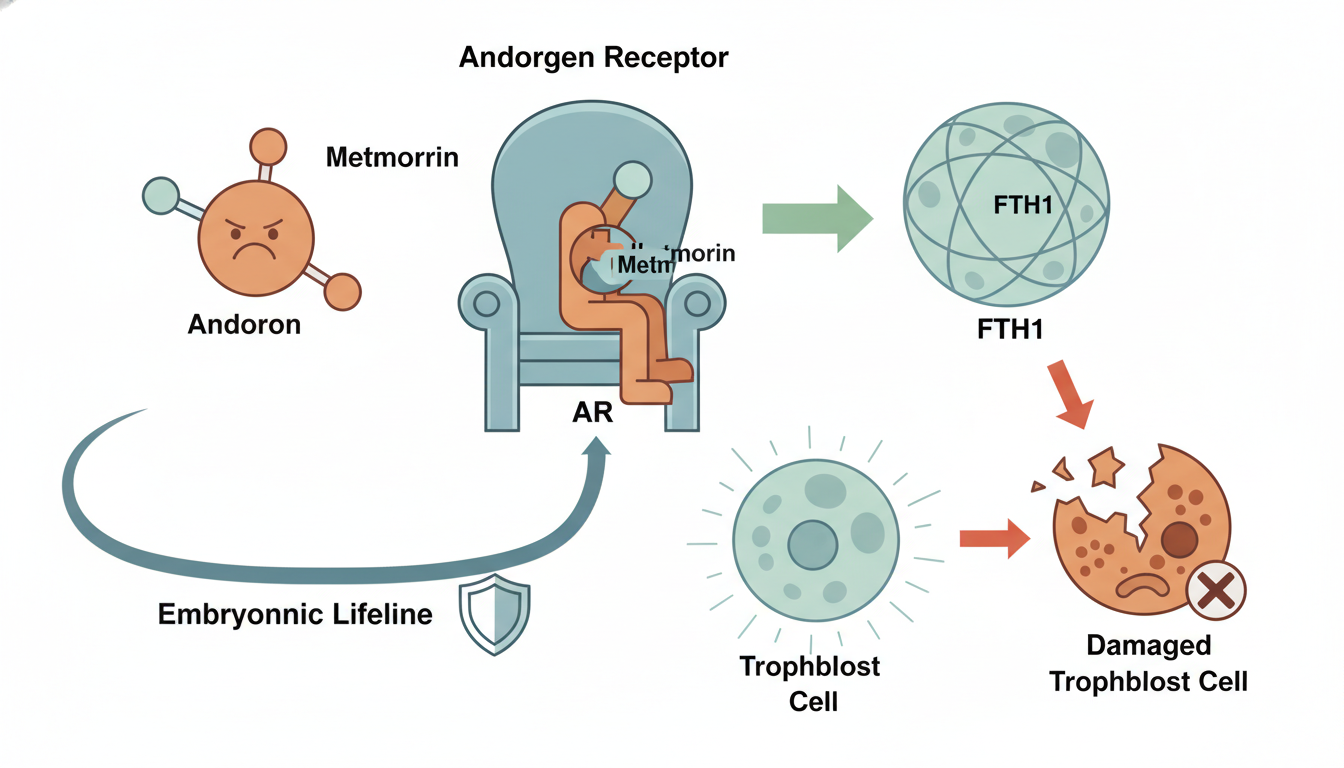
长期以来,二甲双胍作为治疗2型糖尿病的“神药”,也常被用于改善PCOS患者的胰岛素抵抗。然而,它究竟如何帮助降低妊娠丢失风险,具体机制一直不甚明了。此次研究,意外地揭示了它的一个全新身份:雄激素受体的竞争者。
研究发现,二甲双胍分子能够与雄激素“争抢”同一个“王座”——雄激素受体(AR)。当二甲双胍成功占据受体后,雄激素就无法发出那些激活CMA、破坏FTH1的“指令”。如此一来,“铁管家”FTH1得以稳定存在,滋养层细胞免于“生锈”的命运,胚胎的生命线也因此得到了保护。
在PCOS小鼠模型中,二甲双胍的干预显著降低了早期胚胎的吸收率,这为它的临床应用提供了强有力的科学依据。
然而,科学的叙事从不是非黑即白。尽管这项研究为二甲双胍描绘了英雄般的角色,但我们必须保持审慎。近年来,其他研究(包括浙江大学王福俤/闵军霞教授团队的另一项重要发现)也指出,二甲双胍在某些情况下,例如在急性肾损伤模型中,反而会通过与铁的相互作用,诱导肾脏细胞发生铁死亡,加剧组织损伤。
这揭示了二甲双胍作为一把“双刃剑”的复杂性。它对铁死亡的影响是高度情境依赖的。在高雄激素的滋养层细胞中,它扮演保护者;但在其他组织或病理状态下,它可能成为破坏者。这警示我们,任何药物的应用都需精准评估,绝不能盲目推广。此外,二甲双胍能够自由穿过胎盘,其对胎儿的长期影响,仍是科学界持续关注和研究的开放问题。
浙江大学团队的这项里程碑式研究,不仅为解释PCOS相关的妊娠丢失提供了核心机制,更为未来的临床干预开辟了新大陆。它告诉我们,战斗的方向或许应该从笼统的“保胎”转向更精准的“防锈”。
未来的图景令人期待:
精准诊断:未来或许可以通过检测孕早期女性滋养层细胞的铁死亡水平,来预测妊娠丢失的风险。
靶向治疗:除了二甲双胍,科学家们可能会开发出更特异性靶向CMA-FTH1通路的药物,以更安全、更高效的方式保护胎盘。
个体化方案:结合PCOS的不同亚型(如高雄激素型、肥胖型等),为患者制定个体化的治疗方案,决定是否以及何时使用二甲双胍等药物。
从一个令人心碎的临床难题,到一个清晰的细胞死亡机制,再到一个老药新用的科学突破,这条探索之路充满了挑战与希望。它不仅是对生命奥秘的又一次深刻洞察,更是对无数家庭深切期盼的回应。微观世界里的“生锈”之谜被解开,预示着在宏观的生命孕育之路上,我们将能构筑起更坚固的防线。