
5 天前

5 天前
想象一下:皮肤像被慢慢浇筑的水泥,从指尖开始变硬、紧绷,逐渐蔓延到手臂、躯干,连呼吸时肺部的扩张都变得艰难——这不是科幻电影的设定,是硬皮病患者正在经历的日常。这种自身免疫性疾病会让身体的组织疯狂纤维化,传统治疗要么压不住病情,要么带来严重的副作用。2026年3月,吉林大学李萍、姜金兰团队的研究,给这场和纤维化的拉锯战带来了新转机:他们把脐带间充质干细胞放进4℃环境里‘冷藏’72小时,造出了能精准瞄准病灶、还能从两条通路同时出击的RT-MSCs。为什么普通的冷藏操作,能让干细胞变身抗纤维化的‘特种兵’?
你可以把线粒体看成细胞里的‘发电站’,给细胞供能的同时,一旦受损也会释放‘垃圾信号’,触发成纤维细胞疯狂分泌胶原蛋白——这正是硬皮病纤维化的关键。而线粒体自噬,就是细胞给受损线粒体做‘垃圾分类’的过程:把坏的线粒体打包送到溶酶体里降解,不让它们继续搞破坏。
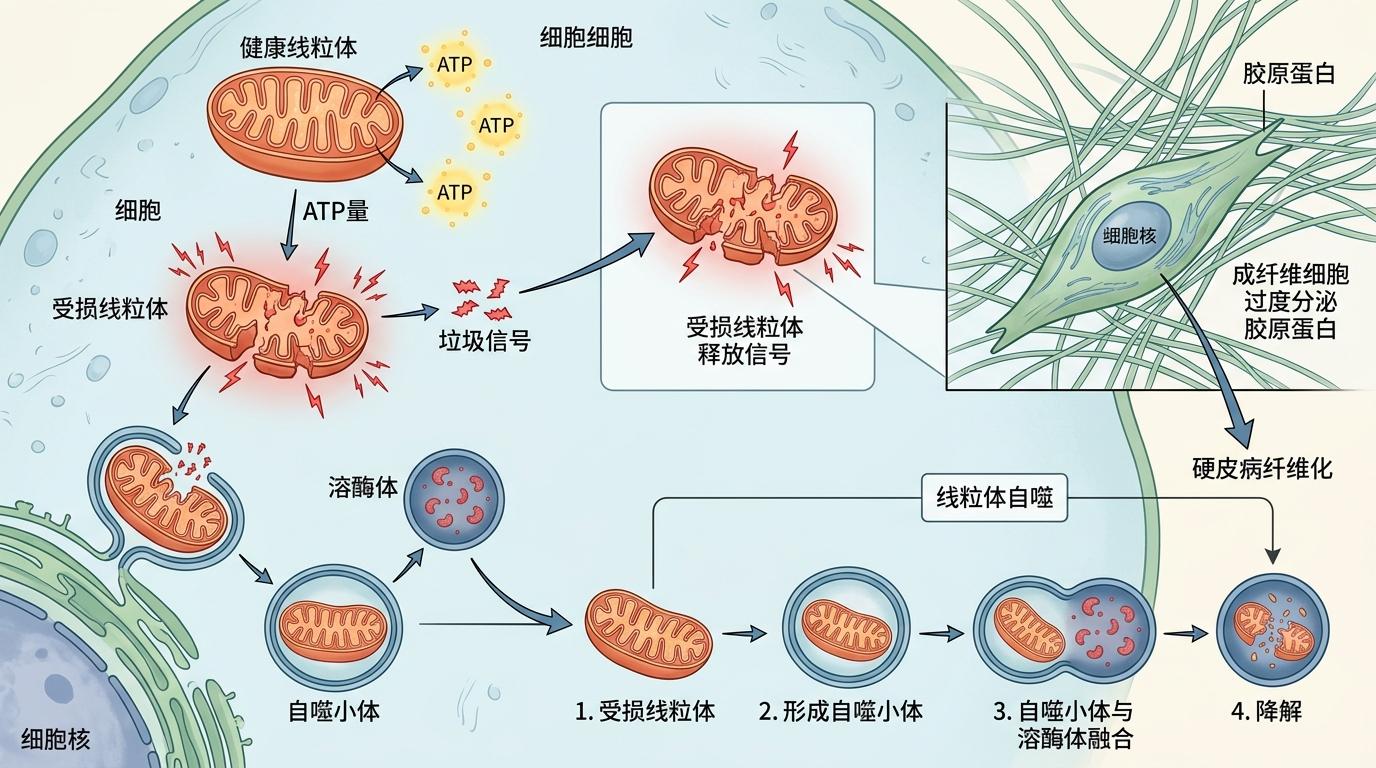
硬皮病模型里,成纤维细胞的线粒体自噬会陷入‘过度激活’的混乱状态:好的坏的线粒体都被胡乱清理,反而让细胞陷入能量危机,进一步刺激纤维化。RT-MSCs的作用,就是把这个混乱的开关拨回正轨。实验显示,它能精准调节PINK1/Parkin这两条线粒体自噬的核心通路,降低过度活跃的自噬水平,同时修复受损线粒体的形态。简单说,就是让细胞只处理真正的‘垃圾’,别把还能干活的‘发电站’也一起扔了。
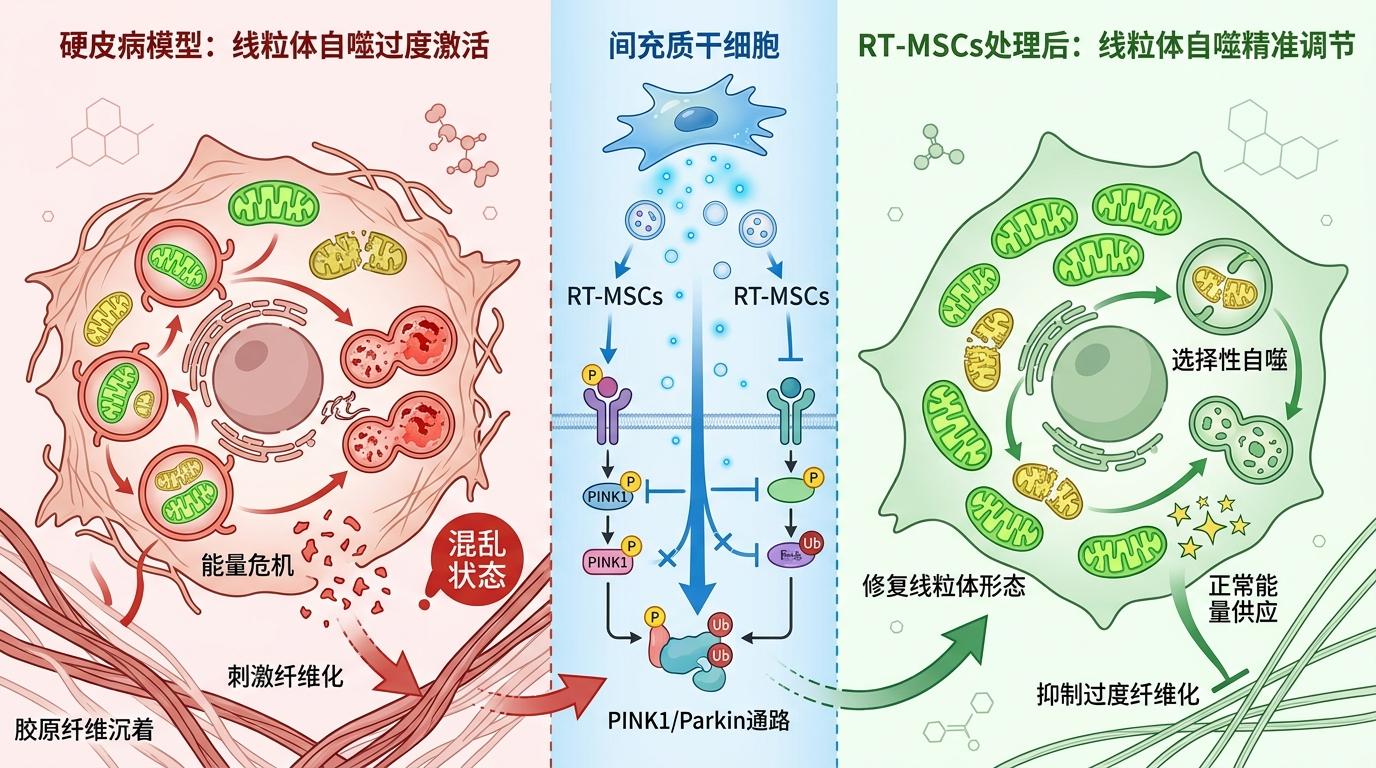
更关键的是,这些冷藏过的干细胞像装了导航:注射后30分钟内就能聚集到皮肤、肺部的纤维化病灶,还能在那里‘驻扎’7天——比普通干细胞的靶向能力强得多,相当于把‘治疗弹药’精准投放到了战场最前线。
你可能想不到,硬皮病的纤维化,和肠道里的菌群也有着千丝万缕的联系。硬皮病患者的肠道菌群会严重失调:抗炎的益生菌减少,促炎的致病菌增多,这些紊乱的菌群会通过代谢产物进入血液循环,进一步加剧全身的免疫异常和纤维化。
RT-MSCs就像给肠道菌群‘重新洗牌’的操盘手。研究团队通过16S rRNA测序发现,它能让硬皮病小鼠肠道里失衡的菌群结构逐渐恢复正常:减少条件致病菌的数量,增加能产生短链脂肪酸的益生菌。这些益生菌的代谢产物不仅能修复受损的肠道屏障,还能调节全身的免疫反应,减少促炎细胞因子的释放。
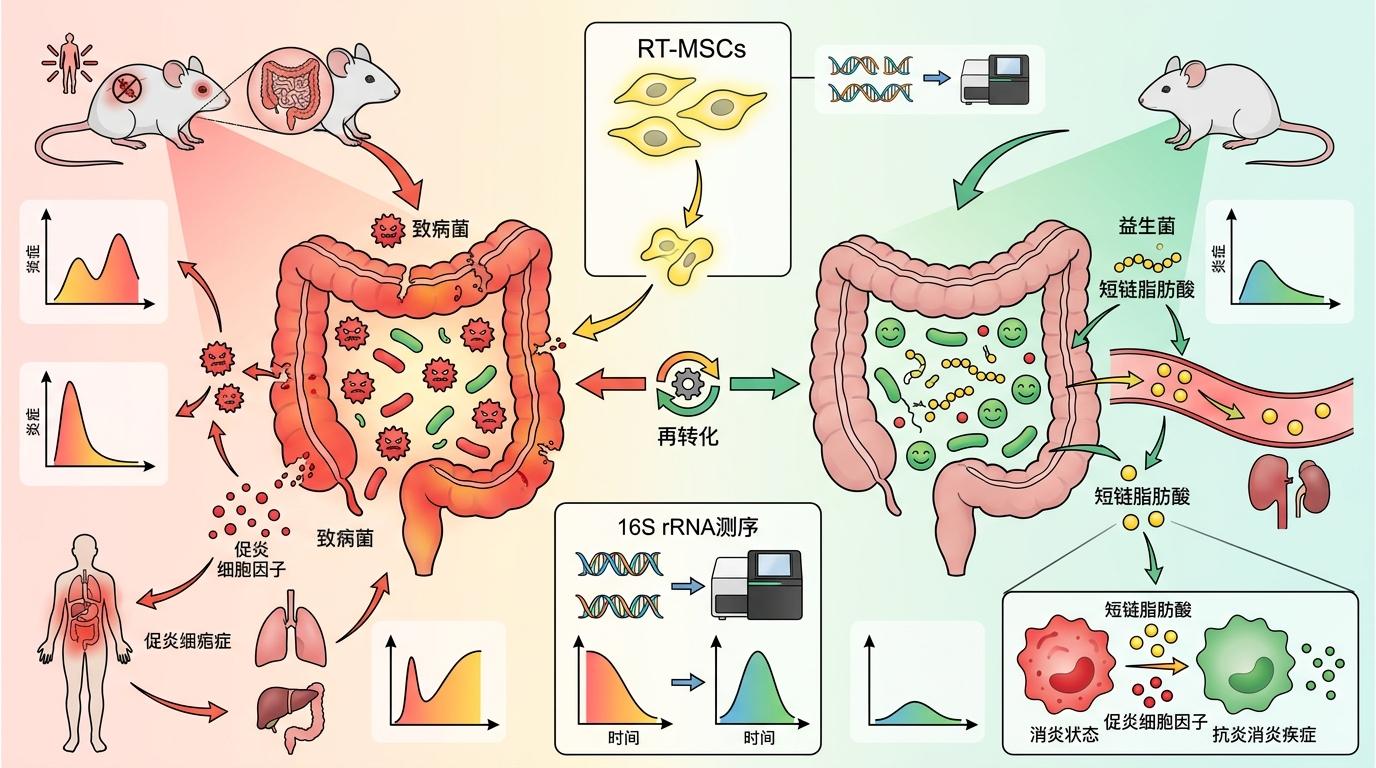
更巧妙的是,RT-MSCs还能瞄准纤维化的‘原料库’——精氨酸代谢。精氨酸是合成胶原蛋白的关键原料,硬皮病患者体内的精氨酸代谢会偏向胶原蛋白合成的方向。而RT-MSCs能把这个代谢通路‘掰’向产生一氧化氮的方向,既减少了纤维化的原料,又能扩张血管,改善硬皮病患者常见的雷诺现象。
不过要提醒的是,目前这些结果都来自动物实验,离真正应用到患者身上,还需要更多临床试验验证菌群调节的长期效果。
和所有新兴疗法一样,RT-MSCs也有它的局限。比如,目前还不清楚这种冷藏处理的干细胞,在不同年龄、不同病情阶段的患者身上效果是否一致;肠道菌群的调节作用,会不会因为患者本身的菌群基础不同而出现巨大差异。而且干细胞治疗的成本、标准化制备流程,都是横在临床转化面前的现实问题。
但不可否认的是,RT-MSCs给硬皮病治疗带来了全新的思路:它不再是单纯用药物压制免疫反应,而是从细胞层面修复线粒体功能,从肠道层面调节免疫稳态——这种‘多靶点调控’的思路,比传统治疗更接近疾病的根源。更重要的是,它的安全性已经在动物实验中得到验证:连续注射后,小鼠的心脏、肝脏、肾脏等主要器官都没有出现毒性损伤,也没有肿瘤形成的迹象。
对于被硬皮病困住的患者来说,每一次治疗突破,都是在为他们撬开一道缝隙,让阳光照进来。RT-MSCs的意义,不仅在于它能减缓纤维化的速度,更在于它让我们看到:治疗自身免疫病,或许可以不用‘对抗’,而是用更温和的方式,帮身体重新找回平衡。
修复比对抗更接近治愈的本质。未来的某天,当冷藏干细胞走进临床,那些被硬化皮肤束缚的双手,或许能重新握住温度,那些被纤维化困住的呼吸,或许能重新变得顺畅——这正是科学最动人的地方:用一点点改变,给人带来重新生活的希望。
点击充电,成为大圆镜下一个视频选题!