
1 个月前

1 个月前
你可能没听过慢性化脓性关节炎,但一定懂“治不好的感染”有多磨人:关节红肿热痛反复,抗生素用了一轮又一轮,病菌却像打不死的小强——它们藏进了本该消灭它们的巨噬细胞里,把免疫细胞变成自己的“庇护所”。
浙江大学的研究团队最近揪出了这场“内鬼叛变”的核心密码:病菌悄悄改写了巨噬细胞的脂质代谢,让本该负责杀菌的溶酶体彻底失灵。更关键的是,他们造出了一种能精准修复这个漏洞的纳米武器,把被策反的巨噬细胞重新拉回战场。
为什么病菌能在免疫细胞里安家?这个纳米武器又靠什么逆转战局?
我们可以把巨噬细胞想象成身体里的“巡逻清洁工”:平时到处转悠,碰到病菌就一口吞下,送到细胞里的“消毒车间”——溶酶体里分解。溶酶体就像个装满强酸和消化酶的垃圾桶,只要病菌被扔进去,基本难逃一死。
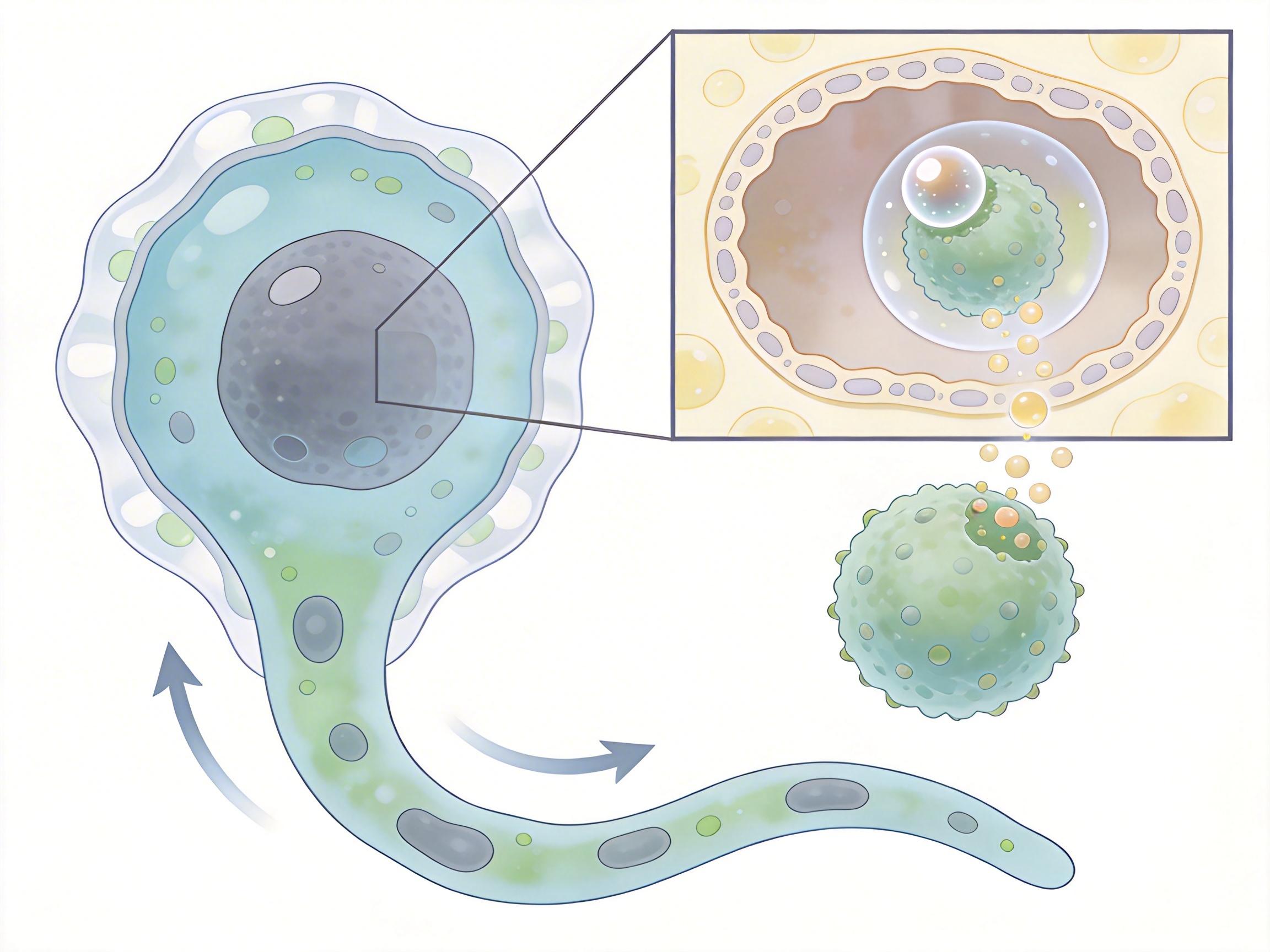
但金黄色葡萄球菌这类狡猾的病菌,早就摸透了巨噬细胞的软肋。它们被吞进细胞后,不会乖乖等着被消化,反而会触发巨噬细胞的“代谢重编程”:原本靠糖酵解提供杀菌能量的巨噬细胞,突然转向脂质代谢,一种叫BMP的磷脂开始在溶酶体里越积越多。
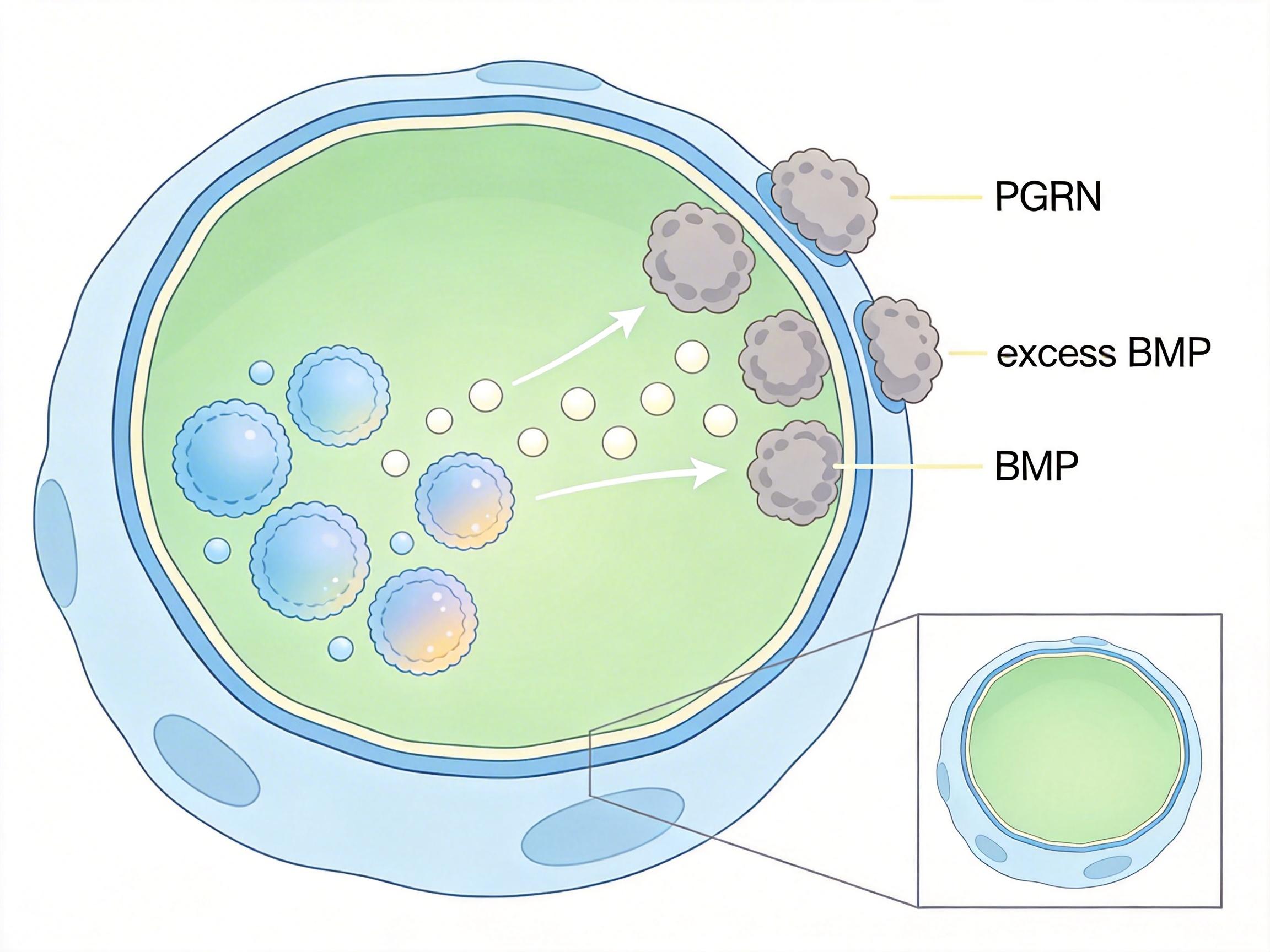
BMP本来是维持溶酶体膜稳定的“黏合剂”,但过量的BMP会像水垢一样糊住溶酶体,再加上一种叫PGRN的溶酶体“维修工”被病菌消耗殆尽,溶酶体的膜开始破裂,消化酶漏得满地都是,杀菌能力直接归零。
更糟的还在后面。失去杀菌能力的巨噬细胞,会从“战斗型”转变成“安抚型”:不再分泌炎症因子召唤援兵,反而释放信号抑制免疫反应——相当于直接给病菌开了“免死金牌”,让它们在细胞里安心繁殖,形成永远清不干净的感染源。
既然找到了问题的核心——PGRN缺失导致溶酶体失灵,那直接给巨噬细胞补PGRN不就行了?没那么简单。PGRN是一种蛋白质,直接注射的话,不仅很难穿透细胞膜进入巨噬细胞,还会在血液里很快被分解,根本到不了病灶。
研究团队的解法是给PGRN做了个“纳米快递盒”——NPs@PGRN双靶向纳米递送系统。这个纳米颗粒只有几十纳米大,表面带着能精准识别巨噬细胞的“导航信号”,能穿过关节的生理屏障,直直钻进被病菌占领的巨噬细胞里。
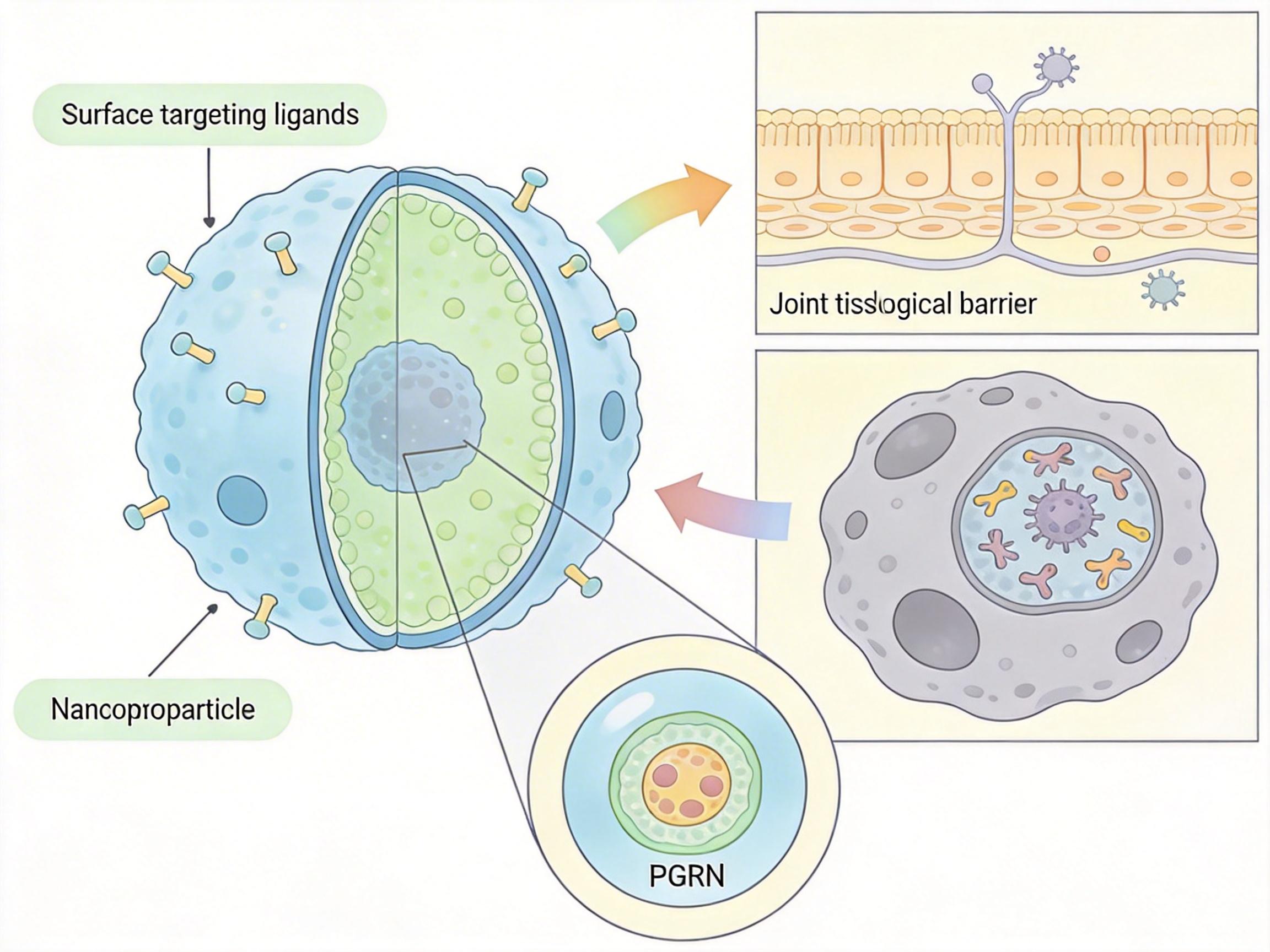
一旦进入细胞,纳米颗粒就会在溶酶体的酸性环境里自动解体,释放出包裹的PGRN。补回来的PGRN会立刻和过量的BMP结合,把糊在溶酶体膜上的“水垢”清理干净,同时修复破裂的膜结构,让溶酶体重新变回那个能杀菌的“消毒车间”。
实验数据给出了最直接的结果:在慢性化脓性关节炎的小鼠模型里,注射NPs@PGRN后,巨噬细胞的溶酶体杀菌能力恢复了90%以上,关节里的细菌负荷下降了80%,原本转向“安抚型”的巨噬细胞,又重新变回了能主动追杀病菌的“战斗型”。
这次研究最关键的突破,其实不是造出了纳米武器,而是第一次把“脂质代谢”和“免疫功能”的关联,清晰地摆在了慢性感染的治疗面前。
过去我们总以为,免疫细胞的功能只和基因、细胞因子有关,却没注意到代谢是免疫细胞的“能量开关”。就像一辆坦克,要是给它加的不是汽油而是水,再厉害的炮也开不起来。病菌就是通过篡改巨噬细胞的“加油方式”,让免疫坦克彻底趴窝。
更值得深思的是,这种“代谢策反”不是慢性化脓性关节炎独有的——肺结核、慢性乙肝这类“治不好的感染”,背后都有病菌改写宿主细胞代谢的影子。这次找到的PGRN-BMP-溶酶体轴,相当于给这类疾病的治疗打开了一扇新的门:与其盯着病菌本身用抗生素,不如修复被破坏的免疫细胞代谢,让身体自己的卫士重新发挥作用。
当然,目前这还只是动物实验的结果,要用到临床上还需要更多的验证。但至少我们终于搞懂了:那些躲在细胞里的病菌,不是杀不死,而是我们之前没找到正确的开关。
当我们和病菌的战争从“用抗生素追杀”转向“修复自身免疫代谢”,这场持续了几十年的拉锯战,终于有了换赛道的可能。
过去我们总把病菌当成外来的敌人,却忘了很多时候,战争的胜负其实取决于我们自身的细胞站在哪一边。就像这次研究揭示的:真正的战场,从来都不是病菌和抗生素的对抗,而是病菌和我们细胞代谢的博弈。
免疫的本质,是代谢的平衡。 这句话或许会成为未来感染治疗的核心——与其想着怎么杀光病菌,不如先把自己的细胞调理好,让它们重新拿起武器,守护我们的身体。
点击充电,成为大圆镜下一个视频选题!