对抗知识焦虑,从看懂这条开始
App 下载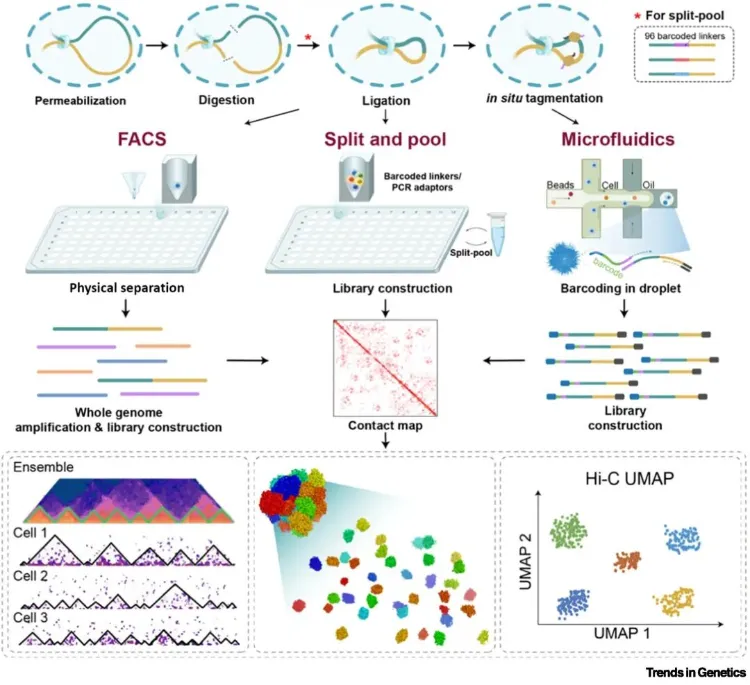
折叠的代码:解密DNA的三维交响乐,重写生命与医学的未来
细胞核结构|分子折纸|DNA折叠|三维基因组|基因组学|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
细胞核结构|分子折纸|DNA折叠|三维基因组|基因组学|生命科学
如果将人体内一个细胞核中的DNA完全展开,其长度接近两米。然而,它却被巧妙地折叠并压缩在一个直径仅有10微米的细胞核内。这相当于将一座珠穆朗玛峰大小的精细模型,装入一枚小小的乒乓球。这并非一次随意的揉捏,而是一场遵循着精确规则的“分子折纸”艺术。这种三维空间结构,正是生命复杂性的核心秘密。长期以来,我们习惯于将基因组视为一本线性的“生命之书”,逐字阅读其A、T、C、G组成的序列。但我们日益发现,这本书的真正魔力在于它是如何被折叠的——遥远的章节可以紧密相贴,创造出全新的意义。解开这个折叠之谜,正是三维基因组学这场革命的核心。
这场革命的里程碑时刻,由浙江大学生命科学研究院的阮一骏研究员与柴皓曦副研究员在《遗传学趋势》(Trends in Genetics)期刊上的一篇综述文章得以系统性地梳理。这篇文章回顾了三维基因组学技术走过的15年历程,将其比作一个进入“及笄之年”的少年,标志着该领域从初创的探索期迈向了深度洞察与应用的成熟期。故事的序幕在2009年拉开,Hi-C和ChIA-PET两项革命性技术的诞生,如同为科学家们装上了能透视细胞核的“3D眼镜”,首次让我们得以在全基因组尺度上绘制染色质相互作用的宏伟蓝图。
Hi-C技术像一张无差别的广角网,捕获细胞核内所有DNA片段在空间上的邻近关系;而ChIA-PET技术则更为精准,它通过引入抗体,专门“钓”取由特定蛋白质(如转录因子)介导的染色质互作。这两大技术的问世,共同奠定了三维基因组学的基础,揭示了基因组在细胞核内并非一团乱麻,而是层次分明的精巧结构:
最初的3D图谱是静态的,如同城市规划图,展示了建筑物的布局。但生命是动态的,科学家们渴望看到这座城市24小时的运转实况。过去十五年,技术竞赛的目标就是不断提升分辨率与维度,将静态地图升级为高清动态电影。
分辨率的极限冲刺:从最初只能看清“街区”轮廓,到后来通过Micro-C技术,分辨率被推向了核小体级别。而牛津大学李杭蓬和James O.J. Davies团队开发的MCCu技术,更是实现了单碱基对的超高精度,让我们能看清增强子和启动子内部,不同转录因子结合位点之间纳米级别的精细拓扑结构。这就像从卫星地图,直接切换到了可以看清每块砖头纹理的街景模式。
从群体平均到个体写真:早期的技术只能提供成千上万个细胞的“平均”图像,掩盖了细胞间的个性差异。单细胞Hi-C等技术的出现,让我们能为每个细胞绘制独一无二的3D基因组肖像,这对于理解肿瘤异质性等复杂问题至关重要。
从“测序”到“直播”:最激动人心的突破,莫过于将这一切“可视化”。清华大学王海峰、颉伟团队与中科院方显杨团队合作开发的CRISPR PRO-LiveFISH技术,为细胞装上了高清“显微镜”。他们巧妙地利用CRISPR技术给特定的DNA片段贴上荧光标签,从而在活细胞中实时追踪染色质的动态舞蹈。通过这项技术,他们亲眼看到,当抑制一种名为BRD4的关键蛋白时,一个超级增强子与其靶基因之间的空间连接是如何被“剪断”的,生动地展示了三维结构与基因功能的直接因果联系。
拥有了这些强大的工具,科学家们开始解答生命科学中最核心的问题:基因组的三维结构是如何驱动我们从一个受精卵发育成复杂个体,又是如何在疾病中失序的?
发育与分化:干细胞如何决定自己的命运?答案很大程度上写在三维基因组的重塑中。**黏连蛋白(Cohesin)**复合物就像一个动态的“建筑师”,通过挤压DNA形成染色质环,精确地连接增强子和启动子。在胚胎干细胞中,它维持着多能性基因的开放;在神经干细胞分化时,它又会重组结构,激活神经发育相关基因。三维结构的动态变化,正是细胞身份建立与功能执行的底层逻辑。
疾病的根源:许多疾病的发生,源于基因调控的“脱轨”。癌症中,染色体的异常折叠可能将一个沉睡的癌基因“传送”到一个高度活跃的区域,导致其疯狂表达。西湖大学董晨团队的研究发现,在肿瘤微环境中,T细胞之所以会“耗竭”而失去攻击能力,其背后就有转录因子IRF8重塑染色质三维结构,改变了免疫相关基因表达网络的深刻机制。在神经退行性疾病如肌萎缩侧索硬化症(ALS)中,TDP-43蛋白的异常聚集也与三维基因组紊乱导致的基因剪接错误密切相关。这些发现将疾病的认知从单一基因突变,提升到了“基因组结构病”的全新维度,为开发“染色质疗法”提供了可能。
农业的未来:作物的产量、抗性等复杂性状,往往由多个基因协同调控。中国科学院植物研究所张梅团队对玉米的研究发现,不同自交系之间的结构变异,极大地塑造了各自特有的三维调控网络。杂交后代之所以表现出“杂种优势”,部分原因在于其三维基因组发生了广泛重构,激活了关键基因的表达。这为我们通过精准设计基因组三维结构,来培育高产、优质的“超级作物”提供了全新的育种思路。
随着单细胞、多组学和空间技术的融合,我们正迎来一个数据爆炸的时代。如何从海量、复杂的数据中提取规律?人工智能(AI)成为了不可或缺的导航员。深度学习模型,如ChromFound,能够整合数百万个单细胞的数据,不仅能预测基因表达,还能推断增强子与基因的调控关系,揭示隐藏在数据背后的生物学原理。
未来的三维基因组学,将是一幅更加宏大和精细的画卷:
四维基因组学:结合活细胞成像,我们将时间维度(第四维)融入三维空间,观察生命活动中基因组的实时动态变化,理解基因调控的时序性。
空间多组学:技术将走出单个细胞核,进入组织和器官的真实环境。利用Patho-DBiT等空间组学技术,我们可以在一张组织切片上,同时看到每个细胞的三维基因组结构、基因表达谱和蛋白水平,理解细胞如何在其“社区”环境中相互影响。
从观察到操控:科学家们不再满足于被动观察。南京大学韩瑞琦课题组开发的TACL系统,已经可以像“遥控器”一样,在细胞的特定位置精准地“开启”或“关闭”黏连蛋白的活性,从而主动创造或破坏染色质环,直接验证其功能。这标志着我们正从“解读基因组”迈向“编辑基因组结构”的时代。
从一条线性序列到一个动态、折叠的三维宇宙,我们对基因组的认知在过去15年里发生了天翻地覆的变化。三维基因组学不仅为我们解释了基因调控的深层机制,更为我们理解发育、衰老、疾病乃至进化提供了全新的框架。它告诉我们,生命不仅在于“有什么”基因,更在于这些基因如何被“组织”起来。随着AI、单细胞和空间技术的不断融合,我们正以前所未有的深度和广度,绘制着生命的动态蓝图。未来,我们或许不仅能阅读和编辑生命的文字,更能成为其空间结构的建筑师,通过重塑折叠的代码,修复疾病的根源,设计更美好的生命形态。