对抗知识焦虑,从看懂这条开始
App 下载
心碎时心尖先瘫,分子快递员揭开区域差异
急性应激反应|心尖部功能障碍|细胞外囊泡|心碎综合征|心脑血管疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
急性应激反应|心尖部功能障碍|细胞外囊泡|心碎综合征|心脑血管疾病|医学健康
58岁的张阿姨在女儿车祸离世后突发胸痛,被送进急诊时心电图异常、心肌酶升高,所有人都以为是急性心梗——直到冠脉造影显示她的血管完全通畅。医生告诉她,这是「心碎综合征」:左心室心尖部像被扎破的气球一样膨出,彻底失去收缩能力,可紧挨着的心底部还在有力跳动。
这种病在绝经后女性中占疑似心梗病例的6%以上,急性期死亡率和心梗相当,却一直没人能解释:同一个心脏,同一场应激打击,为什么心尖「瘫了」,心底却安然无恙?瑞典科学家最新的研究,终于从心脏里的「分子快递员」身上找到了答案。
要解开这个区域差异的谜题,得先认识细胞外囊泡(EVs)——一种细胞分泌的纳米级膜囊泡,就像心脏里的「分子快递员」,带着蛋白质、RNA等包裹物在细胞间穿梭,精准传递信号,还能如实反映发货细胞的真实状态。过去用血检、影像学都抓不住这种微观差异,EVs的蛋白质组图谱,刚好能撬开不同心肌区域的分子黑箱。
瑞典团队先给大鼠注射异丙肾上腺素模拟人类心碎综合征,成功诱导出「心尖瘫软、心底正常」的典型状态。24小时后,他们把大鼠心脏切成米粒大小的组织块,用酶消化加梯度离心的方法,从心尖和心底分别分离出高纯度EVs——这些囊泡在电子显微镜下呈现出典型的杯状形态,直径只有50到400纳米,还带着CD63、TSG101等「快递员专属工牌」。
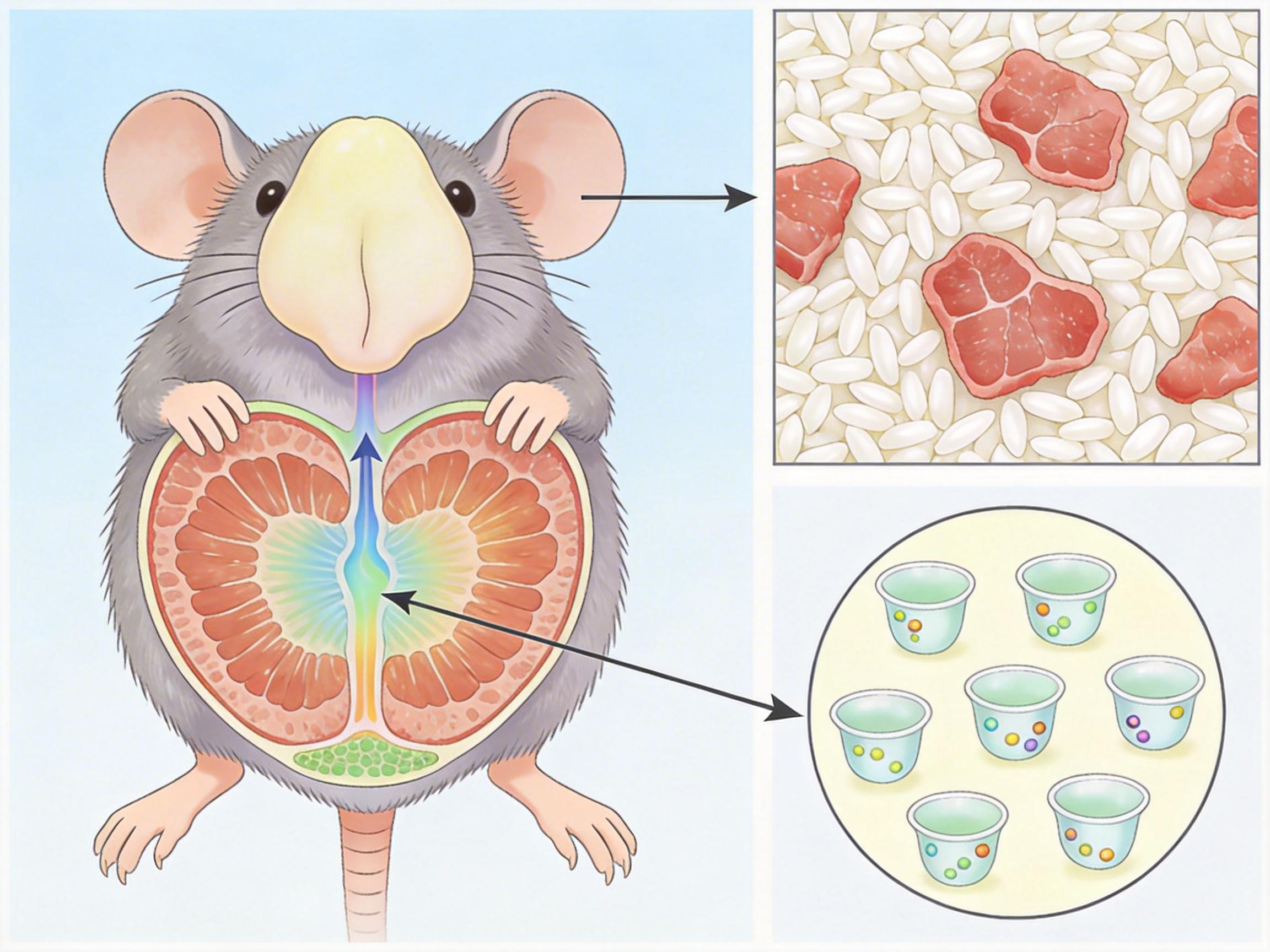
接下来的质谱分析结果,直接颠覆了此前的认知:健康大鼠的心尖和心底EV蛋白组几乎完全一致,就像同一家快递站发出的包裹;但心碎综合征发作后,心尖部EV的蛋白谱发生了天翻地覆的变化,而心底部的EV几乎没什么改变——这直接证实,心碎综合征是一种高度区域特异性的损伤,哪怕共享同一套血液供应和应激刺激,心尖细胞经历的是完全不同的分子风暴。
研究人员在受损伤的心尖EV里,找到了238个和正常心尖差异显著的蛋白,以及562个和自身心底差异显著的蛋白。这些变化像一份清晰的「损伤报告」,把心尖部的困境暴露无遗:
上调的蛋白集中在免疫反应、炎症信号、组织修复和MAPK细胞存活通路——相当于心尖细胞一边向外发送「紧急求救」信号,召唤免疫细胞过来清理损伤,一边启动自救程序,激活促生存通路试图保住自己。
但真正致命的是下调的蛋白:几乎全部和线粒体功能相关,包括电子传递链复合物I、IV的关键亚基。线粒体是细胞的「能量工厂」,负责生产心肌收缩必需的ATP,这些关键亚基的减少,直接让心尖细胞的能量供应陷入瘫痪——这就是心尖部「瘫软」的核心原因。
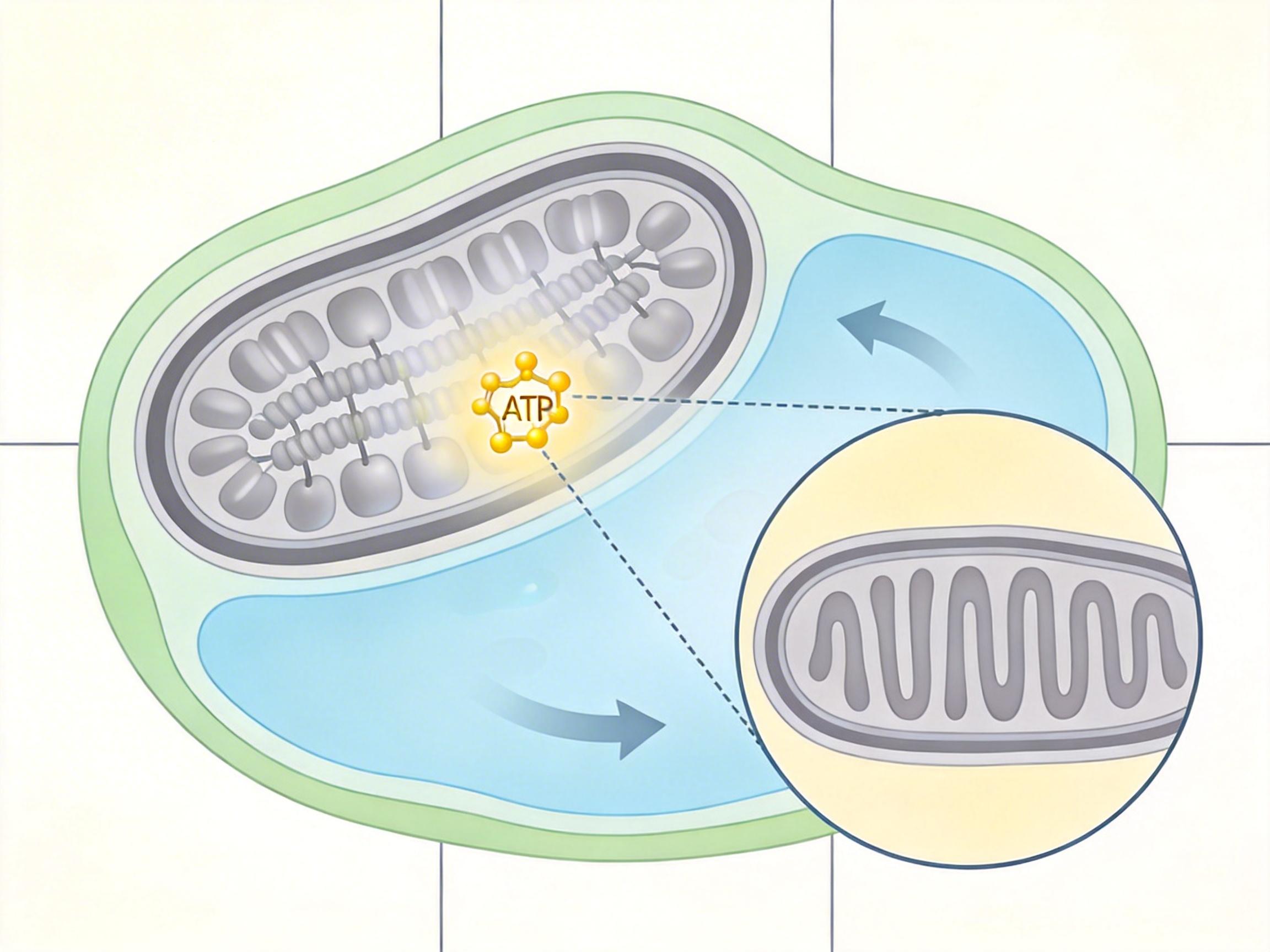
更有意思的是,通过加权基因共表达网络分析,研究人员还发现脂质代谢蛋白和炎症蛋白形成了紧密的互作网络,这和他们之前观察到的病理变化完全吻合:应激后6小时心肌出现水肿和脂质堆积,24小时炎症细胞开始浸润,EV的蛋白图谱就像一部实时记录的「损伤日志」,完整呈现了心脏从受伤到自救的全过程。
这项研究最有价值的地方,在于它给心碎综合征的诊断和治疗打开了全新的视角。
一方面,这些从心脏组织里释放的EV最终会进入血液循环,如果能在患者血液中捕获到类似的特异性蛋白组合——比如某些炎症标志物或线粒体功能相关蛋白,就能开发出比现有血检更精准的诊断工具,甚至能预测患者的恢复速度和远期死亡风险。要知道,此前医生只能靠排除法诊断心碎综合征,很容易和心梗混淆,而EV标志物能实现真正的「精准识别」。
另一方面,研究中发现的MAPK等促生存信号通路上调,提示心脏本身就有自救能力。未来或许可以通过药物调控这些EV的生成或内容,比如强化促生存蛋白的传递,或者补充线粒体相关的修复分子,帮心脏更快、更彻底地恢复。
不过我认为,这项研究目前还有明显的局限性:所有数据都来自动物模型,而且只观察了发病后24小时这一个时间点。心碎综合征是一个动态的过程,从急性发作到完全恢复的几周里,EV的「快递单」会怎么变化?这些EV到底是心肌细胞、成纤维细胞还是内皮细胞分泌的?它们离开心尖后又会去向哪里?这些问题都还没有答案,离真正的临床应用还有很长的路要走。
当我们说「心碎了」的时候,原来心脏真的会发生物理层面的损伤。过去我们只看到了心尖和心底的功能差异,现在通过EVs这个「分子窗口」,终于能读懂心脏内部的微观对话——原来在我们看不见的地方,细胞正在用自己的方式求救、自救。
「心碎不是矫情,是真实的细胞风暴。」这句话或许能让我们重新看待情绪对身体的影响:那些看似无形的悲伤和应激,其实在细胞层面掀起了惊涛骇浪。而EVs的发现,不仅让我们更懂心脏,也让我们更懂自己——原来每一次情绪波动,都在身体里留下了分子级的印记。