对抗知识焦虑,从看懂这条开始
App 下载
大脑'失调'新解:靶向药175逆转自闭症行为,意味着什么?
杨欣王玉田团队|突触功能|药物175|精神分裂症|自闭症谱系障碍|神经退行性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
杨欣王玉田团队|突触功能|药物175|精神分裂症|自闭症谱系障碍|神经退行性疾病|医学健康
想象大脑是一场宏大而精密的交响乐,亿万个神经元如同乐手,通过名为“突触”的连接,共同奏响思维、情感与记忆的乐章。然而,对于自闭症谱系障碍(ASD)和精神分裂症患者而言,这场交响乐似乎总有几个关键声部跑调、失声。他们可能被困在重复的行为模式中,或是在社交的喧嚣里感到无所适从。多年来,科学家们一直在寻找那位“失声”的乐手,试图理解并修复这微妙的失衡。现在,一束光似乎穿透了迷雾。
近期,由不列颠哥伦比亚大学、深圳先进技术研究院及复旦大学的杨欣、王玉田团队发表在《科学·进展》上的一项研究,为这场“失调”的交响乐带来了一把前所未有的精准“调音钥匙”。他们宣布,成功开发出一种名为**“175”的先导化合物**。
这不仅仅是一种新药,更是一种策略的胜利。研究证实,化合物175能够特异性地增强大脑中一种关键受体——GluN2B-NMDAR的功能。在模拟自闭症和精神分裂症的小鼠模型中,它的介入显著逆转了动物的焦虑、社交障碍和认知缺陷。这一突破,为理解这些复杂疾病的根源提供了全新的工具,并为开发精准靶向药物铺平了道路。
要理解这一突破的重要性,我们必须先认识这位“关键乐手”——NMDAR(N-甲基-D-天冬氨酸受体)。它就像大脑中负责学习和记忆的“总开关”或“门禁系统”,控制着神经元之间的信息流动和连接强度。这个门禁系统由多个亚基(部件)构成,其中GluN2B亚基在生命早期的大脑发育中扮演着至关重要的角色。
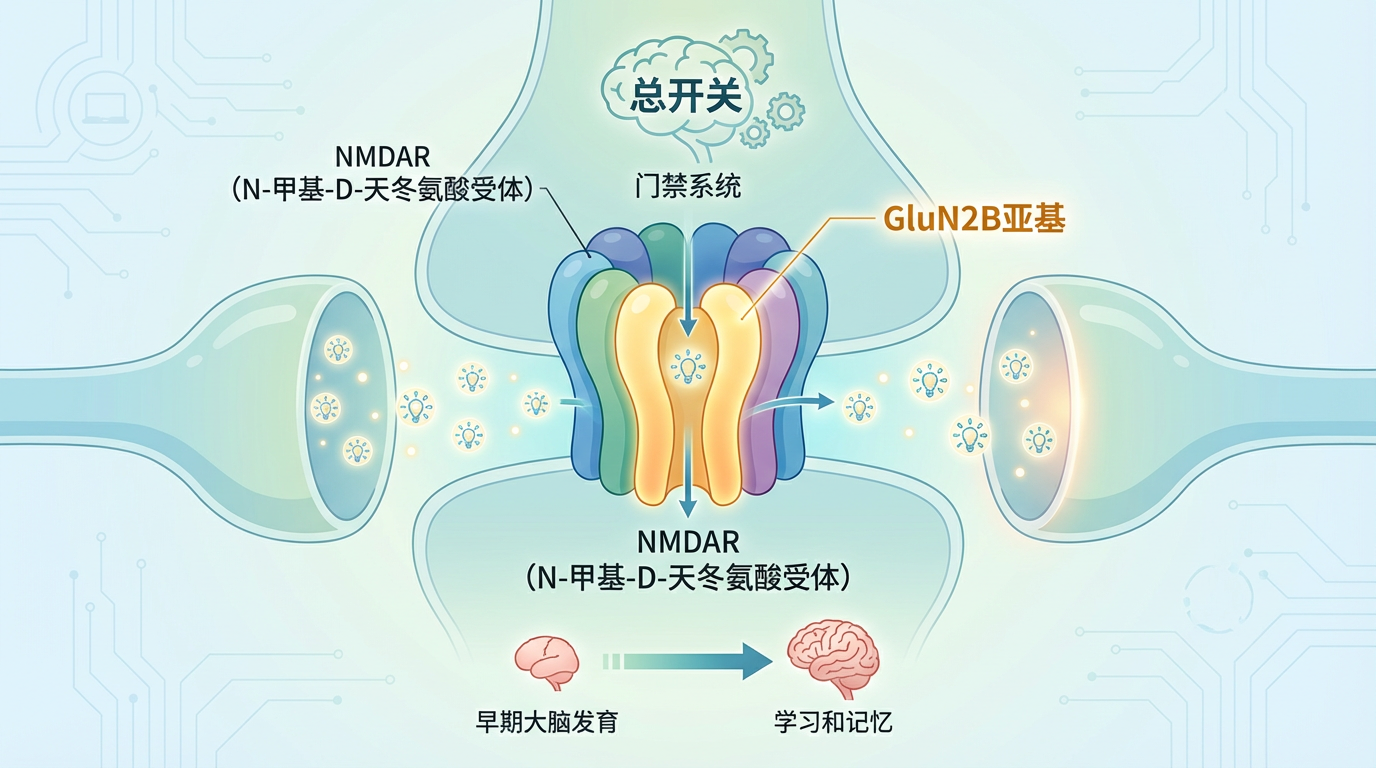
遗传学研究早已发现,编码GluN2B的GRIN2B基因如果出现功能缺失,与自闭症的风险显著相关。这指向一个明确的病理机制:GluN2B功能不足,导致大脑的“学习之门”无法正常工作,进而引发一系列神经发育问题。然而,治疗的困境在于,过去的药物就像一把万能钥匙,试图打开所有NMDAR相关的门,缺乏对GluN2B的选择性。这种“地毯式轰炸”往往带来严重的副作用,成药性极差。科学家们需要的,是一把只开GluN2B这把锁的钥匙。
寻找这把钥匙的过程,堪称现代药物研发的典范。研究团队借助强大的计算机虚拟筛选技术,在超过130万个小分子化合物的数据库中进行“大海捞针”。通过模拟计算,他们预测哪些分子可能与GluN2B亚基上的特定位点结合。

经过层层筛选和体外细胞实验的严格验证,化合物175脱颖而出。它的惊人之处在于其高度的选择性:它增强GluN2B-NMDAR功能的效力,比增强功能相似的GluN2A亚基要强约56倍。更巧妙的是,它的作用机制如同一个“智能增压器”——只在神经活动活跃、需要加强信号传递时才显著发力,而对大脑的正常基础活动影响甚微。这极大地降低了过度激活神经元可能带来的毒性风险,展现了良好的安全前景。
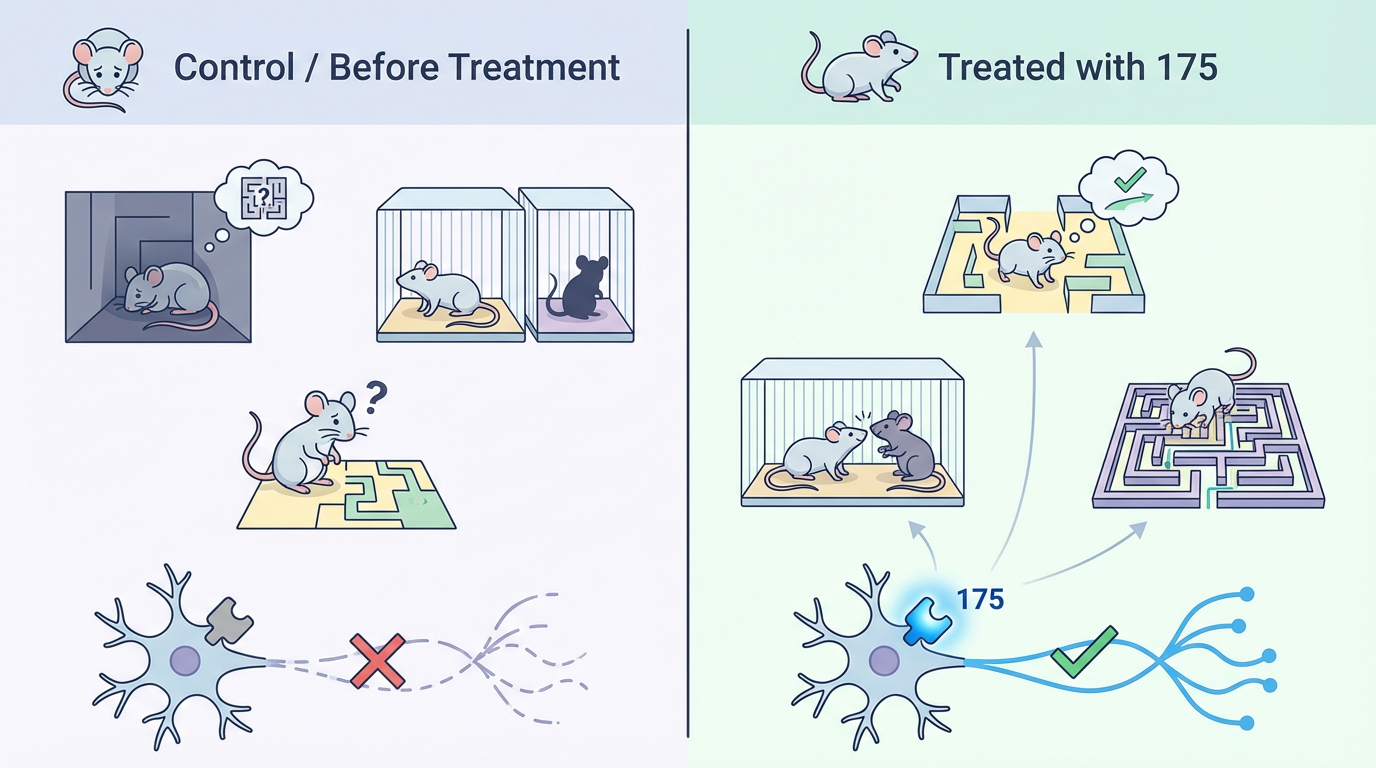
真正的考验在活体动物模型中展开。研究团队将化合物175应用于两种经典的疾病小鼠模型:
结果令人振奋。在两种模型中,接受175治疗的小鼠都表现出显著的行为改善。它们焦虑水平下降,更愿意探索新环境;社交缺陷得到逆转,重新表现出对新同伴的兴趣;受损的工作记忆也得到了有效挽救。这表明,通过精准增强GluN2B的功能,可以直接纠正不同遗传背景下神经环路的失衡,从而改善核心症状。
化合物175的故事揭示了精准医疗的深刻内涵,而另一家公司GRIN Therapeutics的在研药物Radiprodil则从另一面印证了这一点。与175增强功能不足的GluN2B不同,Radiprodil旨在抑制功能“过度活跃”的GluN2B。
在某些罕见的GRIN基因相关神经发育障碍中,基因突变导致GluN2B功能过强,引发严重的癫痫和发育迟缓。Radiprodil作为一种负向调节剂,精准地为“过热”的受体降温。凭借其在临床试验中将患者癫痫发作频率中位数降低86%的惊人数据,它已获得美国FDA的“突破性疗法”认定,正向上市发起冲刺。
这两款药物,一“增”一“抑”,完美诠释了精准医疗的未来:锁定同一个靶点(GluN2B),根据疾病的具体病理(功能缺失或功能获得),施以完全相反但同样精准的干预。
尽管化合物175带来了巨大的希望,但从实验室走向临床,依然有很长的路要走。研究团队坦言,其长期用药的安全性、耐受性仍需系统评估,并且需要在更多、更接近人类患者遗传背景的疾病模型中进行验证。
然而,这项研究的意义远不止于一个候选药物。它提供了一个强有力的范例,证明了通过对大脑受体亚基进行超高选择性的精细调节,来治疗复杂神经精神疾病的可行性。它将引领科学家们从过去“一刀切”的治疗思路,转向为每一种大脑的“失调交响乐”量身定制“调音方案”。这束穿透迷雾的光,正照亮着通往神经精神疾病精准治疗的新大陆。