对抗知识焦虑,从看懂这条开始
App 下载
沉默一个基因,破解乳腺癌骨转移死循环
浙江大学医学院附属第二医院|纳米平台|TREM2基因|骨转移|三阴性乳腺癌|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
浙江大学医学院附属第二医院|纳米平台|TREM2基因|骨转移|三阴性乳腺癌|肿瘤学|医学健康
当三阴性乳腺癌细胞钻进骨头,等待患者的往往是一场无解的恶性循环:肿瘤催生的“叛变”免疫细胞会死死压制抗癌防线,还会招来啃噬骨骼的破骨细胞——骨头越碎,肿瘤长得越快,直到把患者拖入绝境。过去医生对此几乎束手无策,但浙江大学医学院附属第二医院的团队,用一个分层靶向的纳米平台,把这场死局撕开了一道口子:他们让超过50%的“叛变”免疫细胞倒戈,把抗癌T细胞的战斗力翻了一倍,甚至让79.5%的骨转移肿瘤进展停了下来。这一切,只需要精准沉默一个叫TREM2的基因。
三阴性乳腺癌是乳腺癌里最凶悍的亚型,它没有雌激素受体等常见靶点,70%的晚期患者会发生骨转移。一旦癌细胞钻进骨头,就会迅速驯化骨微环境里的“原住民”:首先是髓样细胞——这群本应守护健康的免疫细胞,会被癌细胞分泌的物质“策反”,变成肿瘤相关巨噬细胞(TAMs),一边分泌IL-10、TGF-β等因子压制抗癌T细胞,一边给破骨细胞“发信号”。
破骨细胞是骨头里的“拆迁队”,正常情况下负责替换老化的骨组织,但被癌细胞激活后,它们会疯狂啃噬骨骼。骨头被啃碎后,里面藏着的生长因子会被释放出来,反过来又给癌细胞“喂饭”,让它们长得更快、扩散得更远。就这样,免疫抑制、骨溶解、肿瘤生长,形成了一个牢不可破的死循环。而TREM2基因,就是掌控这场叛变的“总开关”——它能直接指挥髓样细胞变成帮凶,还能加速破骨细胞的生成。
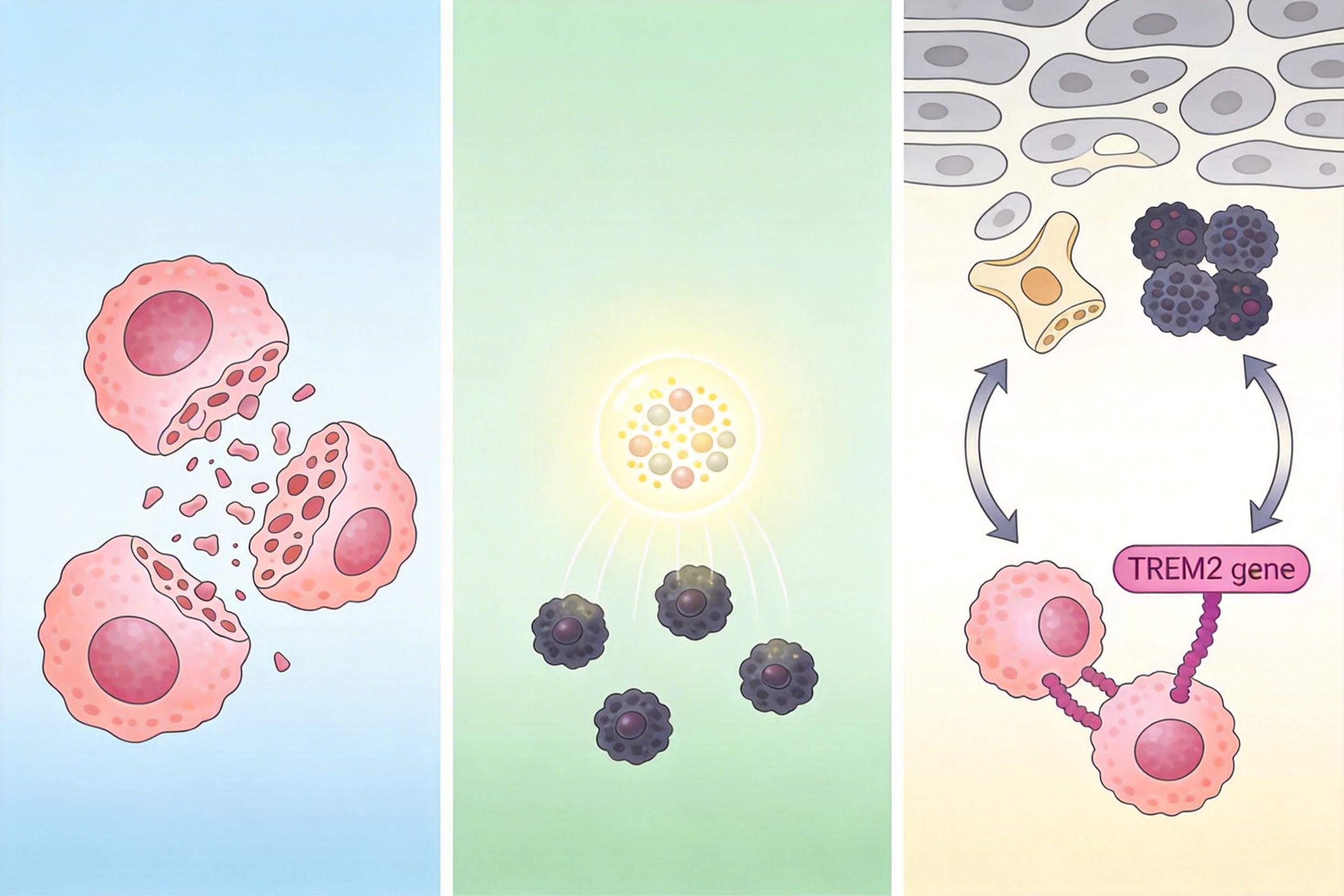
要打破这个死循环,关键是精准关掉TREM2,但难点在于不能“滥杀无辜”——正常组织里的TREM2有修复损伤的作用,盲目抑制会引发副作用。浙大团队的解决方案,是一个三层设计的纳米平台siTREM2@ETP-PEOz-OMVs:
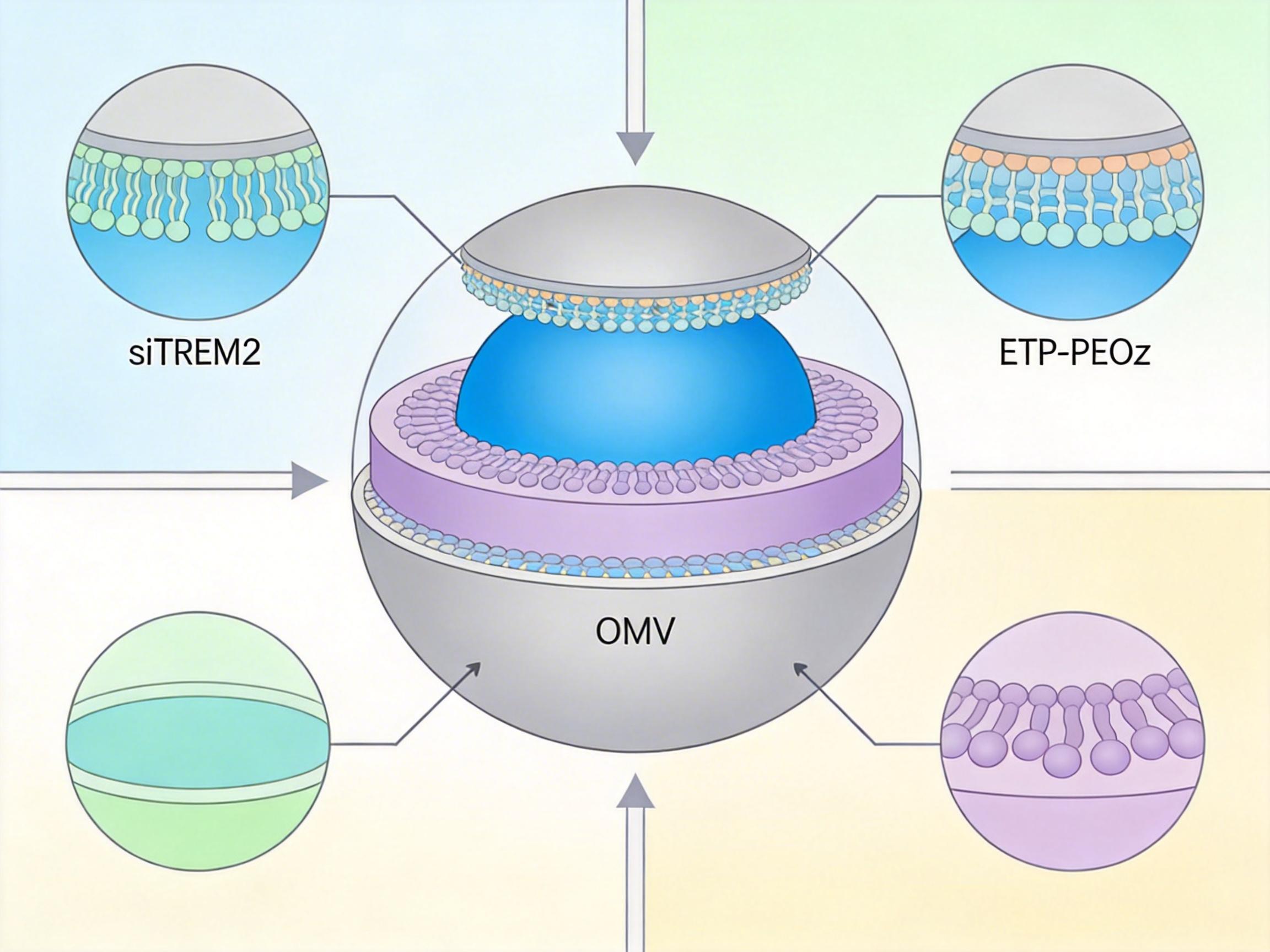
第一层是“导航”。他们用噬菌体展示技术筛选出了能精准识别三阴性乳腺癌细胞的肽段ETP,让纳米颗粒能直奔骨转移病灶,不会在正常组织里乱跑。
第二层是“触发开关”。肿瘤微环境是酸性的,他们给纳米颗粒裹上了pH响应型聚合物PEOz——一旦进入酸性的肿瘤区域,PEOz就会自动分解,释放出里面的外膜囊泡(OMVs)。
第三层是“精准斩首”。OMVs是细菌分泌的天然囊泡,自带能绑定髓样细胞的TLR4受体,能精准钻进叛变的髓样细胞里,释放出沉默TREM2的siRNA。
实验数据直白得惊人:TREM2被沉默后,超过50%的肿瘤相关巨噬细胞倒戈成了能激活免疫的促炎表型,CD4+和CD8+T细胞的浸润量直接翻了一倍,破骨细胞的生成被抑制了70%以上,最终让骨溶解介导的肿瘤进展被摁住了79.5%。
这个纳米平台的突破,给三阴性乳腺癌骨转移患者带来了新希望,但要真正走进临床,还有三道坎要跨:
首先是规模化生产的难题。纳米颗粒的粒径、形态和载药稳定性,每一批都要严格一致,还要符合药品监管的质量标准,这对生产工艺的要求极高。
其次是安全性的验证。虽然动物实验里没发现明显的系统毒性,但纳米颗粒进入人体后,会不会在肝脾等器官蓄积?会不会引发不可预测的免疫反应?这些都需要长期的临床观察。
最后是患者分层的问题。TREM2在不同患者体内的表达水平有差异,不是所有人都能获得同样的疗效,需要找到精准的生物标志物,筛选出最适合的患者群体。
更值得关注的是,TREM2在不同肿瘤里的作用还存在争议——它在有些癌症里是帮凶,在有些癌症里却可能扮演着“守护者”的角色,这意味着这个疗法不能直接套用到所有肿瘤上。
当我们把视线从实验室的培养皿拉回病房,会发现这场针对TREM2的精准打击,本质上是人类在和癌细胞的“驯化术”较劲——过去我们只能被动地对抗肿瘤,现在终于能主动改写肿瘤微环境的“规则”。
精准医学的魅力正在于此:它不是用一种药物打败所有癌症,而是像一把定制的钥匙,精准插进癌细胞的“锁孔”里,把被颠倒的免疫秩序重新扳回来。精准靶点,才是破局癌症的核心。也许未来的某一天,骨转移不再是乳腺癌患者的死刑判决书,而只是一场可以被精准控制的“局部战役”。