对抗知识焦虑,从看懂这条开始
App 下载
边缘器官能救了:铁死亡抑制剂守住移植生命线
缺血再灌注|肺移植|边缘器官|铁死亡抑制剂|FXT-001|新药研发|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
缺血再灌注|肺移植|边缘器官|铁死亡抑制剂|FXT-001|新药研发|医学健康
当一台肺脏从循环死亡的捐献者体内取出时,它已经在缺血状态下“挣扎”了超过12小时——按照传统标准,这属于连移植资格都没有的“边缘器官”。但在比利时安特卫普大学的实验室里,这枚原本被判“死刑”的肺脏,在灌注了一种名为FXT-001的药物后,血管阻力下降30%,水肿完全消退,甚至恢复了正常的气体交换功能。这不是科幻场景,而是2026年《Cell》杂志上公布的真实实验结果:新一代铁死亡抑制剂,正把那些原本被丢弃的器官,重新拉回拯救生命的队列。为什么这种药物能创造奇迹?我们得先从器官移植那道“致命的坎”说起。
你可以把移植器官的缺血再灌注过程,想象成一块铁被丢进潮湿的空气:缺血时细胞像缺氧的鱼,勉强维持呼吸;而当血液重新涌入的瞬间,氧气不是“救命稻草”,而是引发“氧化风暴”的火源——大量自由基如同飞溅的火星,顺着细胞膜上的不饱和脂肪酸蔓延开。
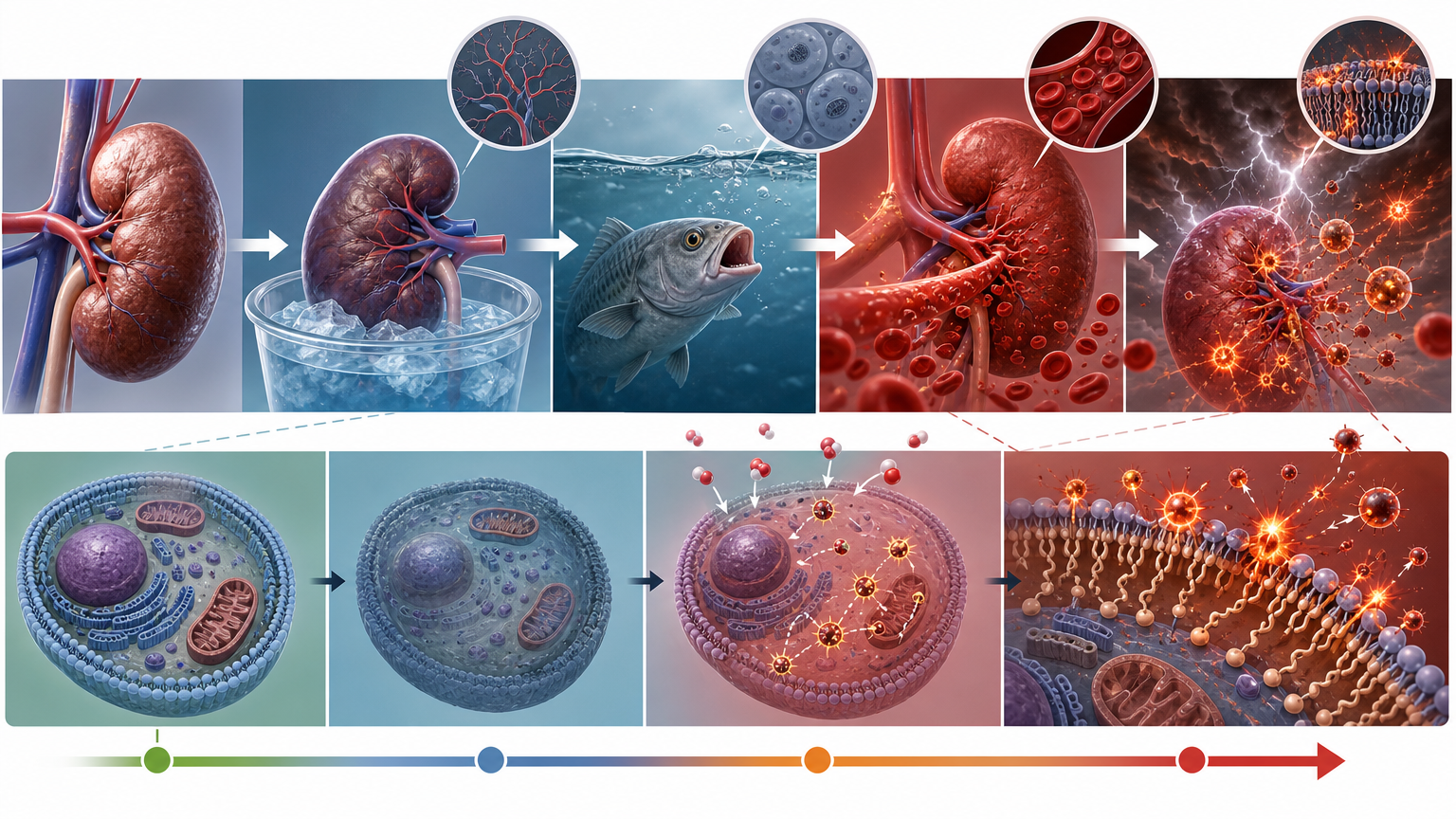
这就是铁死亡的核心:在游离铁离子的催化下,细胞膜的不饱和脂肪酸被过度氧化,就像铁被慢慢锈穿一样,最终导致细胞彻底破裂。在肝脏和肺移植中,这种“生锈”式死亡是早期器官衰竭的头号凶手——仅在肺移植中,就有36%的早期功能障碍由铁死亡直接导致。
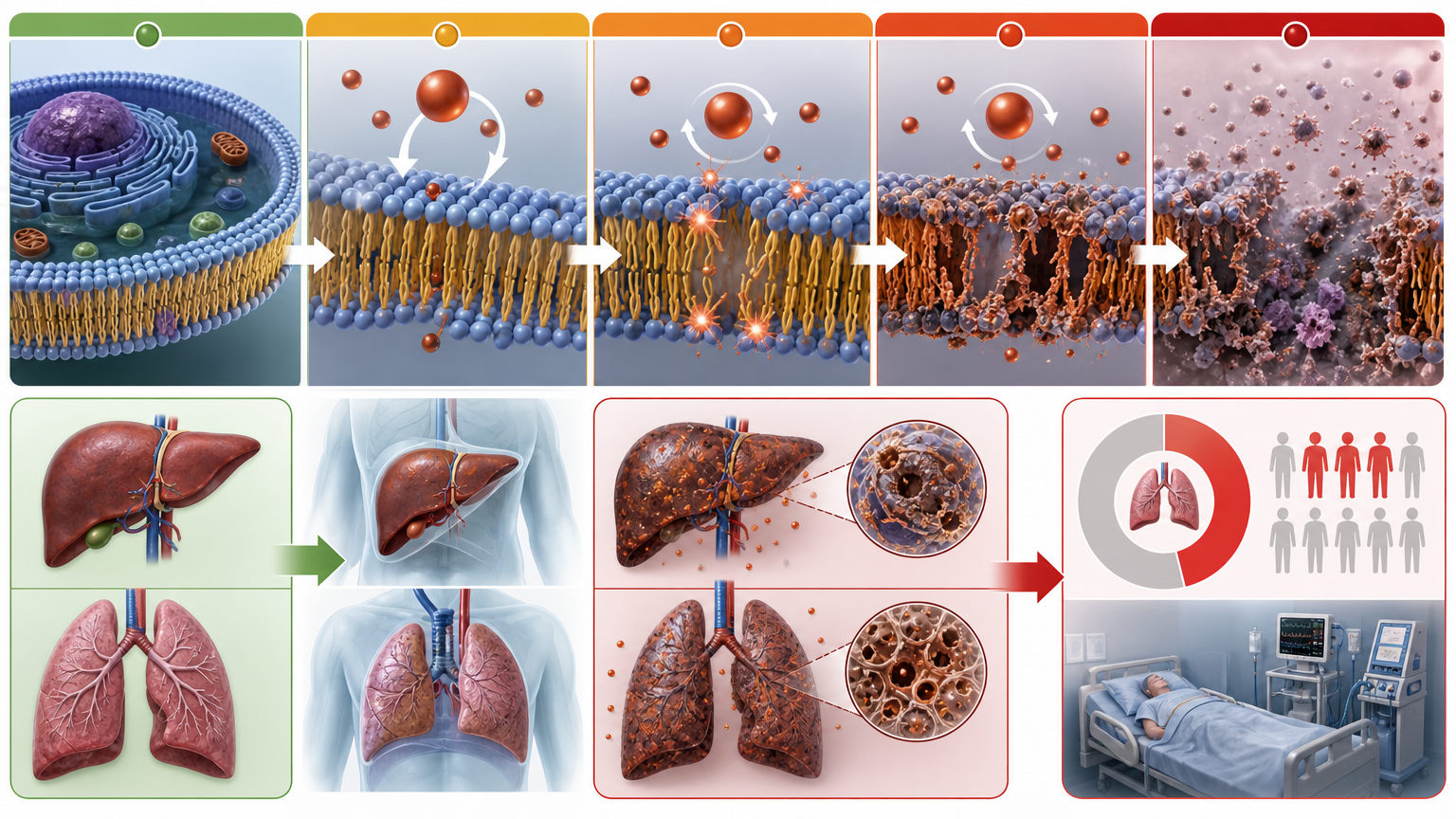
更棘手的是,随着器官短缺加剧,“边缘供体”器官的使用率越来越高:老年器官、脂肪肝器官、循环死亡捐献的器官,这些本就脆弱的组织,对铁死亡的抵抗力几乎为零。
第一代铁死亡抑制剂的困境,就像用湿抹布去扑山火:要么是铁螯合剂只能抓住游离铁,却挡不住已经燃起的自由基;要么是抗氧化剂能灭火,却没法斩断铁离子这个“火源”。而且这些药物要么溶解度差,要么在体内代谢太快,根本没法在器官移植的关键窗口期发挥作用。
FXT-001的创新之处,在于它是一个“双重捕获者”:
在猪肝移植模拟实验中,它让肝脏的脂质过氧化标志物下降了60%,肝细胞存活率提升了45%;而在人类边缘肺脏的灌注实验里,未用药的肺脏在4小时内功能完全恶化,用药后的肺脏却维持了正常的生理指标——这是首次在人类离体器官上,证实铁死亡抑制剂的保护效果。
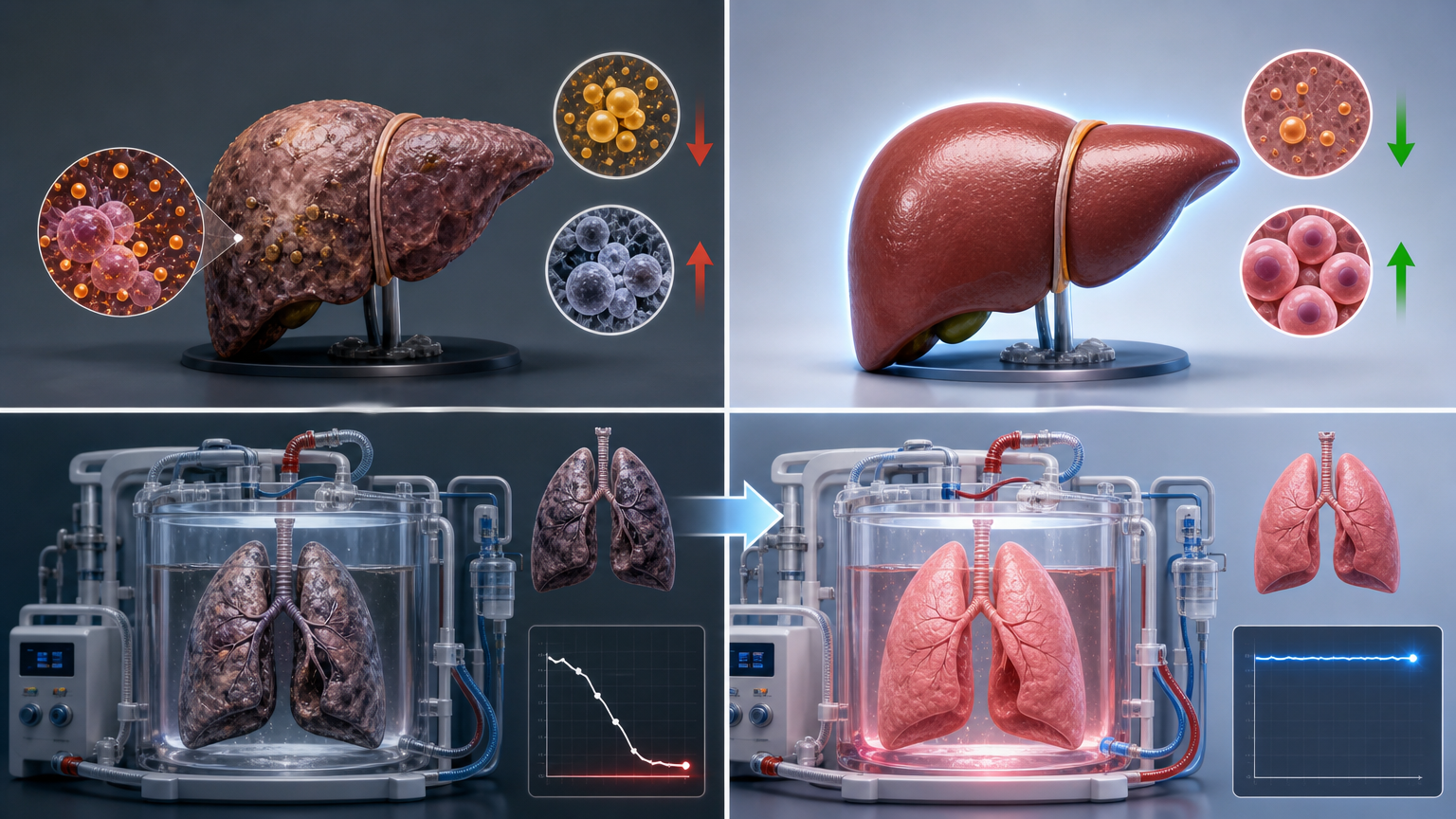
更关键的是,如今普及的体外机械灌注技术,给了这种药物精准发力的“窗口”:在器官移植前的体外保存阶段,药物可以直接通过灌注液进入器官组织,既避免了全身用药的副作用,又能让药物在最需要的时刻集中发挥作用。
当然,这剂“器官救心丸”并非完美无缺。目前的实验仅停留在离体器官和大型动物模型阶段,进入人体临床试验后,还需要解决三个核心问题:
首先是个体差异。不同供体器官的铁代谢水平、氧化应激状态千差万别,如何根据器官的具体情况调整药物剂量,实现精准保护,仍是未知数。
其次是长期安全性。铁死亡不仅会损伤移植器官,也参与免疫细胞的功能调节——过度抑制铁死亡,是否会影响受体的免疫排斥反应?这需要更长时间的观察验证。
最后是成本问题。体外机械灌注设备本身价格不菲,再加上新型抑制剂的使用,会不会进一步推高移植手术的成本,反而让原本受益的患者望而却步?
研究团队已经在FXT-001的基础上,开发出了药代动力学更优的FXT-002和FXT-003,但这些问题的答案,还得等临床试验给出结果。
当我们谈论器官移植时,我们谈论的从来都不只是技术,而是生命的可能性。每一枚被拯救的边缘器官,背后都是一个等待被填满的病床,一个盼着家人回家的家庭。
FXT-001的意义,不仅在于它找到了阻断铁死亡的新路径,更在于它让我们看到:那些原本被认为“不够好”的器官,那些被医学标准过滤掉的生命机会,其实还有被挽救的可能。
给器官一次机会,就是给生命一次机会。 未来,当更多边缘器官能顺利走上手术台,我们或许会发现,所谓的“医疗极限”,不过是下一次突破的起点。