对抗知识焦虑,从看懂这条开始
App 下载
基因的“幽灵疤痕”:完美修复下的永久性创伤
遗传信息传递|三维基因结构|染色质疲劳|DNA修复|分子细胞生物学|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
遗传信息传递|三维基因结构|染色质疲劳|DNA修复|分子细胞生物学|生命科学
在生命科学的宏伟叙事中,DNA修复常被描绘成一个英雄般的篇章。细胞拥有一套精密的“纠错系统”,能够识别并修补遗传密码上的断裂与损伤,确保生命蓝图的完整性。我们曾以为,一次成功的修复,就像抹去书页上的一个错字,让一切恢复如初。然而,一项发表于《科学》杂志的颠覆性研究揭示了一个令人不安的真相:即使DNA序列被完美修复,断裂处依然会留下一个看不见的“幽灵疤痕”。这个伤疤不记录在DNA的碱基序列里,而是烙印在其三维的折叠结构上。这种结构性的“创伤后遗症”,不仅会持续抑制周边基因的功能,甚至可以像遗传信息一样,代代相传,形成一种被科学家命名为**“染色质疲劳”(chromatin fatigue)**的持久损伤。
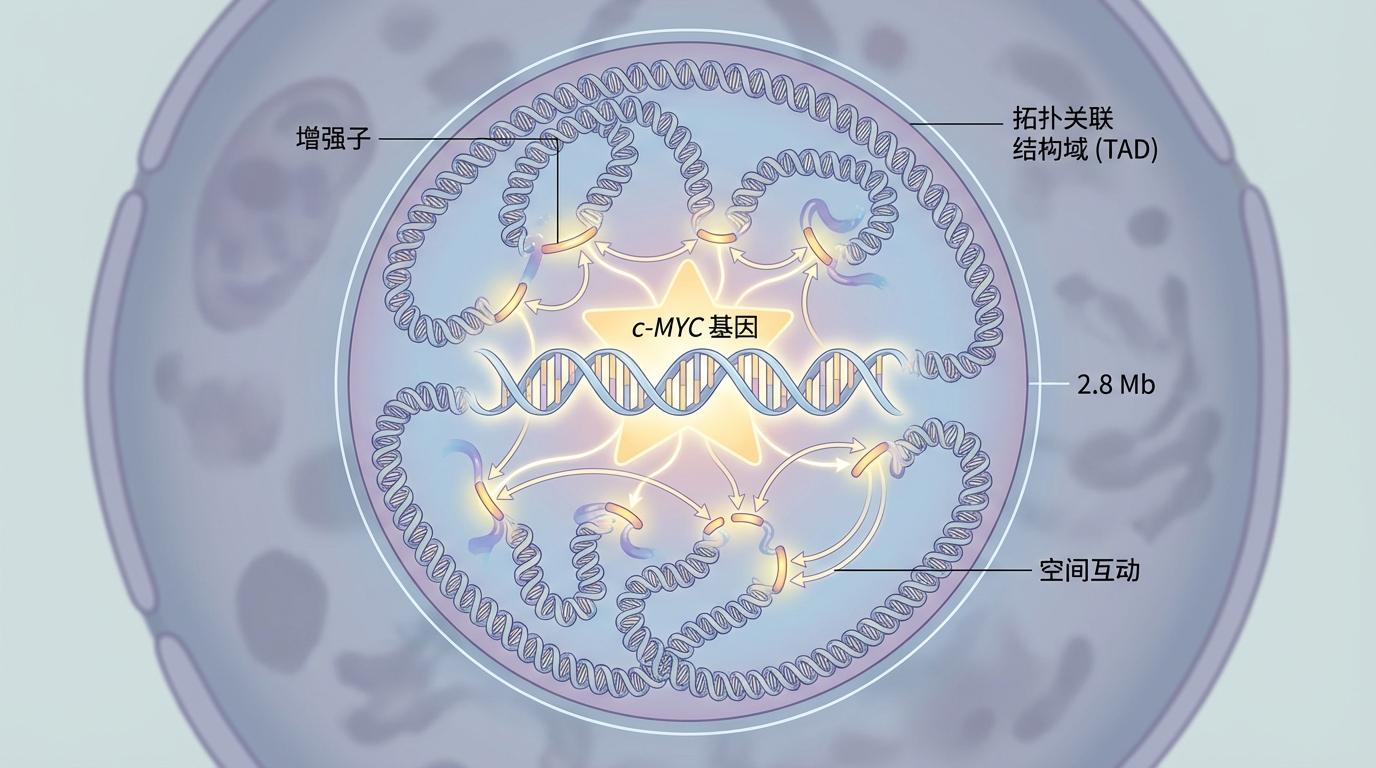
故事始于丹麦哥本哈根大学的一个顶尖实验室。由科学家Jiri Lukas领导的团队,将目光投向了一个在细胞生命活动中举足轻重的“明星”基因:c-MYC。它不仅是细胞生长和增殖的关键调控者,更重要的是,它的表达高度依赖于其所在的三维空间结构——一个典型的“拓扑敏感”基因。c-MYC被包裹在一个约2.8兆碱基(Mb)的巨大“社区”里,这个社区在遗传学上被称为拓扑关联结构域(Topologically Associated Domains, TAD)。在TAD这个社区内部,基因和调控元件(如增强子)通过空间上的紧密折叠而频繁互动,协同工作。
Lukas团队提出了一个大胆的问题:如果在这个社区的任意一处制造一点麻烦——一次DNA双链断裂(DSB),即使麻烦点离c-MYC的“住宅”很远,会发生什么?
借助CRISPR-Cas9这把精准的“基因剪刀”,研究人员在c-MYC所在的TAD内部的12个不同位置,制造了单一、精准的DNA双链断裂。随后,他们静静观察细胞的自我修复过程。
结果令人震惊。细胞的修复机制在24小时内就高效地完成了任务,DNA序列恢复完整。然而,c-MYC基因却“失声”了。无论断裂点发生在社区的哪个角落,哪怕距离c-MYC基因本身有上百万个碱基对之遥,c-MYC蛋白的表达量都出现了显著且持续的下降。这种沉默效应持续了至少96小时,细胞已经历数次分裂,但这份“沉默的记忆”却被忠实地传递给了每一个子代细胞。
序列完美无瑕,功能却永久受损。谜题的答案,显然隐藏在更高维度的结构之中。为了亲眼“看见”这个幽灵疤痕,研究团队动用了两项尖端技术。
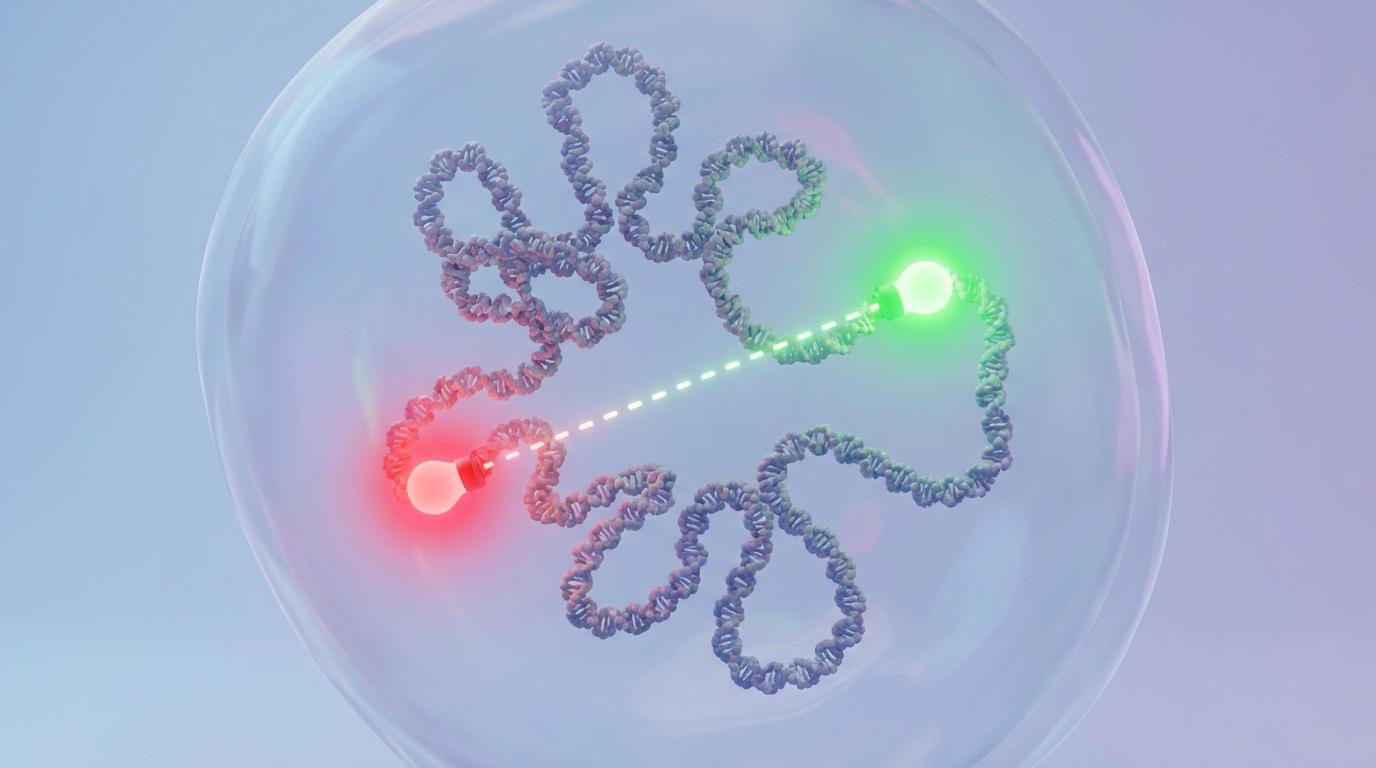
首先,他们使用了**三维DNA荧光原位杂交(3D DNA FISH)**技术。他们给c-MYC所在TAD的两端分别挂上不同颜色的“荧光灯笼”,通过测量两个灯笼在细胞核内的三维空间距离,来判断整个TAD社区的“拥挤”程度。
数据清晰地表明,修复后的TAD在空间上变得更加松散、开放,其内部原有的紧密折叠结构被削弱了。这便是那个“结构伤疤”的宏观表现。
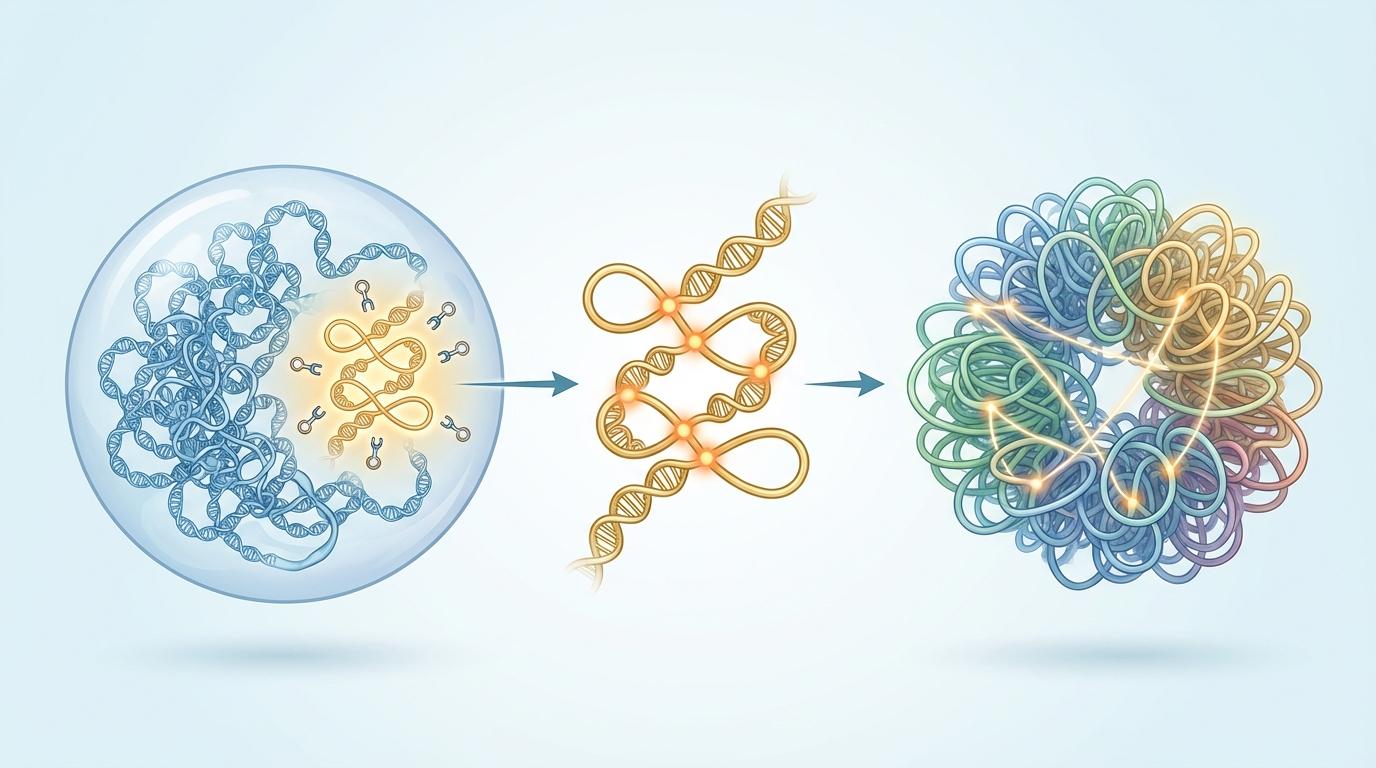
接着,通过区域捕获微C技术(Region Capture Micro-C),他们绘制了该区域DNA片段之间详细的“三维互动地图”。结果发现:
这个“一减一增”的结构重塑模式,像一道无法愈合的伤疤,永久地改变了基因组的局部地貌。修复过程虽然缝合了断口,却未能将精密的建筑结构复原。更重要的是,这种结构紊乱直接导致了功能失调。修复后的c-MYC基因对外界的生长信号变得“迟钝”,其响应速度和强度都大打折扣,仿佛变成了一个“听力受损”的接收器。
“染色质疲劳”这一概念的提出,为我们理解DNA损伤的长期后果打开了一个全新的维度,其意义远远超出了分子生物学的范畴。
1. 对基因编辑技术的警示 这项研究对以CRISPR为代表的基因编辑技术提出了一个严肃的问题。这些技术的核心原理正是通过制造DNA双链断裂来启动编辑程序。新发现表明,即使实现了完美的“在靶”修复,没有引入任何序列突变,修复过程本身就可能在目标基因及其邻近区域引发“染色质疲劳”,导致其功能被长期抑制或失调。这为基因治疗,尤其是针对胚胎的生殖系编辑,敲响了警钟:我们评估其安全性的标准,必须从一维的DNA序列,扩展到三维的染色质结构和长期的功能稳定性。
2. 解读衰老与癌症的新视角 在一个生物体的漫长一生中,细胞会不断遭受来自内外环境的DNA损伤。每一次双链断裂的修复,都可能在基因组的某个角落留下一个微小的“染色质疲劳”伤疤。单个伤疤的影响或许微不足道,但随着时间的推移,成千上万个这样的伤疤在全基因组范围内不断累积,是否会导致整个基因组的响应能力和调控精度进行性下降?这或许为我们理解细胞衰老和组织老化提供了一个全新的机制假说。同样,在癌症发展过程中,基因组的不稳定性是其核心特征之一,这些无法复原的结构伤疤,可能正是驱动正常细胞走向癌变的早期、被忽视的步骤之一。
3. 对生命韧性的重新思考 这项研究也揭示了生命在进化压力下的无奈权衡。面对DNA双链断裂这种致命损伤,细胞的首要任务是“活下去”。为了维持基因组序列的完整性,它不得不启动一套会留下永久结构伤痕的修复程序。这是一种生存的策略,但代价是功能的永久性折损。
Jiri Lukas团队的研究,如同一位高超的建筑师,带领我们超越了基因蓝图的平面文字,看到了其背后宏伟而脆弱的立体结构。它告诉我们,基因组是有记忆的,它不仅记得序列中的每一个碱基,也记得每一次创伤与修复留下的结构烙印。这些“幽灵疤痕”或许无声,却深刻地影响着细胞的命运、个体的健康,乃至物种的演化。在未来,倾听并解读这些来自基因组深处的无声叹息,将是我们理解生命、对抗疾病的全新起点。