
15 小时前

15 小时前
当一位老人记不起刚吃过的饭,当唐氏综合征孩子学不会简单的词语,当我们自己在30岁后开始忘事——这些看似无关的认知困境,背后可能藏着同一个细胞级别的「故障」:整合应激反应(ISR)的持续激活。这是细胞原本用来应对压力的生存机制,却在某些情况下变成了「记忆杀手」。2026年,贝勒医学院的团队从一种非洲猪瘟病毒身上,找到了一把能关掉这个故障的钥匙,甚至能让健康小鼠的记忆变得更好。这到底是怎么回事?
你可以把ISR理解成细胞的「应急省电模式」——当细胞遇到病毒感染、营养不足或者蛋白质折叠错误时,这个开关会被触发:先暂停大部分蛋白质的合成,减少能量消耗,同时优先生产能应对危机的「应急蛋白」,帮细胞熬过难关。

但真实的机制比这更精确:ISR通过四种激酶磷酸化翻译起始因子eIF2α,让全局蛋白质合成减速,却选择性激活转录因子ATF4的翻译,启动应激适应程序。正常情况下,危机解除后,PPP1R15B和PP1组成的磷酸酶复合物会给eIF2α「去磷酸化」,让细胞恢复正常运作。
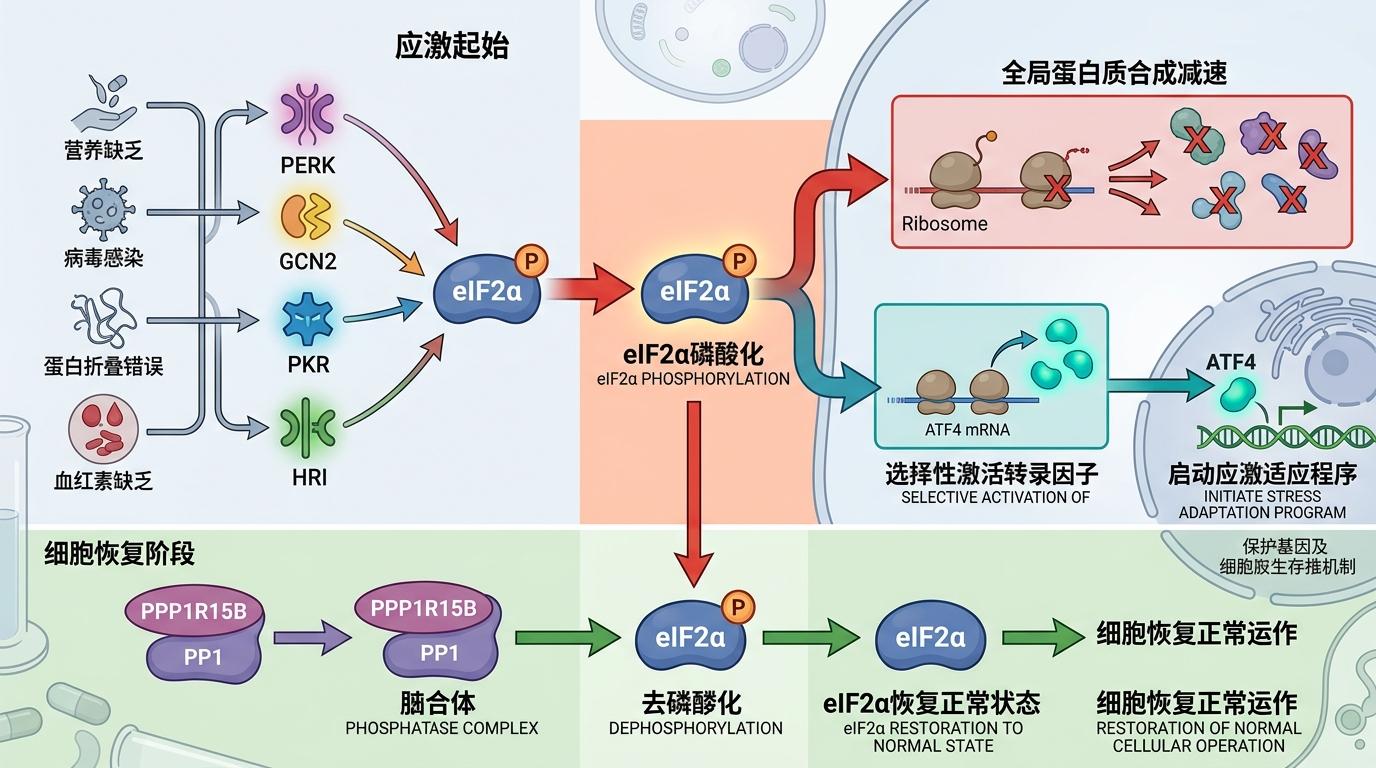
麻烦出在「持续激活」上。比如携带PPP1R15B R658C突变的小鼠,这个突变让磷酸酶复合物不稳定,ISR一直处于开启状态,蛋白质合成长期受抑,海马区突触可塑性下降,最终出现长期记忆缺陷。研究人员通过基因手段关闭ISR后,小鼠的认知功能居然恢复了——这直接坐实了ISR持续激活和认知障碍的因果关系。
既然ISR持续激活是问题核心,那能不能直接关掉它?科学家把目光投向了病毒——这些靠劫持细胞生存的「老油条」,早就进化出了对付ISR的办法。
非洲猪瘟病毒编码的DP71L蛋白,就是其中的佼佼者。它是PPP1R15B的病毒同源物,只保留了和PP1、eIF2结合的关键结构,是目前发现的最小的ISR抑制剂。它能精准地让eIF2α去磷酸化,把卡在「应急模式」的细胞拉回正常状态。
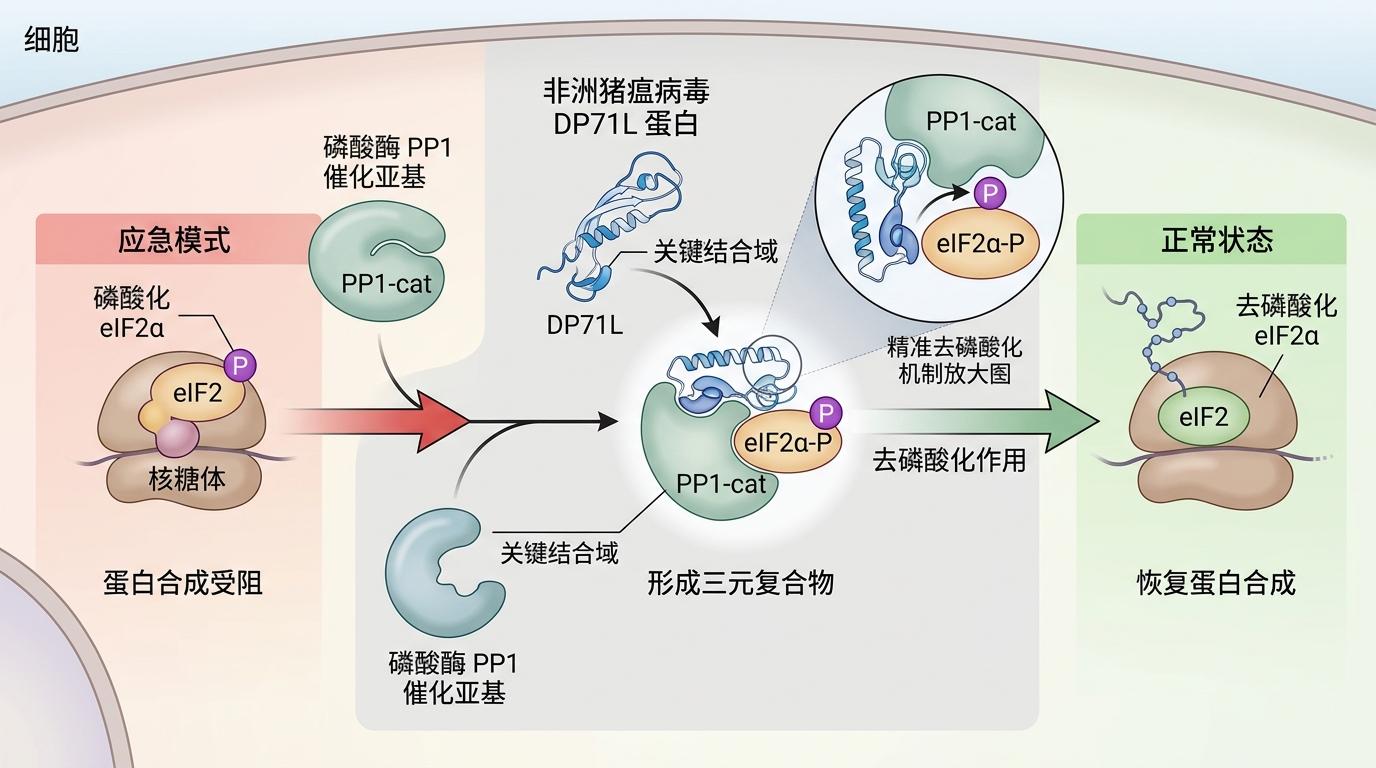
实验结果超出了预期:给患有唐氏综合征、阿尔茨海默病的小鼠注射DP71L,它们的突触缺陷得到逆转,记忆功能显著改善;即便是健康小鼠,DP71L也能增强它们的突触可塑性,让它们的长期记忆变得更好。更有意思的是,DP71L还能通过抑制ISR,阻断肿瘤细胞的代谢重编程和免疫逃逸——这个原本为了帮病毒逃避免疫的蛋白,成了跨界的「疾病克星」。
当然,挑战依然存在。比如如何让DP71L安全地穿过血脑屏障,如何避免过度抑制ISR带来的副作用——毕竟ISR本身是细胞的生存机制,完全关掉可能让细胞失去应对真实危机的能力。
ISR的影响远不止认知障碍。瑞典哥德堡大学的研究发现,衰老会通过表观遗传激活ISR,让肺腺癌放弃原发肿瘤的生长,转而获得转移能力——ATF4驱动的上皮和代谢可塑性,成了肿瘤扩散的「通行证」。
另一项发表在《自然》的研究则揭示了ISR的免疫逃逸机制:ATF4会诱导脂质运载蛋白LCN2的表达,吸引免疫抑制性巨噬细胞进入肿瘤微环境,把T细胞挡在外面。而敲除ATF4或者使用抗LCN2抗体,就能重新激活抗肿瘤免疫反应。
这意味着ISR是一个横跨神经、肿瘤、免疫的「核心调控枢纽」。从病毒蛋白中获得的灵感,或许能为多种疾病的治疗打开新的大门——比如用ISR抑制剂阻止肿瘤转移,用ISR激活剂增强细胞的应激抵抗能力。
当我们把目光从宏观的疾病症状,聚焦到细胞内的一个小小开关,才发现生命的复杂远超想象:原本用来保护我们的机制,可能在某个突变、某次衰老、某个病毒感染的节点,变成伤害我们的元凶;而那些让我们谈之色变的病毒,却在亿万年的进化中,藏着治愈我们的密码。
「生存机制的失衡,往往是疾病的根源。」这句话不仅适用于ISR,也适用于很多我们尚未攻克的难题。未来的精准医学,或许就是在这些细微的平衡中,找到逆转命运的支点——就像DP71L做的那样,把失控的开关,轻轻拨回正确的位置。
点击催更,成为大圆镜下一个视频选题!