对抗知识焦虑,从看懂这条开始
App 下载
餐后抽的T细胞,抗癌能力比空腹的强
白血病小鼠|匹兹堡大学|乳糜微粒|CAR-T细胞|T细胞|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
白血病小鼠|匹兹堡大学|乳糜微粒|CAR-T细胞|T细胞|肿瘤学|医学健康
想象一下:同样是你体内的T细胞,早上空腹抽的和吃完午饭6小时后抽的,抗癌能力居然天差地别。匹兹堡大学的研究团队在《Nature》上证实了这个反直觉的发现——餐后提取的T细胞,不仅代谢能力更强,连做成CAR-T细胞后,都能让白血病小鼠的生存期显著延长,肿瘤复发率大幅降低。这不是长期饮食调整的结果,仅仅是一顿饭带来的改变。为什么一顿饭能给免疫细胞带来这么持久的buff?背后的关键信使,是我们从未重视过的乳糜微粒。
你可以把乳糜微粒想象成餐后肠道派出的「营养快递卡车」——它们满载着肠道吸收的甘油三酯,顺着淋巴管进入血液,给全身细胞运送能量。但这次研究发现,T细胞也是这些快递的「签收方」。
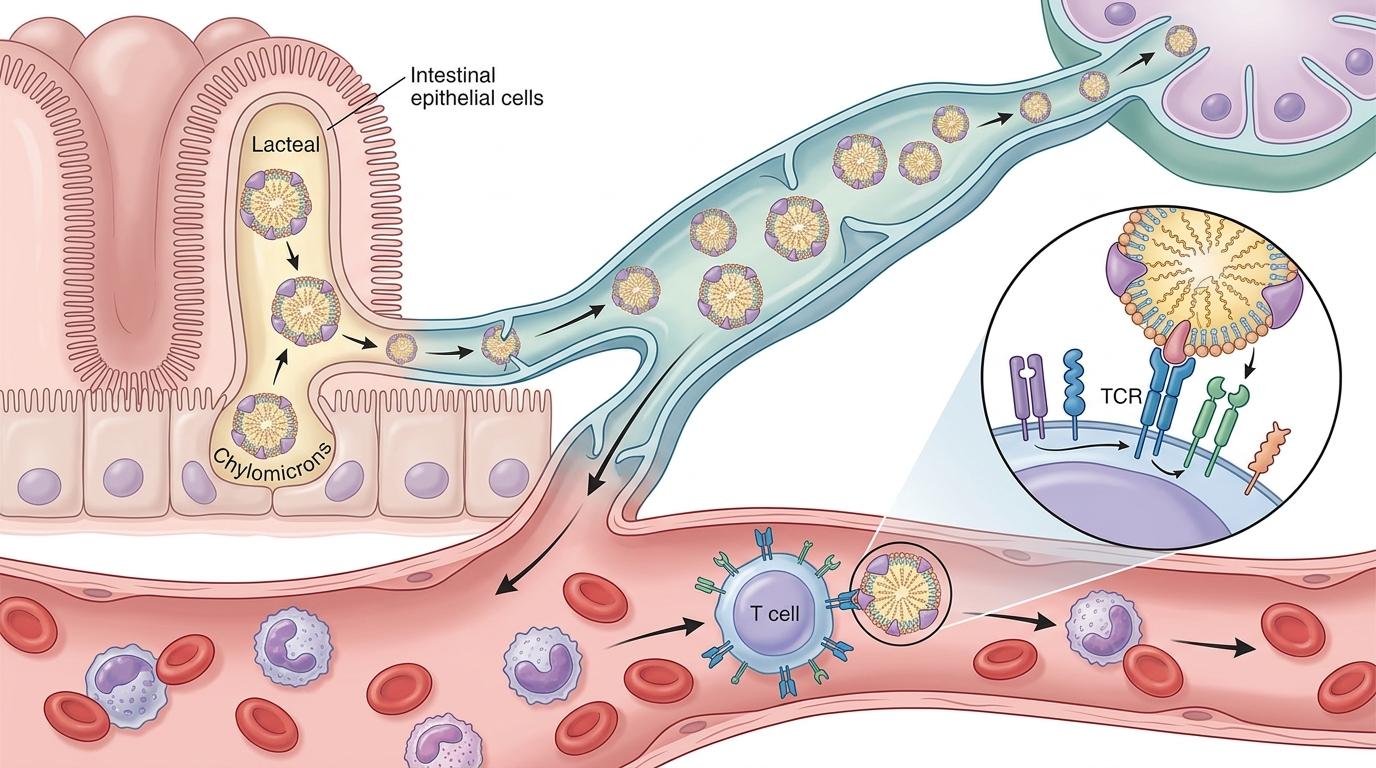
T细胞表面有一种叫低密度脂蛋白受体(LDLR)的「收货地址」,能精准抓住乳糜微粒。当这些脂质被T细胞摄取后,细胞内的能量感受器mTORC1会被立刻激活——这个蛋白复合体就像细胞的「动力调度中心」,它会下令加速蛋白质翻译,让T细胞提前合成大量免疫反应所需的「战备物资」。
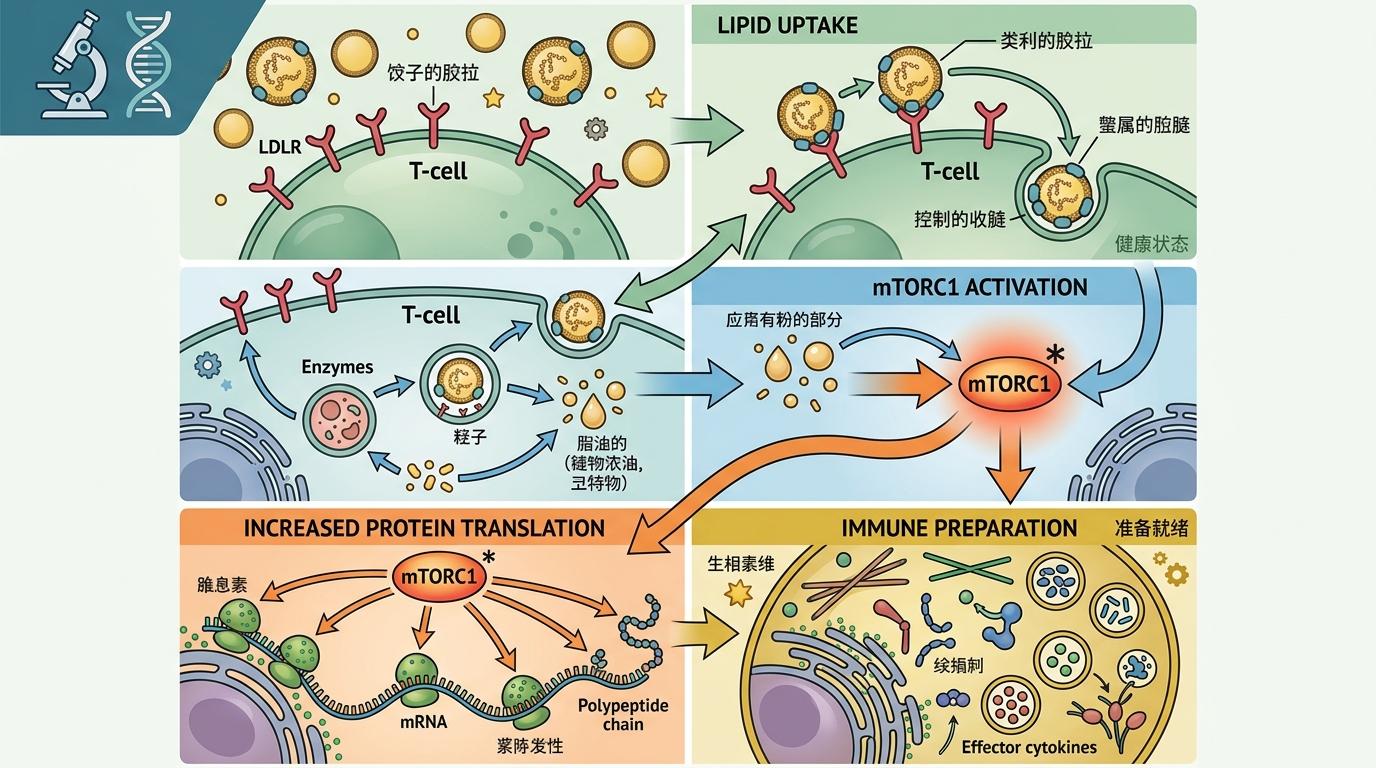
不是临时抱佛脚的应急反应,而是真正的「提前预热」:当T细胞后续遇到病毒或癌细胞时,不需要从零开始合成蛋白,能在几小时内快速启动杀伤程序,分泌更多干扰素-γ和肿瘤坏死因子。更关键的是,这种代谢增强的状态能遗传给T细胞的后代,就算体外扩增7天,甚至在体内形成记忆T细胞后,优势依然存在。
研究团队做了一组直接的对比实验:从同一个健康人体内,分别在空腹和餐后6小时抽取T细胞,再用它们构建靶向CD19的CAR-T细胞。结果一目了然——
餐后T细胞做成的CAR-T,线粒体ATP生成率比空腹组高30%,对CD19阳性肿瘤细胞的杀伤效率提升了40%。在白血病小鼠模型中,两组CAR-T初期都能控制肿瘤,但空腹组小鼠在20天后开始出现肿瘤复发,而餐后组的小鼠,有60%在观察期内保持无瘤状态,生存期比空腹组长了一倍多。
这不是个例。在小鼠病毒感染模型中,餐后T细胞的扩增数量是空腹组的2.5倍,而且在感染45天后的记忆阶段,依然能保持数量优势,甚至能持续40周以上。这种持久性恰恰是CAR-T治疗最需要的——很多时候,CAR-T细胞的快速耗竭就是治疗失败的核心原因。
当然,这项研究也有局限:目前只验证了针对白血病的CD19 CAR-T,对实体瘤的效果还不明确;而且不同饮食结构(比如高脂餐和低脂餐)对乳糜微粒的组成影响不同,是否会进一步影响T细胞功能,还需要更多研究。
过去我们总觉得,营养对免疫的影响是长期的——比如生酮饮食、素食,需要坚持几周甚至几个月才能看到效果。但这次研究彻底打破了这个认知:一顿饭的影响,能持续几个月甚至更久。
这也给了我们很多现实的启示:比如未来医院采集T细胞做CAR-T时,可能会提前让患者吃一顿标准餐,而不是要求空腹;疫苗接种或许也能和饮食结合——在接种前适当进食,让T细胞处于更活跃的状态,可能会诱导出更多记忆T细胞,提升疫苗的保护时效。
甚至连常规的免疫功能检测,都可能需要重新标准化:现在我们抽血查免疫指标时,很少考虑空腹还是餐后,但研究显示,餐后T细胞的葡萄糖摄取能力比空腹组高2.3倍,直接用这个结果来判断免疫功能,显然会有偏差。
我们总把免疫系统想象成一个独立的作战系统,却忘了它和消化系统的联系比我们想象的更紧密——肠道吸收的每一份营养,都可能成为免疫细胞的「弹药」。
「一顿饭,就是一次免疫动员。」这个发现不仅让我们重新理解了营养的价值,也给免疫治疗打开了一扇新的大门:有时候,最有效的治疗优化方案,不是复杂的基因编辑,而是调整一顿饭的时间。未来的精准医疗,或许会从餐桌上的细节开始。