对抗知识焦虑,从看懂这条开始
App 下载
治心衰的老药,能拦住心脏瓣膜钙化
救命通路|间质细胞|四川大学|心衰老药|主动脉瓣钙化|心脑血管疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
救命通路|间质细胞|四川大学|心衰老药|主动脉瓣钙化|心脑血管疾病|医学健康
75岁以上老人里,每10个就有1个藏着一颗正在变硬的心脏——主动脉瓣钙化,这个听起来陌生的毛病,是导致心衰、猝死的隐形杀手。一旦瓣膜硬到打不开,就只能开胸换瓣,可手术的并发症风险,有时比疾病本身更可怕。过去医生能做的只有等,等病情恶化到必须手术的那天。直到四川大学的团队在钙化的瓣膜里,发现了一条被「关死」的救命通路——而激活它的钥匙,居然是一款已经上市的心衰老药。为什么这条通路会失效?老药又怎么能治新病?
你可以把主动脉瓣想象成心脏的「大门」,每次心跳都要精准开合,保证血液单向流动。而瓣膜里的间质细胞,就是守护这扇门的「维修工」——平时安安静静,一旦出了问题就会立刻行动。但在钙化的瓣膜里,这些维修工集体「叛变」了:它们放弃修复本职,转而疯狂生成类似骨头的钙化组织,把柔软的瓣膜硬变成石头。
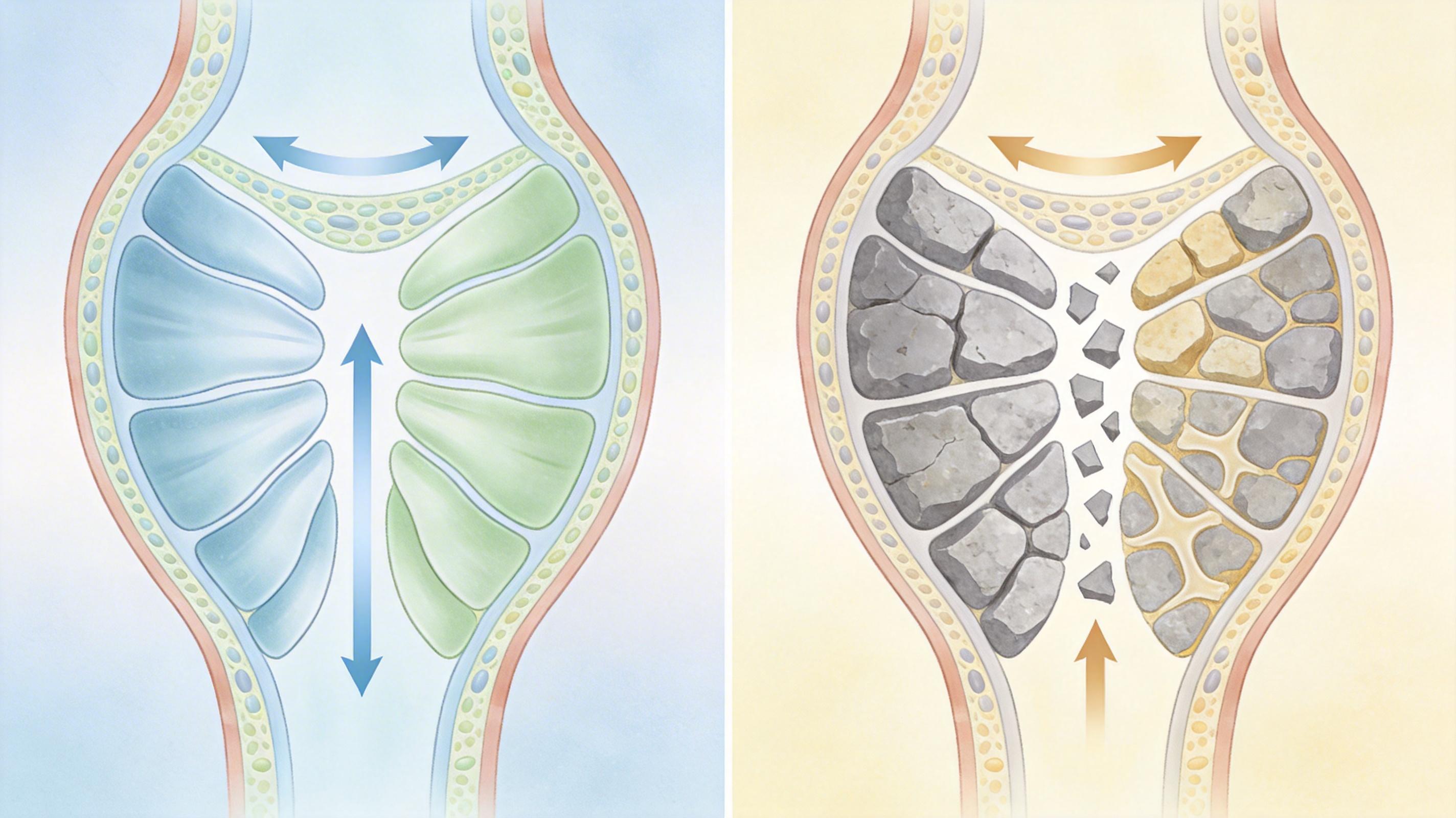
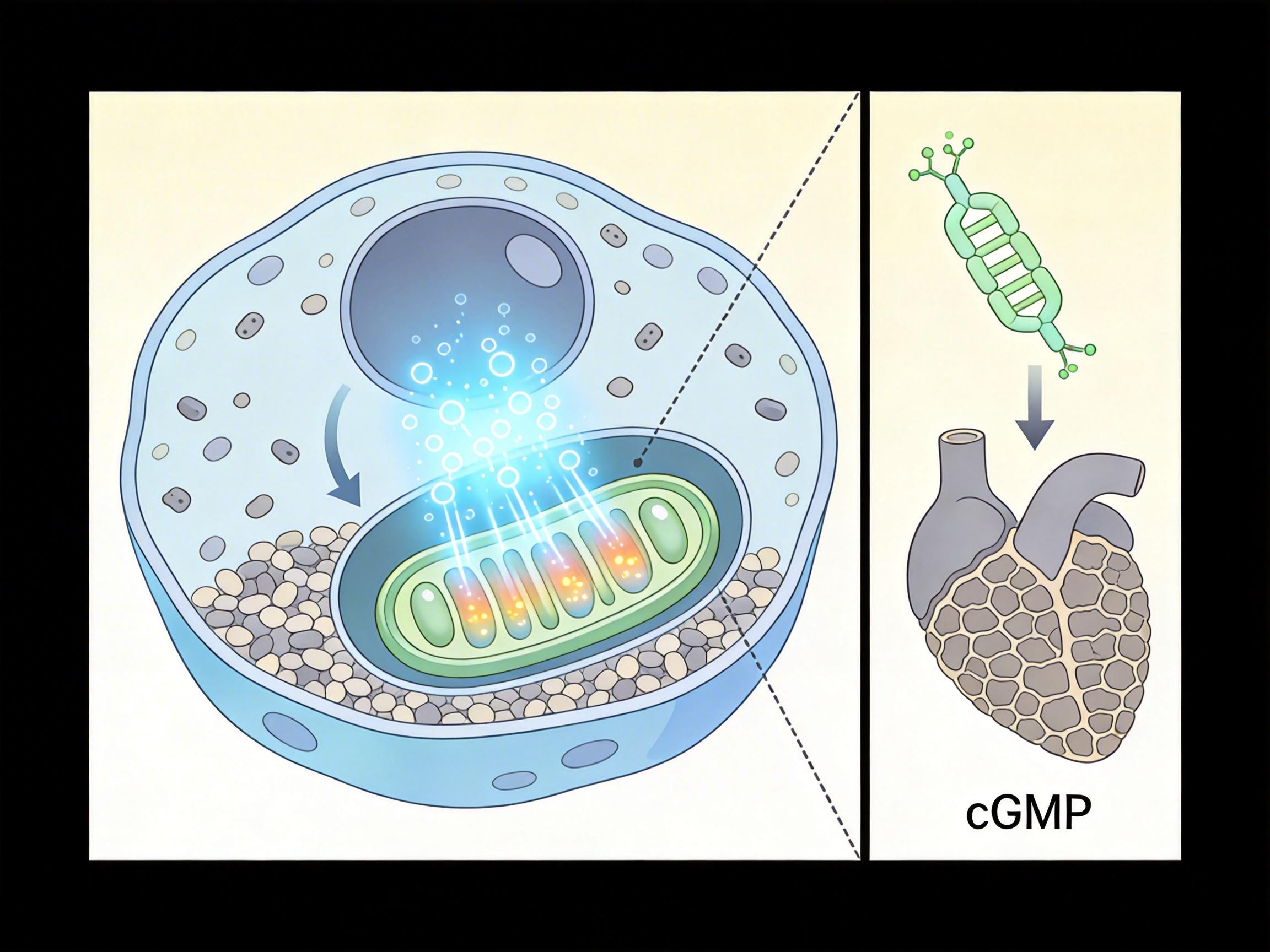
四川大学的团队在对比健康和钙化的瓣膜组织时发现,叛变的根源,是一条叫cGMP-PKG的信号通路被抑制了。你可以把这条通路理解成细胞里的「清道夫开关」——平时它会指挥细胞启动自噬,把受损的线粒体、错误折叠的蛋白这些「垃圾」清出去,维持瓣膜的正常功能。
当这个开关失灵,细胞里的垃圾越堆越多,线粒体开始疯狂产生活性氧,就像厨房着火却没人救火,最终把维修工逼成了「破坏者」。更关键的是,患者血液里的cGMP水平越低,瓣膜钙化就越严重,两者像跷跷板一样精准对应。
既然找到了被关死的开关,接下来的问题就是:怎么把它重新拧开?
团队测试了三种能激活cGMP-PKG通路的物质:BNP(一种人体自身分泌的肽类)、西地那非(治疗勃起功能障碍的药物),还有vericiguat——这款2021年就上市的心衰药。结果让所有人意外:vericiguat的效果远远超过另外两者,它不仅能在实验室里阻止瓣膜细胞钙化,还能在小鼠模型里让已经变硬的瓣膜重新柔软起来。
它的原理说起来其实很简单:vericiguat是一种可溶性鸟苷酸环化酶刺激剂,能直接绕过通路里被氧化损伤的环节,强制提升细胞内的cGMP水平,激活PKG蛋白。而被激活的PKG会精准找到自噬的「启动键」——ULK1蛋白,在它的第556位丝氨酸上打一个磷酸化的标记,就像给清道夫下达了开工指令。
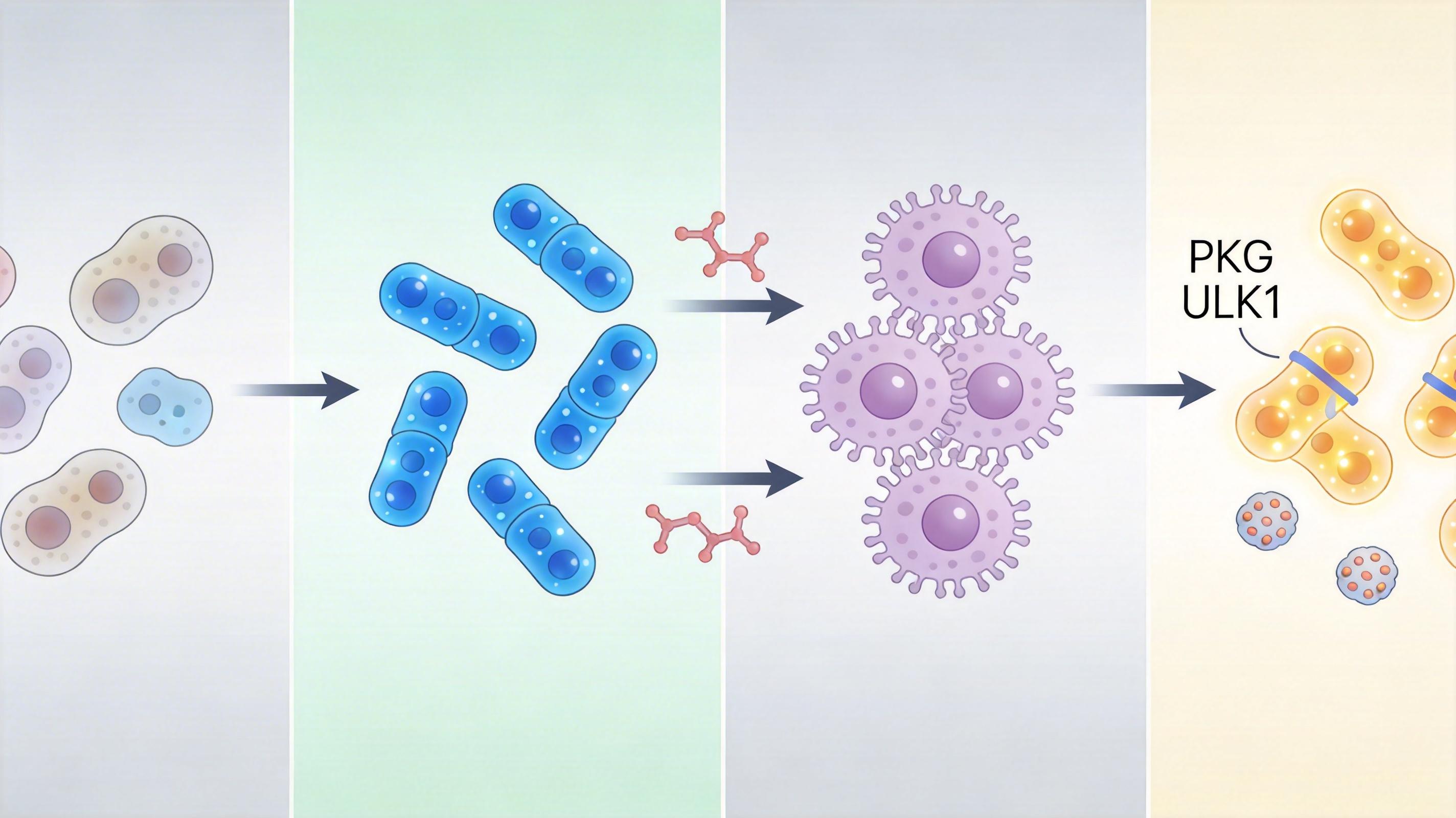
清道夫一开工,受损的线粒体被及时清理,活性氧的产量降下来,叛变的瓣膜间质细胞又变回了维修工。团队做了一个反向验证:如果用药物阻断自噬,哪怕再激活cGMP-PKG通路,瓣膜钙化也会照常发生——这说明自噬就是这条通路发挥作用的核心环节。
我认为,这项研究最有价值的地方,不是发现了一条新通路,而是给了那些「等手术」的患者一个新选择。
过去我们总觉得,瓣膜钙化是不可逆转的退行性病变,就像人老了头发会白,只能等硬到必须换的时候再动手。但这项研究证明,只要在早期精准激活cGMP-PKG通路,就能把病变拦在手术前。而vericiguat作为已经上市的药物,跳过了漫长的临床试验周期,很快就能用到患者身上——这比任何全新靶点的药物都更有现实意义。
当然,它也不是万能的。目前的研究只验证了它在轻中度钙化患者中的效果,对于已经完全硬死的瓣膜,它也无能为力。而且vericiguat可能会导致轻微低血压,需要医生根据患者情况调整剂量。但不可否认的是,它给了我们一个全新的思路:与其等心脏的大门彻底焊死,不如在它刚开始生锈的时候,就给它上点润滑油。
从实验室的细胞培养皿,到临床患者的心脏,这条被遗忘的通路,终于重新回到了我们的视野里。我们总在追求「突破性」的新药,却常常忽略,那些已经在患者身上用了好几年的老药,可能藏着解决新问题的钥匙。
「早干预,胜晚修补」,这不仅是对心脏瓣膜病的启示,也是对所有慢性疾病的提醒。未来的医学,或许不再是等疾病爆发后再猛药强攻,而是在它刚开始萌芽时,就用精准的信号调控,把它拉回正常轨道。毕竟,对于心脏来说,能不换门,就尽量别换。