对抗知识焦虑,从看懂这条开始
App 下载
亲兄弟的基因突变,让他摆脱了HIV和血癌
奥斯陆大学医院|骨髓增生异常综合征|HIV长期缓解|CCR5基因突变|干细胞移植|感染性疾病|基因组学|生命科学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
奥斯陆大学医院|骨髓增生异常综合征|HIV长期缓解|CCR5基因突变|干细胞移植|感染性疾病|基因组学|生命科学|医学健康
2026年春,奥斯陆大学医院的病房里,63岁的挪威老人看着手里的检测报告——血液、骨髓、肠道里,连半滴有复制能力的HIV病毒都找不到。他已经4年没吃抗逆转录病毒药了。
2006年确诊HIV,2017年又查出骨髓增生异常综合征,两次被判“重症”的他,2020年接受了亲兄弟的干细胞移植。没人料到,这份来自家人的“生命礼物”,不仅治好他的血癌,还让他成了全球第10位实现HIV长期缓解的人。
这不是奇迹,而是藏在基因里的“门锁”被找对了——为什么亲兄弟的干细胞能同时击退两种绝症?
你可以把HIV入侵细胞的过程想象成小偷开门:先撬掉CD4“大门”,再用CCR5“门把手”拧开最后一道锁——绝大多数HIV毒株都靠这套流程钻进免疫细胞。
但有些人的CCR5基因天生缺了32个碱基对,也就是**CCR5Δ32突变**——相当于把门把手直接拆了。携带两份这种突变的人(纯合子),对90%以上的HIV毒株天然免疫,北欧人群里每100个人里才有1个这样的“天选者”。
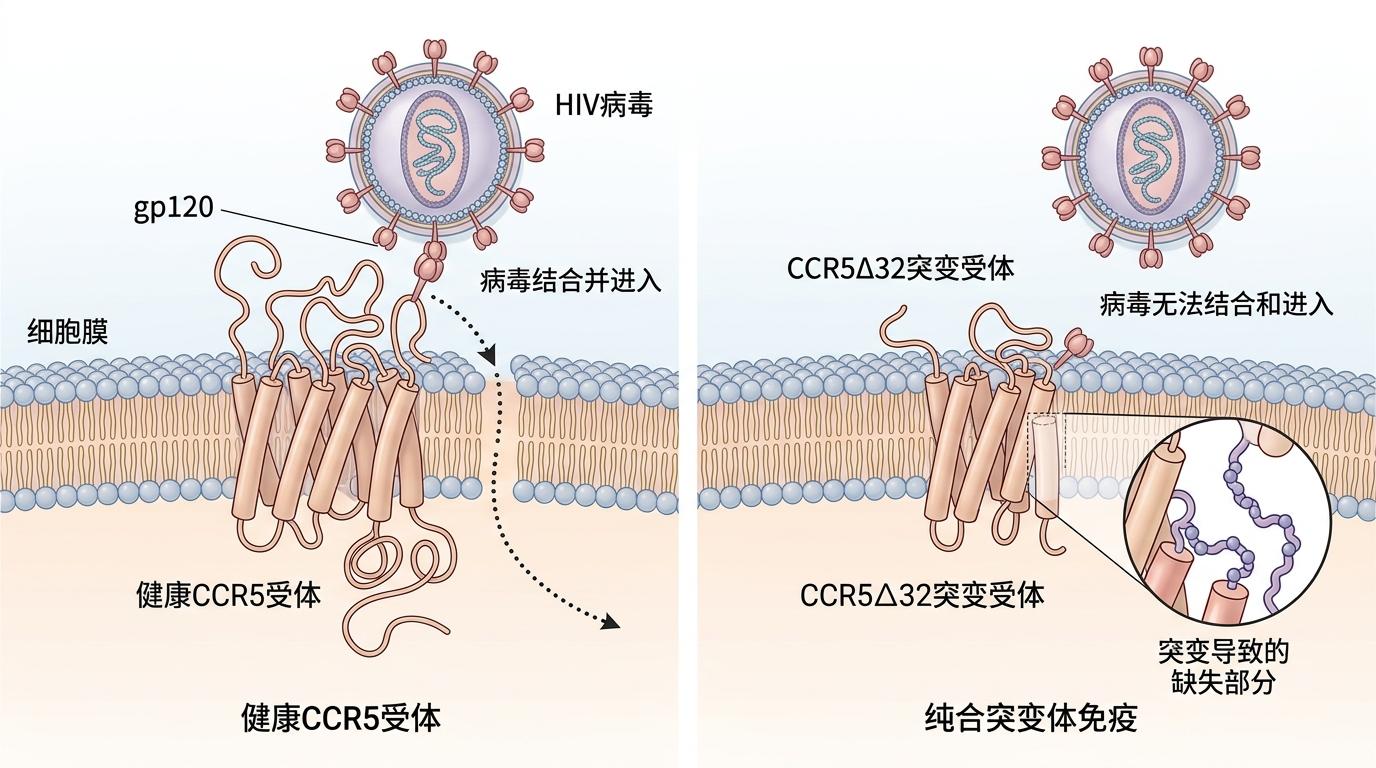
奥斯陆病人的亲兄弟,恰好就是这1%。移植后,老人的免疫系统被完全替换:新的CD4+T细胞表面没有CCR5“门把手”,HIV就算撬开了大门,也找不到地方拧锁。
但真实的机制比这更精确:
这不是单一环节的胜利,而是一套“清空-替换-清扫”的组合拳。
更值得关注的是,奥斯陆病人的案例,其实暴露了当前HIV治愈路径的两大局限。
首先是“幸存者偏差”。全球目前的10例HIV长期缓解病例,全都是同时患有血液癌症的患者——只有为了治癌症,才会冒风险做干细胞移植。这种治疗的1年内死亡率高达10%-20%,不可能给普通HIV感染者用。而能找到CCR5Δ32纯合子供者的概率,更是低到像中两次彩票:先得有血缘亲属,亲属还得恰好是那1%的“天选者”。
其次是病毒的“逃逸漏洞”。CCR5Δ32突变只对依赖CCR5的HIV毒株有效,约10%-20%的患者体内存在依赖CXCR4受体的毒株——相当于小偷换了另一把钥匙。德国曾有一位患者,移植后原本占比极低的CXCR4毒株迅速扩增,最终导致病毒反弹去世。
就连奥斯陆病人的治愈,也藏着运气成分:他体内的HIV毒株全是依赖CCR5的,没有留下“逃逸”的口子。
现在的问题是,如何把这种“小众治愈”变成更多人能用的方案?答案指向基因编辑——给患者自己的细胞“装”上CCR5Δ32突变的“防火墙”。
目前最成熟的是CRISPR/Cas9技术:从患者体内取出造血干细胞,用CRISPR敲除CCR5基因,再输回患者体内。2019年中国的临床试验显示,经过编辑的干细胞能在患者体内存活19个月,且没有明显副作用;美国的试验也证明,编辑后的细胞能有效降低病毒载量。
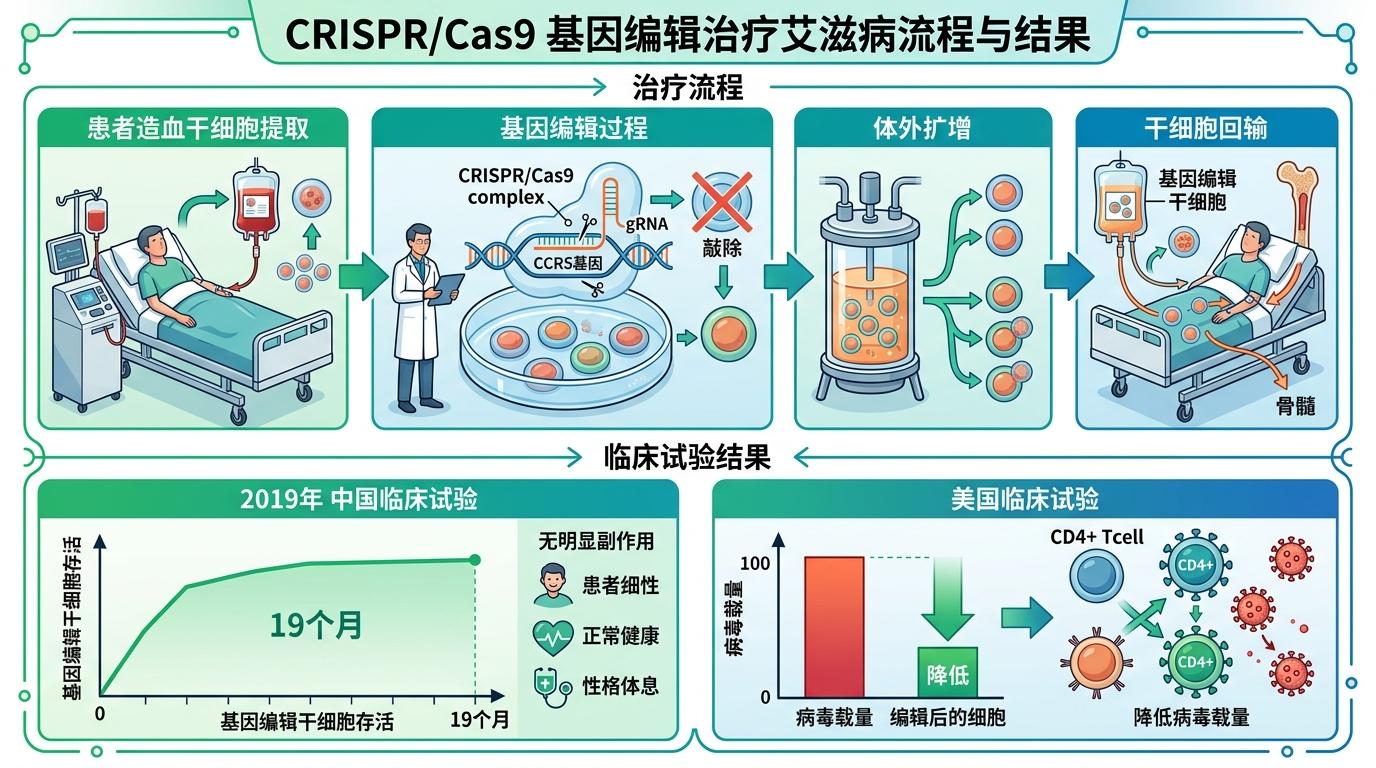
但这还不够。单一敲除CCR5仍可能被CXCR4毒株逃逸,科学家正在尝试多靶点编辑:同时敲除CCR5和CXCR4,或者直接编辑HIV的基因组片段。更关键的是递送难题——如何让基因编辑工具精准到达所有潜伏病毒的细胞,比如肠道、淋巴结里的静息T细胞,目前还没有完美的解决方案。
另一条路径是免疫疗法:用CAR-T细胞精准追杀藏着HIV的潜伏细胞,或者用广谱中和抗体封锁病毒的入侵路线。这些疗法不需要移植,风险更低,正在小规模临床试验中验证效果。
奥斯陆病人的故事,不是“HIV被攻克”的宣告,而是给科研者递了一张更清晰的“地图”——我们终于确认,只要切断病毒的入侵路径,再配合免疫系统的清扫,HIV是可以被“功能性治愈”的。
治愈的本质,是让免疫系统重新掌握主动权。未来的HIV治疗,不会是少数人的“幸运彩票”,而是像现在的抗病毒药一样,成为每个患者都能触及的选项——也许是一针基因编辑的干细胞,也许是几次免疫疗法的注射,让人们不用再终身服药,不用再活在病毒反弹的恐惧里。
就像奥斯陆病人现在做的那样:每天出门散步,和朋友喝咖啡,像没感染过HIV一样生活。这不是奇迹,是科学一步步铺出来的路。