
1 个月前

1 个月前
对于全球数百万在器官移植名单上焦急等待的患者而言,时间是最残忍的敌人。每一天,都有生命因等不到合适的供体而遗憾凋零。据统计,中国的器官移植供需比高达1:15,巨大的缺口让无数家庭陷入绝望。长期以来,科学家们尝试用异种移植、传统组织工程等方法填补这一鸿沟,但免疫排斥的“高墙”与制造技术的“瓶颈”始终难以逾越。我们能否像建造房屋一样,用标准化的“积木”精准地“搭建”出一个功能完善的人工器官?
近日,一项发表于《Mater Today Bio》的研究为这个梦想照亮了现实。研究团队通过创新的3D生物打印技术,成功制造出可精准组装的“器官积木”,并用其构建了带有复杂血管网络的大体积肝组织。这一里程碑式的突破,标志着人工器官制造正从“手工作坊”时代迈向“精密智造”时代,离临床应用又近了一大步。
在“器官积木”诞生之前,组织工程学界长期在两条技术路线上挣扎,仿佛一场看不到尽头的“两线作战”。
自上而下:科学家先用生物材料构建一个器官形状的支架,再像播种一样将细胞接种上去。这种方法虽然能形成宏观结构,但过程粗放,无法精准控制细胞在三维空间中的位置,仅适用于皮肤、骨骼等结构简单的组织。对于肝脏、心脏这类内部拥有精细微观结构(如肝小叶、毛细血管网)的复杂器官,则束手无策。
自下而上:科学家先培养出细胞球或类器官,再试图将它们“堆叠”起来。这种方法能获得高细胞密度的组织,但细胞的自发组装过程充满随机性,导致成品尺寸不一、功能不稳,可重复性极差,如同用一堆形状各异的石头砌墙,难以实现工业化和临床转化。
传统的挤出式3D生物打印虽然提升了可重复性,但其打印精度不足,始终是制造功能性人工器官的“阿喀琉斯之踵”。
面对行业痛点,研究团队提出了一种颠覆性的解决方案:模具引导的3D生物打印策略。这套策略如同一条高度自动化的“乐高积木”生产线,将器官制造的精度和效率提升到了前所未有的高度。
第一步:精密“开模” 研究人员首先用生物相容性材料聚己内酯(PCL)3D打印出精密的模具。这个模具就像乐高积木的模具,为后续的“器官积木”设定了精确的尺寸和内部结构。借助模具的几何约束,最终成型的器官积木尺寸误差被控制在惊人的160微米以内,成功复刻了毛细血管束、肝小叶等天然组织的复杂微结构。
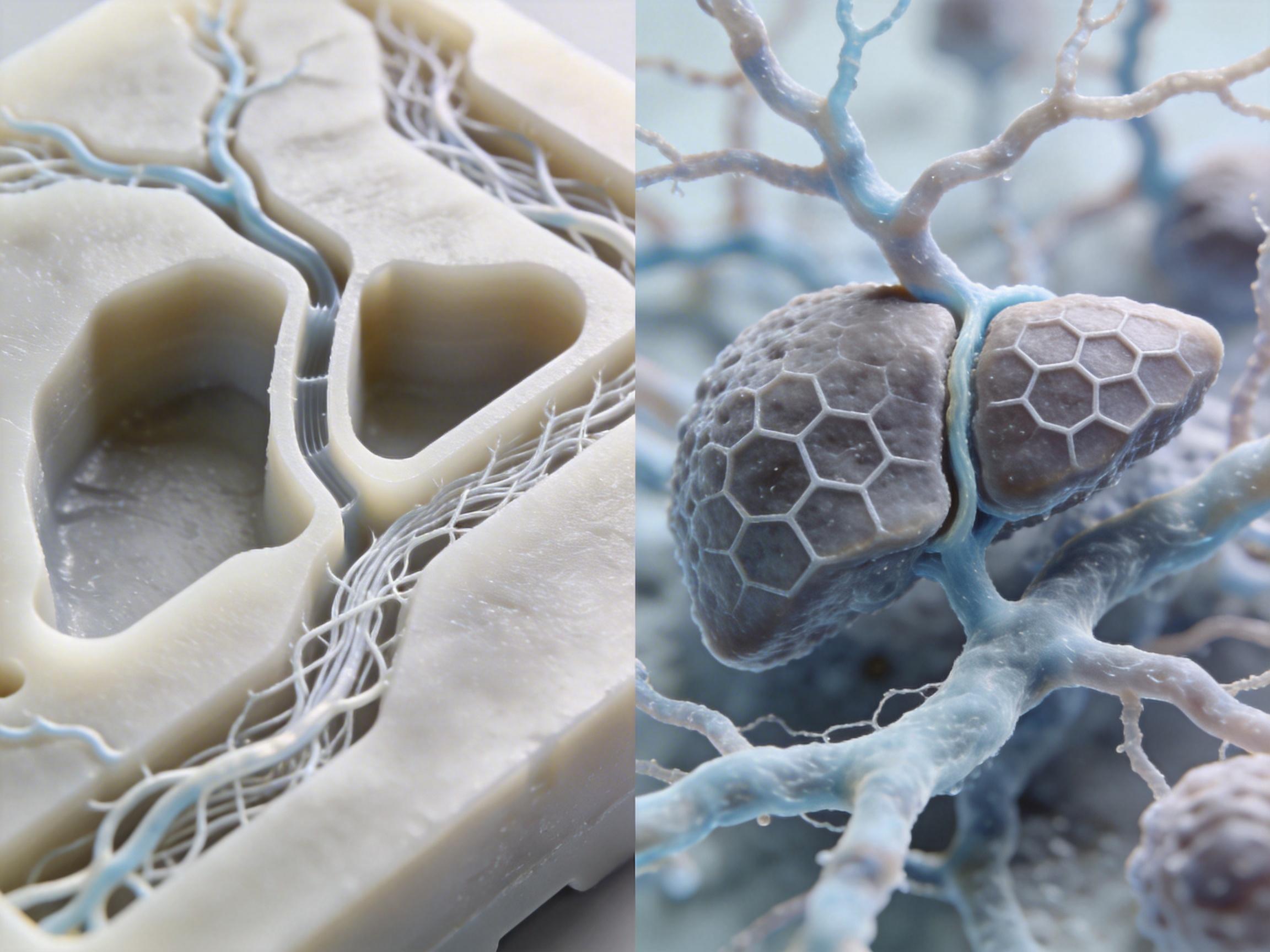
第二步:优化“原料” 胶原蛋白是理想的生物墨水,但其质地柔软,在打印中极易因重力和表面张力而变形。团队通过精准调控水凝胶的流变特性,并选择在特定缓冲液环境中打印,巧妙地规避了表面张力导致的结构失真,让柔软的胶原蛋白也能实现高精度成型。
第三步:强化“积木” 单个积木的机械强度同样至关重要。研究团队选用低毒性的天然交联剂——京尼平(Genipin)对积木进行“固化”处理。经过1小时的交联,积木的压缩强度实现了跨越式增长,足以抵抗细胞活动引发的结构收缩。更关键的是,这一强化过程并未损害细胞的活性与核心生物学功能,实现了力学性能与生物活性的完美兼容。
有了标准化、高强度的“器官积木”,下一步就是组装。研究团队选用纤维蛋白作为“生物胶水”,将积木无缝拼接起来。奇迹在此时发生:组装不仅是物理上的拼接,更是生物学上的融合。
积木间的成纤维细胞开始分泌血管内皮生长因子(VEGF),这种信号分子像“指挥官”一样,引导血管内皮细胞跨越积木边界,相互连接,最终形成一个连续、贯通的血管网络。这解决了大体积人工组织长期以来因营养和氧气供应不足而导致内部细胞死亡的核心难题。
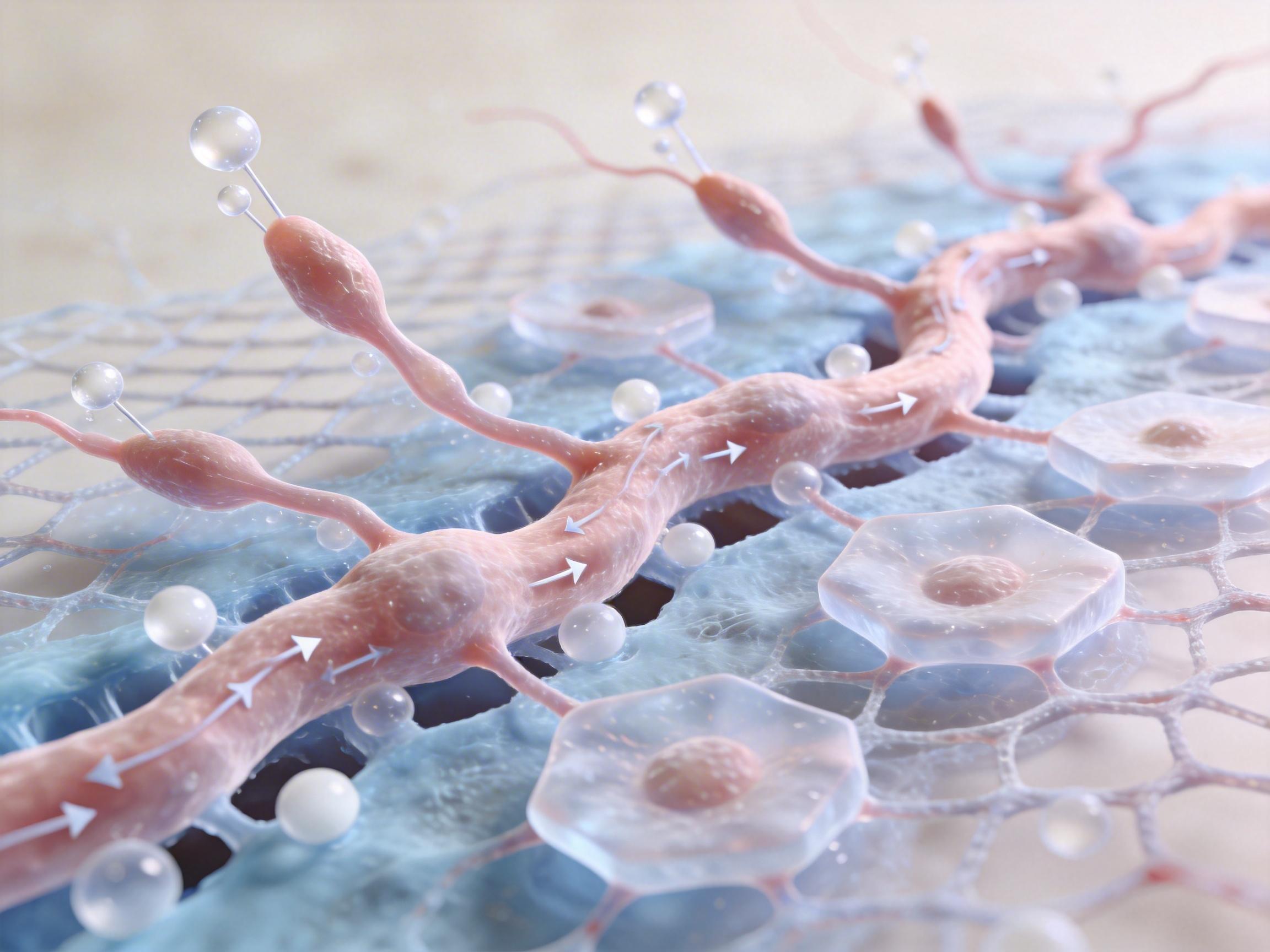
利用这一技术,团队成功用4个预设了血管通道的肝脏积木,组装成一个带有直径1毫米中心血管腔和16个外周微血管通道的大体积肝组织。这个人工血管网络不仅结构完整,还具备了生理屏障功能,能像天然血管一样精准控制物质运输,标志着人工器官的功能化复刻取得了重大突破。
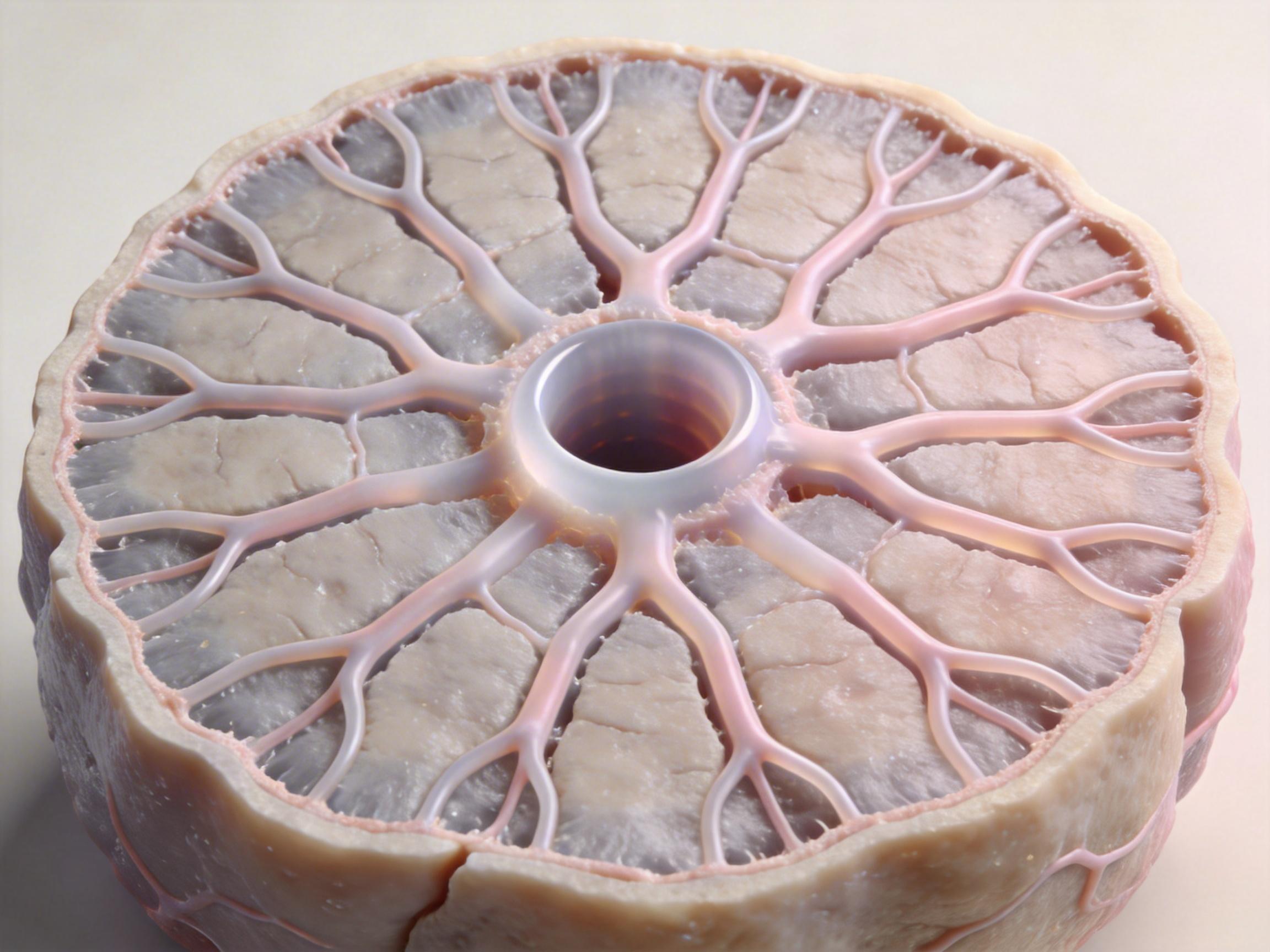
这项研究的核心价值在于,它巧妙地融合了精密制造与自下而上组装策略的优点,一举攻克了行业内尺寸精度低和可重复性差两大难题,为人工器官的标准化、规模化生产铺平了道路。
当然,从实验室走向临床,依然有很长的路要走。如何进一步优化生物墨水,如何整合免疫系统以避免排斥反应(例如结合CAR-Treg细胞疗法或免疫保护涂层技术),以及如何应对复杂的伦理与监管挑战,都是未来需要攻克的关卡。
但无论如何,这项“器官积木”技术已经打开了一扇通往未来的大门。它不仅为肝、心等复杂器官的再造提供了全新的工程化蓝图,也让全球数百万等待器官移植的患者看到了新的曙光。曾经遥不可及的“器官再生”梦想,正在这一块块微小的“生命积木”中,被前所未有地清晰地构建出来。
点击充电,成为大圆镜下一个视频选题!