
22 天前

22 天前
你可能没意识到,每10头新生仔猪里就有1到3头天生瘦小,它们活下来的概率更低,长肉的速度更慢——每年光是中国,就有3500万头这样的仔猪,直接牵动着十几亿人的肉盘子和钱包。而在人类世界里,每100个新生儿中就有6个遭遇胎儿生长受限,每5个妊娠女性中就有1个被心脏负担加重困扰。这些看似不相干的难题,最近被一头猪和它的妈妈彻底串了起来。北京时间2026年3月27日,江西农业大学的团队在《科学》杂志发表了全球首个覆盖哺乳动物同一个体全身所有组织的单细胞转录组图谱,而这头猪和它的妈妈,就是图谱的唯一主角。
你可以把单细胞转录组图谱想象成一份超精细的“人体细胞通讯录”——它能精准定位到你身体里每一种细胞的位置,还能说出这个细胞正在“干的活”和“用的工具”。这次的研究团队,愣是把一头胎猪的115个组织、它妈妈的119个组织全部分解成单个细胞,总共分析了超过250万个细胞,最终画出了这份包含890种细胞类型的通讯录。
正是这份通讯录,揪出了导致胎儿生长受限的“小偷”——胎儿尿囊绒毛膜滋养层细胞。这是一种紧贴胎盘的细胞,它的本职工作是把妈妈血液里的营养“搬”给胎儿。但研究发现,当这种细胞里负责转运亮氨酸(一种促进肌肉生长的必需氨基酸)的蛋白质“罢工”时,胎儿就会因为缺营养而长不大。
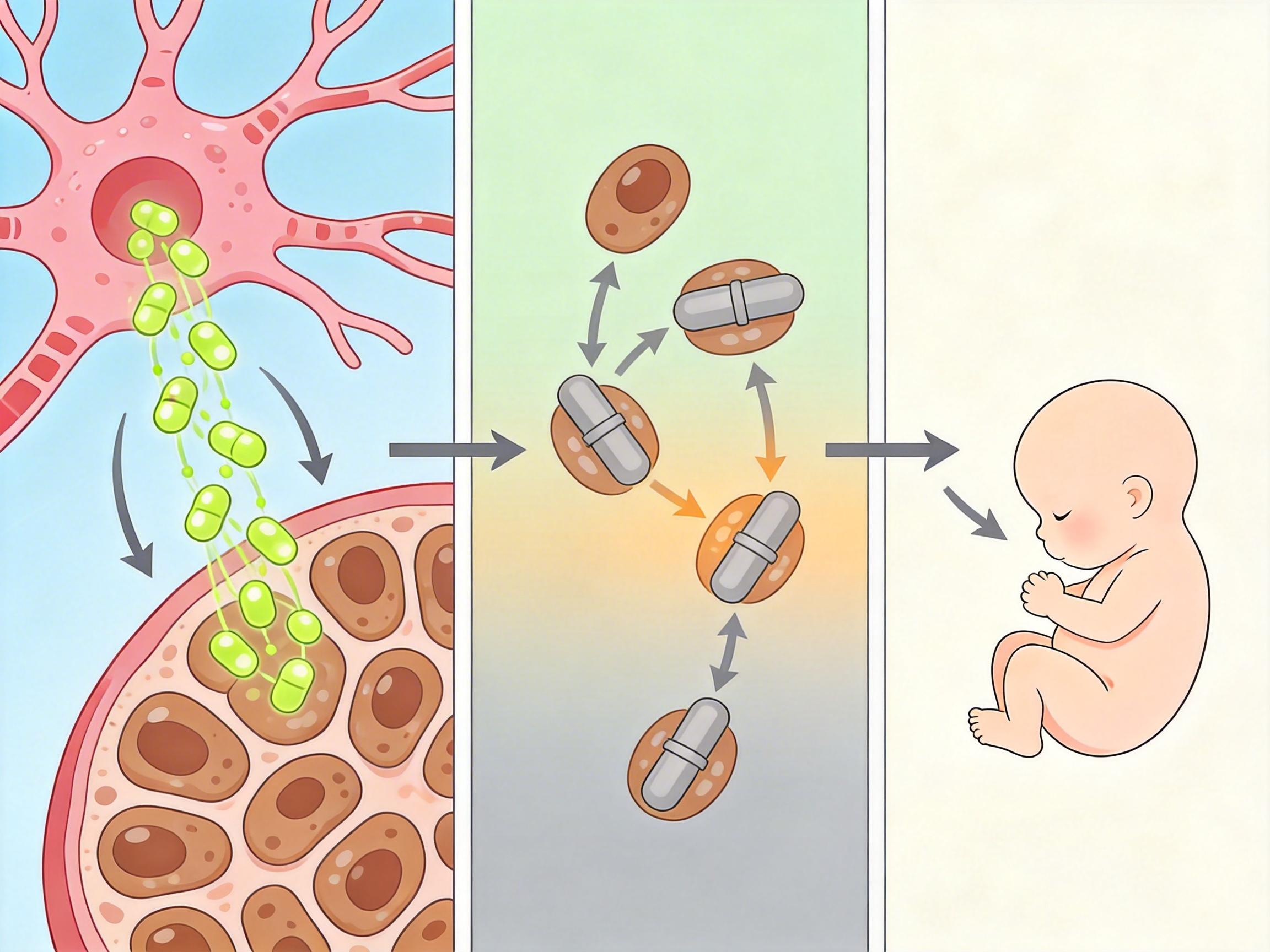
亮氨酸就像给胎儿肌肉发育供能的“充电宝”,一旦转运不足,胎儿的II型肌纤维就没法正常生长,最终导致出生体重偏低。更关键的是,团队通过实验证实,给孕期母体补充亮氨酸,能部分逆转这种生长受限的情况。
除了胎儿的问题,研究还揭开了母体心脏的一个秘密。你可能不知道,妊娠期间女性的血容量会增加50%,心输出量要提升30%,心脏相当于一直在“加班”。但为什么大多数孕妇的心脏能扛住这种负荷,产后还能恢复原样?
答案藏在心脏里一种叫Cap2的毛细血管内皮细胞里。这种细胞就像心脏的“能量调度员”——平时心脏主要靠葡萄糖供能,但妊娠期间,Cap2细胞会主动切换“供能菜单”:它会增强脂肪酸的运输能力,同时降低葡萄糖的转运效率,让心脏从“烧糖”改成“烧脂肪”。
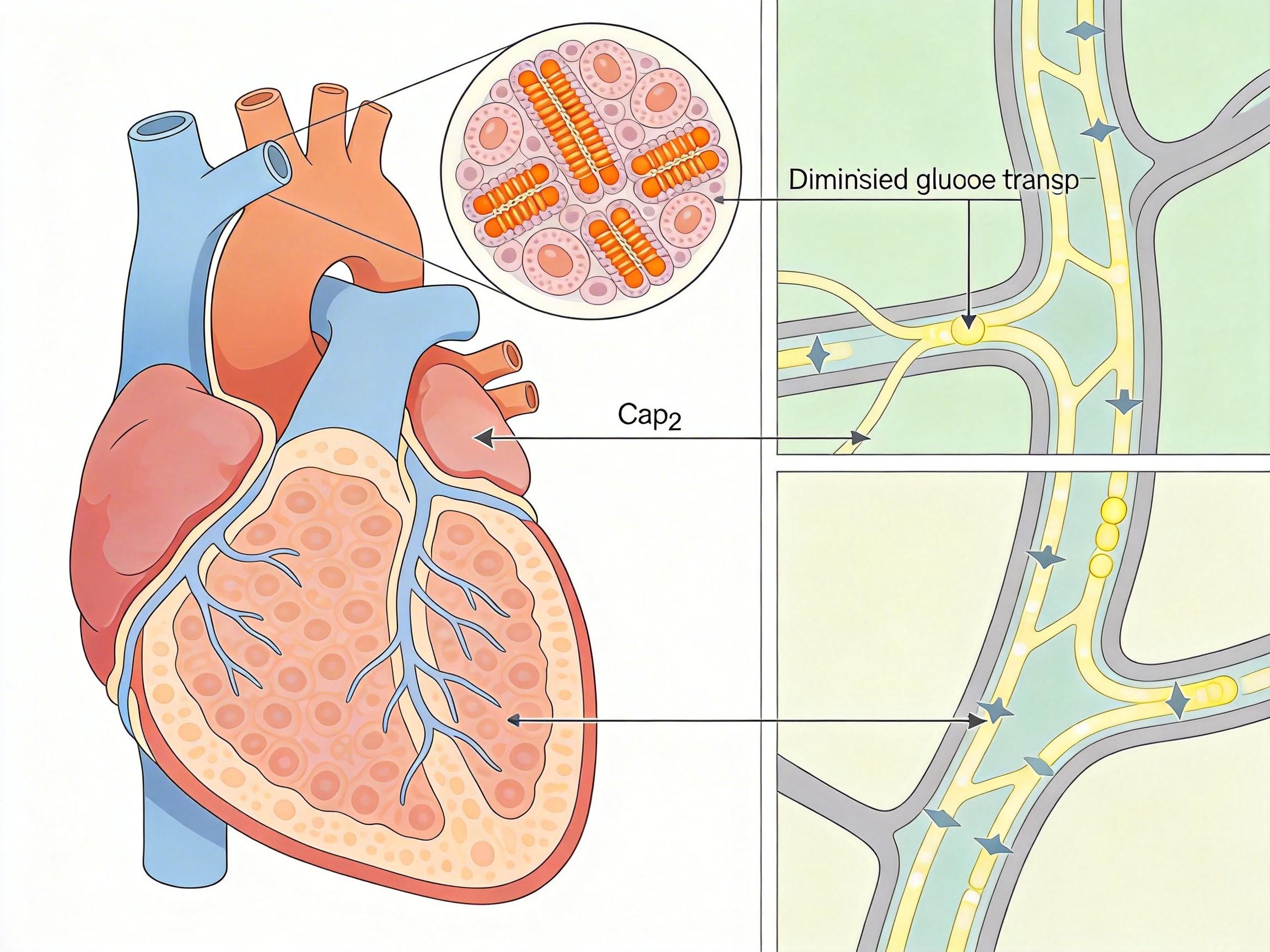
这种转变不是随便发生的。团队发现,妊娠期间Cap2细胞的数量会显著增加,专门负责给加班的心脏供应更高效的能量。等胎儿出生后,这些细胞的数量又会自动回落,让心脏回到原来的能量轨道上。这就是为什么大多数孕妇的心脏只是“生理性肥大”,而非病理性损伤——它只是暂时换了个更高效的工作模式。
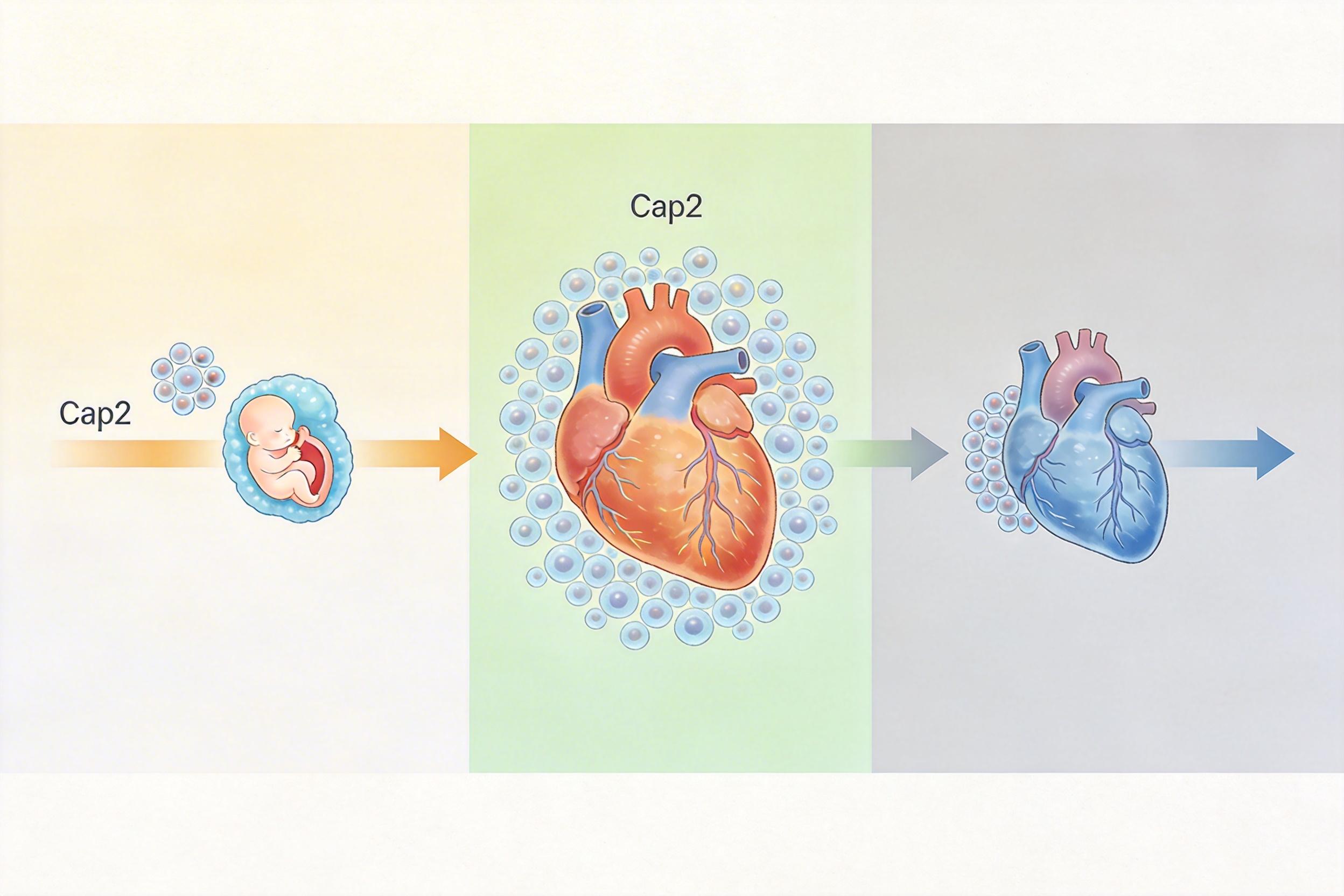
更值得关注的是,这次的研究还证实了猪作为人类疾病模型的价值——猪和人类在关键细胞类型的转录调控上高度保守,尤其是妊娠相关的细胞机制。这意味着,我们在猪身上找到的胎儿生长受限和妊娠心脏适应的机制,直接能为人类相关疾病的研究提供参考。
当然,这项研究也不是完美的。比如,目前还不清楚亮氨酸转运不足的具体触发因素是什么,是基因问题还是环境影响?Cap2细胞的能量切换是如何被精准调控的?这些问题还需要进一步研究。而且,从实验室的发现到实际应用,比如开发针对胎儿生长受限的药物,或者给孕妇提供精准的营养指导,还有很长的路要走。
不过,它的意义已经足够重大——这不仅是中国猪遗传育种领域第一篇发表在《科学》上的独立完成论文,更重要的是,它给我们打开了一扇用单细胞技术研究母胎互动的新大门。
当我们把目光聚焦在实验室里的一头猪时,其实也在关注着每一个家庭的生育健康,每一个养殖户的生计,甚至每一个人的餐桌安全。这份全球首个哺乳动物全身单细胞转录组图谱,就像一张高精度的导航图,它不仅能帮我们找到解决生猪产业难题的方向,更能为人类妊娠相关疾病的研究提供关键线索。
细胞无小事,一猪牵万家。 科学的进步,有时候就藏在这些看似不起眼的细节里——一头猪的细胞图谱,最终连接的是人类的健康与未来。
点击充电,成为大圆镜下一个视频选题!