对抗知识焦虑,从看懂这条开始
App 下载
肺纤维化的隐秘刹车:ERBB4守住上皮细胞身份
细胞身份转变|人远端肺类器官|CD66c⁺基底细胞|肺泡Ⅱ型细胞|ERBB4信号通路|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
细胞身份转变|人远端肺类器官|CD66c⁺基底细胞|肺泡Ⅱ型细胞|ERBB4信号通路|肿瘤学|医学健康
当肺部遭遇新冠、肺炎或特发性肺纤维化的重创,我们总以为肺泡细胞会乖乖修复伤口——但事实是,有些细胞会“叛变”。原本负责分泌表面活性物质的肺泡Ⅱ型细胞、守护气道的分泌细胞,会突然丢掉自己的“身份”,转变成一种叫CD66c⁺的基底细胞。这种细胞不会帮着修复肺泡,反而会分泌炎症因子、拉扯纤维组织,把好好的肺变成硬邦邦的“纤维网”。直到复旦大学的研究团队在实验室里造出了人远端肺类器官,我们才抓住了这场叛变的关键刹车——ERBB4信号通路。
你可以把肺泡上皮细胞想象成一群各司其职的车间工人:肺泡Ⅱ型细胞是“生产员”,制造维持肺泡弹性的表面活性物质;分泌细胞是“清洁工”,分泌黏液清除异物。但在严重肺损伤后,这些工人会集体“换岗”——放弃原本的技能,变成只会“搞破坏”的CD66c⁺基底细胞。
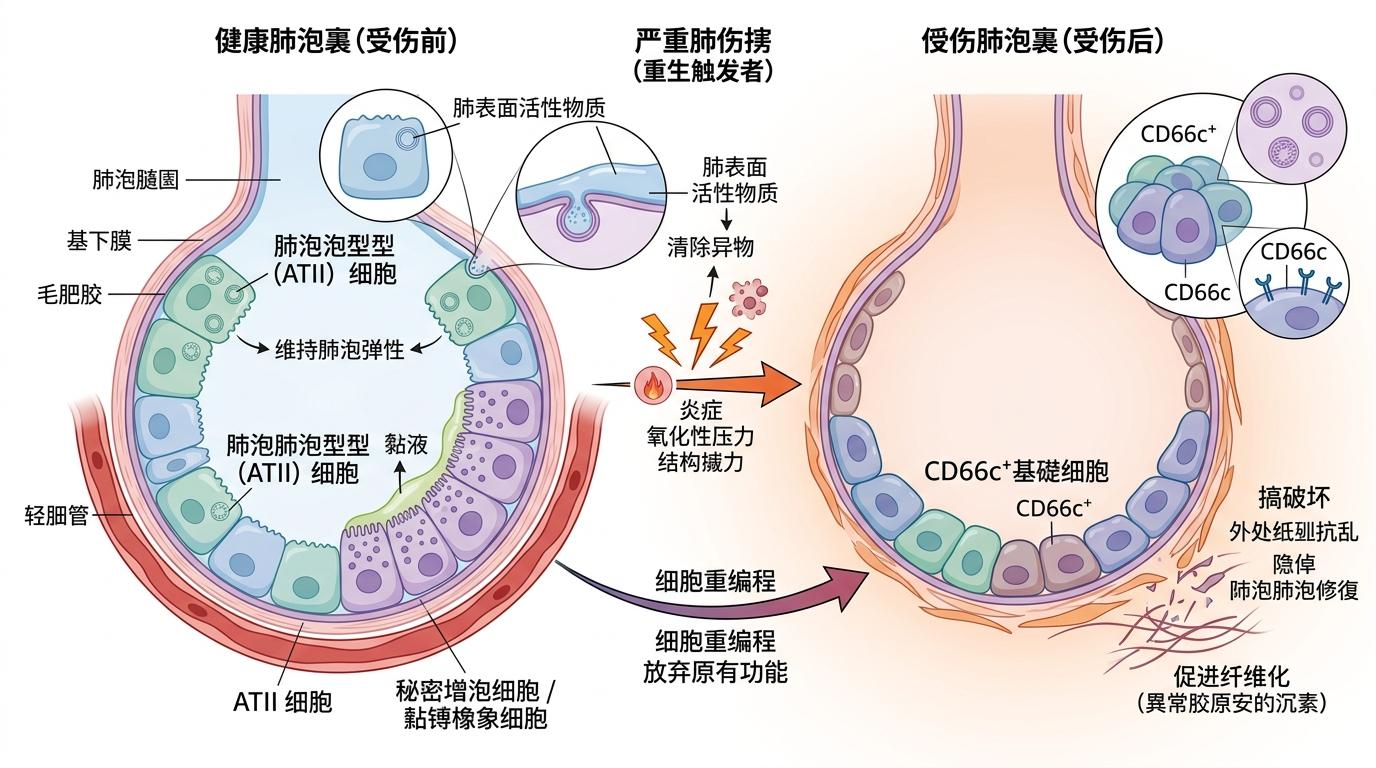
复旦团队用人类远端肺类器官还原了这场叛变:他们在类器官里找到了和特发性肺纤维化患者肺部高度相似的CD66c⁺基底细胞,这些细胞的基因里写满了“促炎”“促纤维化”的指令。更惊人的是,不止一种上皮细胞会叛变:分泌细胞、肺泡Ⅱ型细胞甚至原本的基底细胞,都能转变成这种危险亚型——这意味着肺上皮细胞的“身份”远没有我们想的固定。
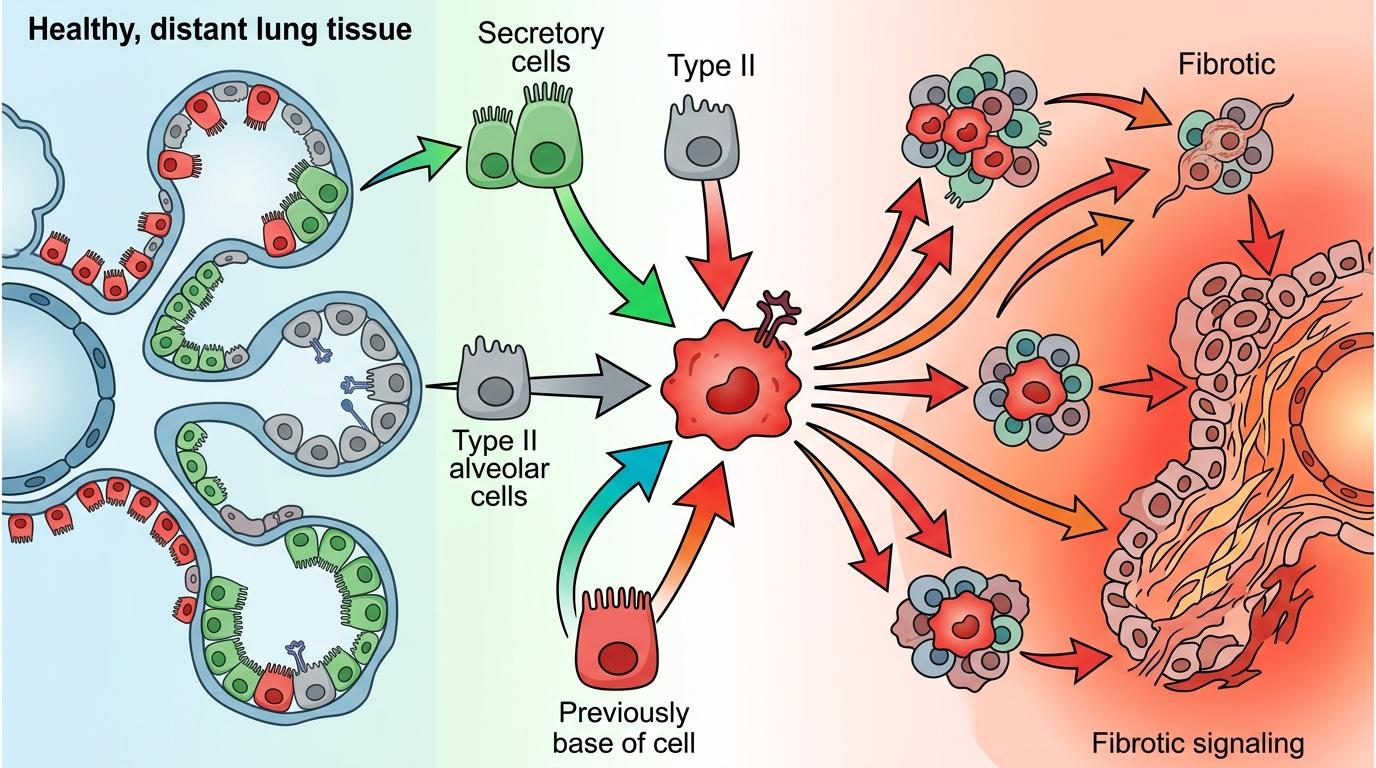
但真实的机制比这更精确:当肺损伤发生,上皮细胞的谱系稳定性被打破,原本维持身份的信号通路失效,细胞开始向病理状态转分化。
如果把上皮细胞的身份叛变比作一辆失控的车,ERBB4就是被人遗忘的刹车。
研究人员发现,用GSK3抑制剂CHIR99021处理肺类器官时,那些准备叛变的上皮细胞突然“安分”了——它们维持住了自己的分泌细胞或肺泡Ⅱ型细胞身份,不再转变成CD66c⁺基底细胞。而这一过程的核心,就是ERBB4-MAPK信号通路被激活了。
更直接的证据来自外源性NRG1:这种物质能通过ERBB4直接阻断转分化。就像给失控的车猛踩刹车,ERBB4一启动,上皮细胞就不会再丢了自己的“本职工作”。研究人员还在特发性肺纤维化患者的肺组织里找到了佐证:患者肺部的ERBB4表达水平明显降低,而CD66c⁺基底细胞却在疯狂扩增——两者的变化完全同步。
直给逻辑链:
ERBB4的作用远不止守住上皮细胞身份这么简单。它就像肺部的“多面守护者”,在免疫和血管系统里也扮演着关键角色。
在免疫层面,ERBB4能调控巨噬细胞的状态:它既可以促进巨噬细胞向抗纤维化的M2型极化,又能通过负反馈回路限制过度炎症反应,避免炎症风暴对肺组织的二次伤害。在血管内皮细胞中,ERBB4被NRG1激活后,能通过PI3K/Akt信号通路减少细胞凋亡,保护肺血管在损伤中存活——这对于新冠、肺栓塞等疾病导致的血管损伤至关重要。
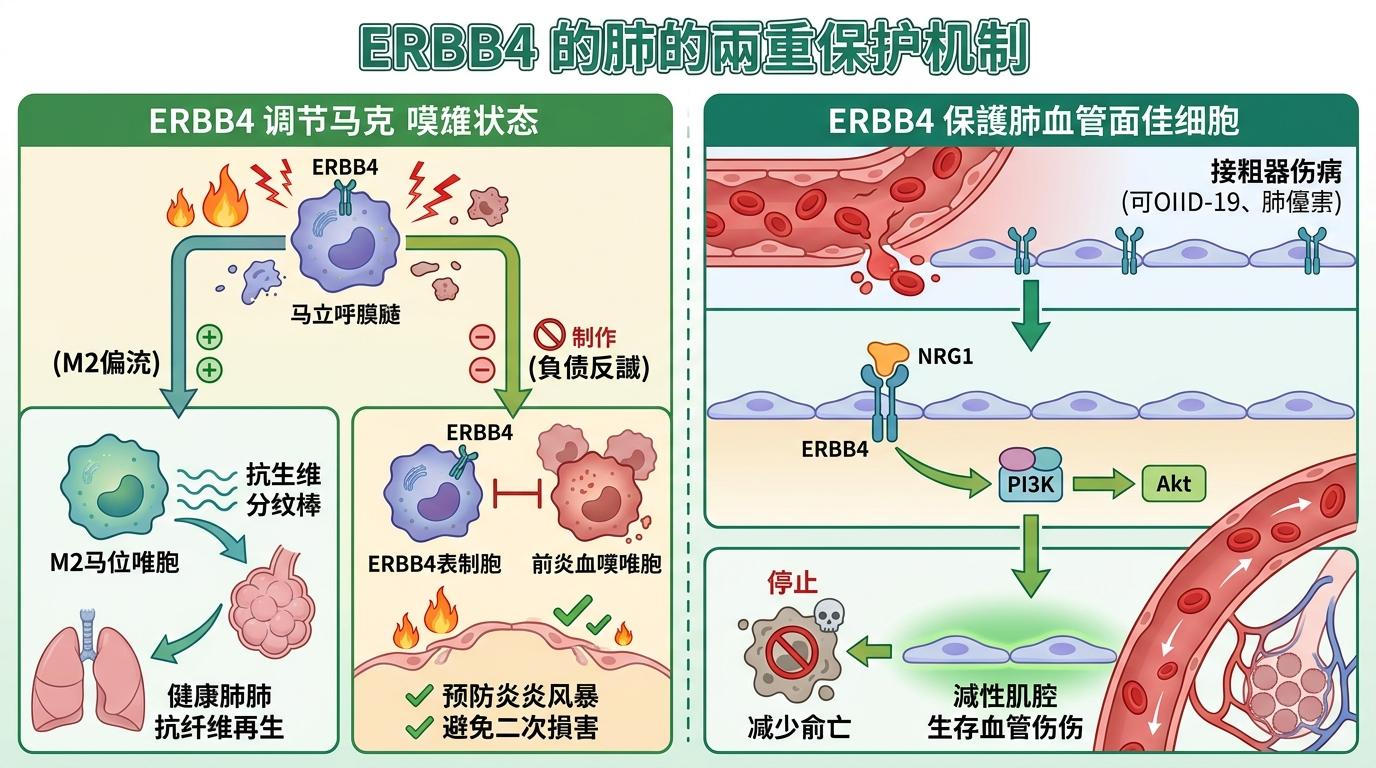
当然,这项研究也留下了未解的谜题:ERBB4的不同剪接异构体在肺损伤中是否有不同作用?如何精准激活ERBB4而不影响其他信号通路?这些问题,正是未来把实验室发现转化为临床治疗的关键。
我们总以为疾病是“外敌入侵”,却忘了很多时候是身体自己的细胞“站错了队”。ERBB4的发现,让我们看到了一种全新的治疗思路:与其直接杀死异常细胞,不如帮它们找回自己的“身份”。
“守住细胞身份,就是守住肺的未来。”这句话不仅适用于肺纤维化,也适用于所有因细胞异常转分化导致的疾病。从实验室里的肺类器官到未来的临床药物,这场关于“身份”的研究,才刚刚拉开序幕——而我们已经看到了希望的微光。