对抗知识焦虑,从看懂这条开始
App 下载
诺奖科学家全职来华,解码细胞能量分子引擎
能量转换机制|X射线晶体学|膜蛋白复合物|吉林大学|哈特穆特·米歇尔|分子细胞生物学|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
能量转换机制|X射线晶体学|膜蛋白复合物|吉林大学|哈特穆特·米歇尔|分子细胞生物学|生命科学
你体内每一次心跳、每一次呼吸的能量,都来自细胞膜上一群只有纳米级大小的“分子引擎”——膜蛋白复合物。过去半个世纪,人类始终无法看清它们的真实模样,直到1985年,哈特穆特·米歇尔用X射线晶体学敲开了这扇门:他首次解析出光合反应中心膜蛋白的三维结构,让人类第一次在原子尺度上,看见光能如何被转化为细胞可利用的化学能。如今,这位诺奖得主全职加盟吉林大学,带着他的团队继续深挖细胞能量转换的核心秘密。
膜蛋白的难,难在“居无定所”。它们嵌在脂质双层构成的细胞膜里,一半亲水一半疏水,一旦离开原生环境就会迅速变性失活。米歇尔当年的突破,靠的是用去污剂模拟细胞膜的脂质环境,硬生生让这些“不安分”的蛋白结成了可供解析的晶体。这一步,打破了“膜蛋白无法结晶”的学界铁律,也为整个膜蛋白结构生物学奠基——要知道,人类60%的药物靶点都是膜蛋白,没有结构就没有精准靶向的可能。
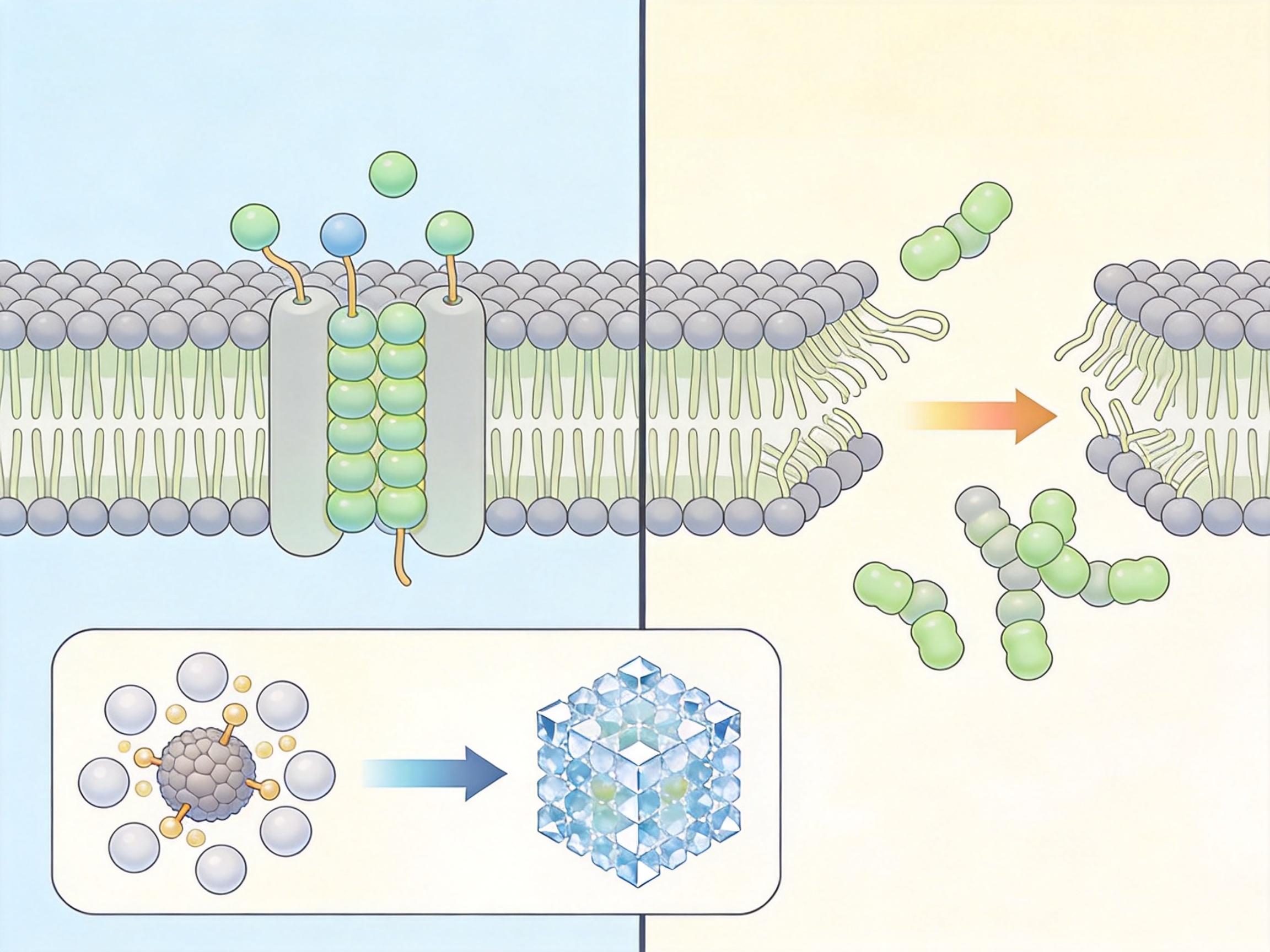
如果把细胞能量转换比作一座水电站,膜蛋白复合物就是那台旋转的水轮机。以光合反应中心为例,米歇尔解析的结构清晰展示了:光能如何激发特殊叶绿素分子释放电子,电子如何沿着蛋白内部的“导线”(铁硫簇、醌类分子)定向传递,最终驱动质子跨膜形成梯度——就像水电站拦起的水位差,而这个梯度的能量,会被另一种膜蛋白ATP合酶转化为细胞的“能量货币”ATP。这个过程的效率高达90%以上,是人类任何人工能量装置都望尘莫及的。
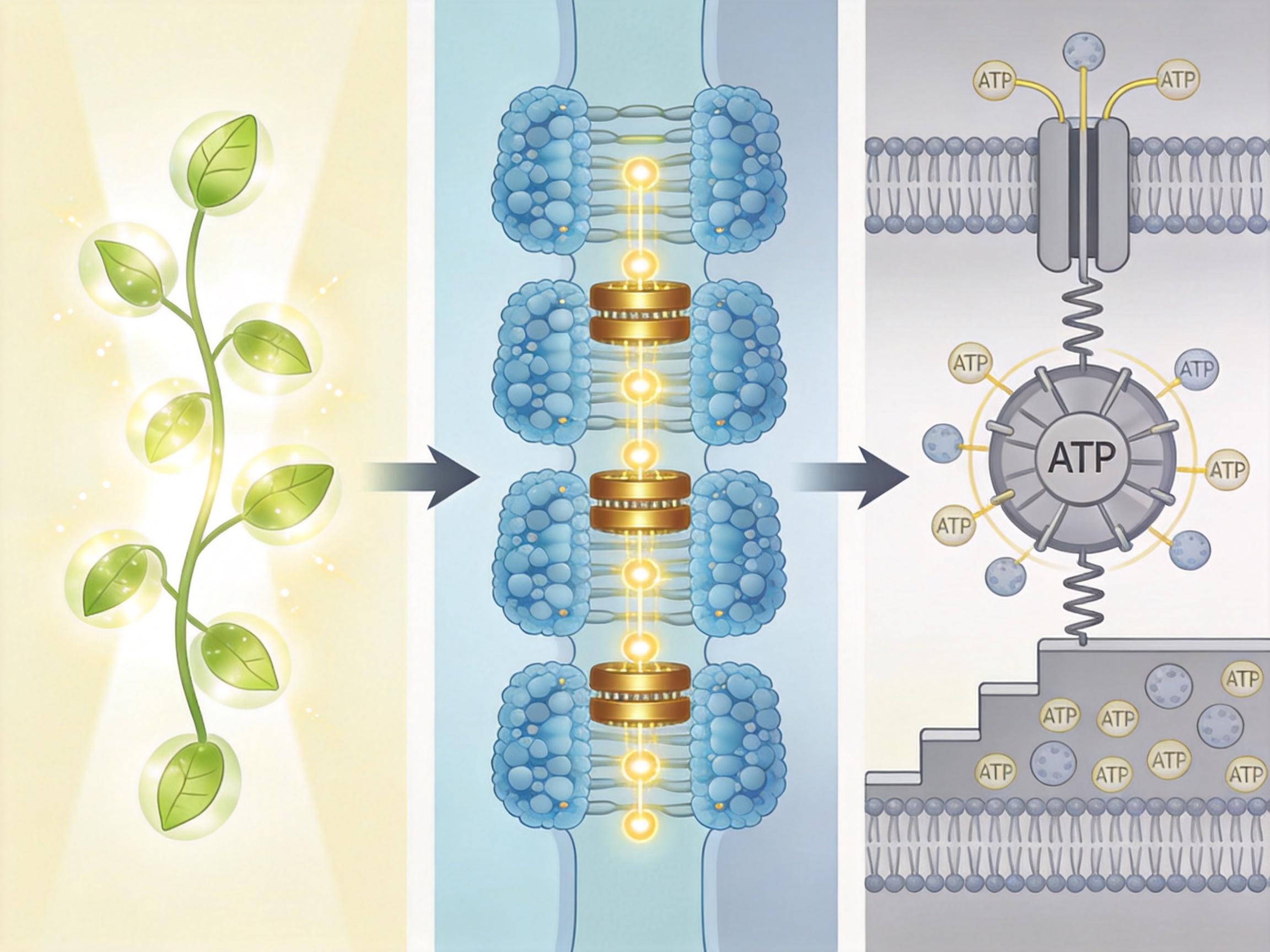
米歇尔的加盟,不止是引入一位顶尖科学家,更是带来了一套从基础研究到应用的完整逻辑。他的团队近年在呼吸链膜蛋白复合物上的研究,已经揭示了细胞有氧呼吸中电子传递与质子泵送的耦合机制——这是人类衰老、神经退行性疾病的核心靶点之一。而吉林大学的平台,能让这些基础研究更快对接临床需求:比如针对线粒体膜蛋白的结构设计药物,治疗因能量代谢障碍导致的疾病。
但我们也得清醒地看到,当前的膜蛋白研究仍有未竟之地。比如,我们能解析静态结构,却很难捕捉它们工作时的动态构象——就像能拍下水电站的照片,却看不到水轮机旋转的瞬间;我们能理解单个蛋白的功能,却还没完全搞清楚它们在细胞膜上形成的“超复合物”如何协同工作。这些,正是米歇尔团队接下来要攻坚的方向。
从看清一个蛋白的结构,到读懂一套能量转换的逻辑,再到用这些逻辑设计药物、模拟生物能源系统,膜蛋白研究的每一步,都在重新定义人类对生命本质的理解。而诺奖科学家的到来,让中国在这场解码生命能量的竞赛中,拿到了一张更靠前的入场券。
看见结构,才能读懂生命的能量密码。