对抗知识焦虑,从看懂这条开始
App 下载
看分子结构找新药,AI破解难治病困局
基因调控|特发性肺纤维化|肝癌|分子结构预测|密歇根州立大学|新药研发|大语言模型|医学健康|人工智能
对抗知识焦虑,从看懂这条开始
App 下载
基因调控|特发性肺纤维化|肝癌|分子结构预测|密歇根州立大学|新药研发|大语言模型|医学健康|人工智能
当肝细胞在体内疯狂增殖成最凶险的肿瘤,当肺间质被纤维化一点点啃噬却无药可医,人类在实验室里的传统武器已经疲于应对——筛选一款能精准修正基因紊乱的新药,要在数百万种化合物里反复试错,耗时数年甚至更久。
但密歇根州立大学的团队用AI改写了这个剧本:他们训练出的模型,只看化学分子的结构,就能精准预测它会如何调控基因表达。靠着这个工具,他们在肝癌和特发性肺纤维化这两大难治疾病中,找到了能缩小肿瘤、逆转纤维化的候选化合物。
这不是科幻,是刚发表在《Cell》上的现实。更关键的是,他们是怎么让AI读懂分子和基因的对话的?
你可以把每个化学分子想象成一串独特的密码,而基因则是细胞里的开关——有的该开却关着,有的该关却狂开,疾病就由此而来。过去,要知道某串密码能拨动哪个开关,只能靠一次次实验;现在,密歇根州立大学的GPS模型,就是能直接翻译这串密码的AI。
这个模型的训练逻辑,像极了教AI识别猫和狗:不是看图片,而是喂给它18746种化合物、978个基因在4种细胞系里的数百万组实验数据——相当于告诉AI,“这个分子会让A基因活性升高”“那个分子会让B基因活性降低”。
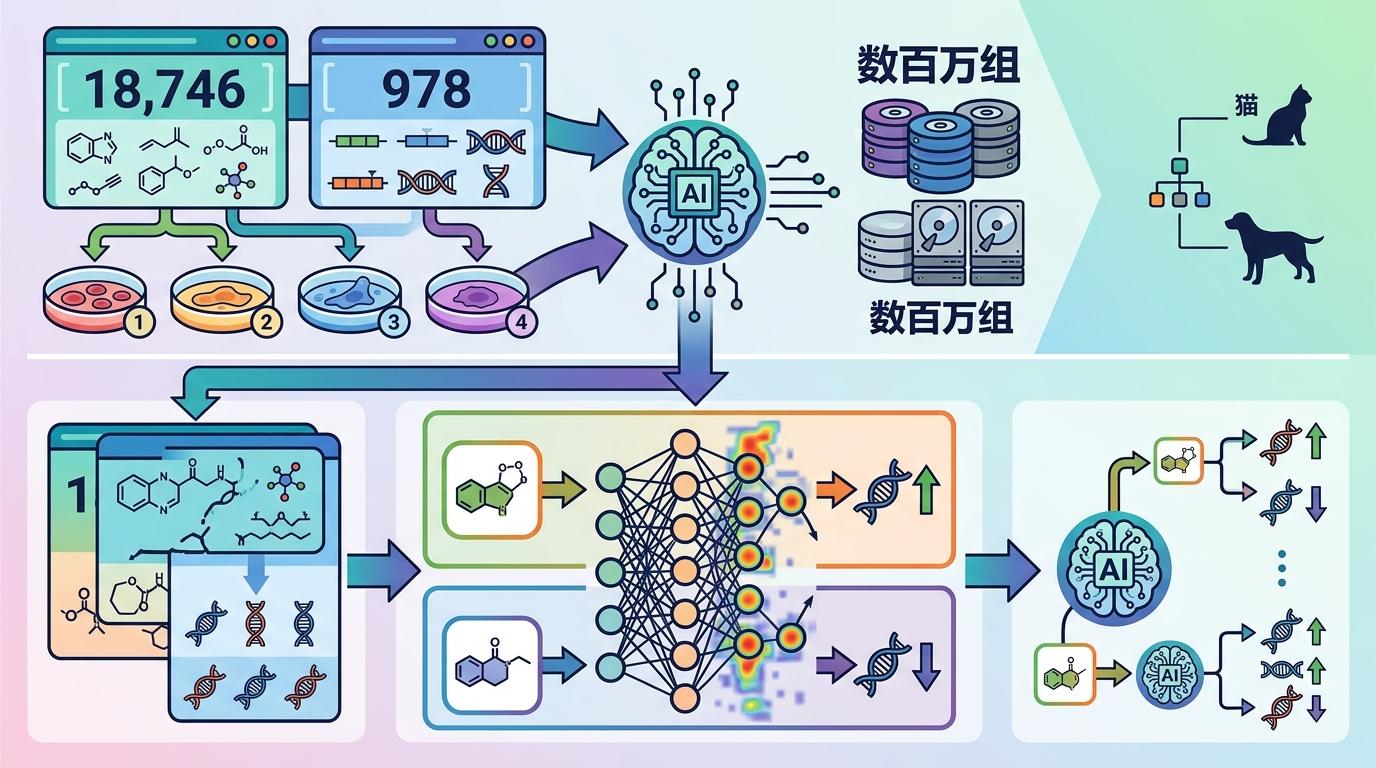
但生物数据从来都是“噪音里找信号”:有的实验结果误差大,有的数据甚至互相矛盾。团队用了一套“稳健协同学习”策略,让模型像经验丰富的侦探,自动过滤掉不可靠的“伪线索”,只留下能真正反映分子和基因关系的强信号。最终,它能精准预测2198个关键基因的表达变化,覆盖细胞周期、转录调控等核心生物过程。
打个更通俗的比方:以前我们要找能打开特定门锁的钥匙,得把整串钥匙挨个试;现在AI看一眼钥匙的齿纹,就知道它能开哪扇门,甚至能设计出刚好匹配的新钥匙。
AI算出的“钥匙”,终究要拿到现实里开门。团队把目标对准了两个最棘手的战场:全球第三大癌症死因的肝细胞癌,和诊断后中位生存期仅3年的特发性肺纤维化。
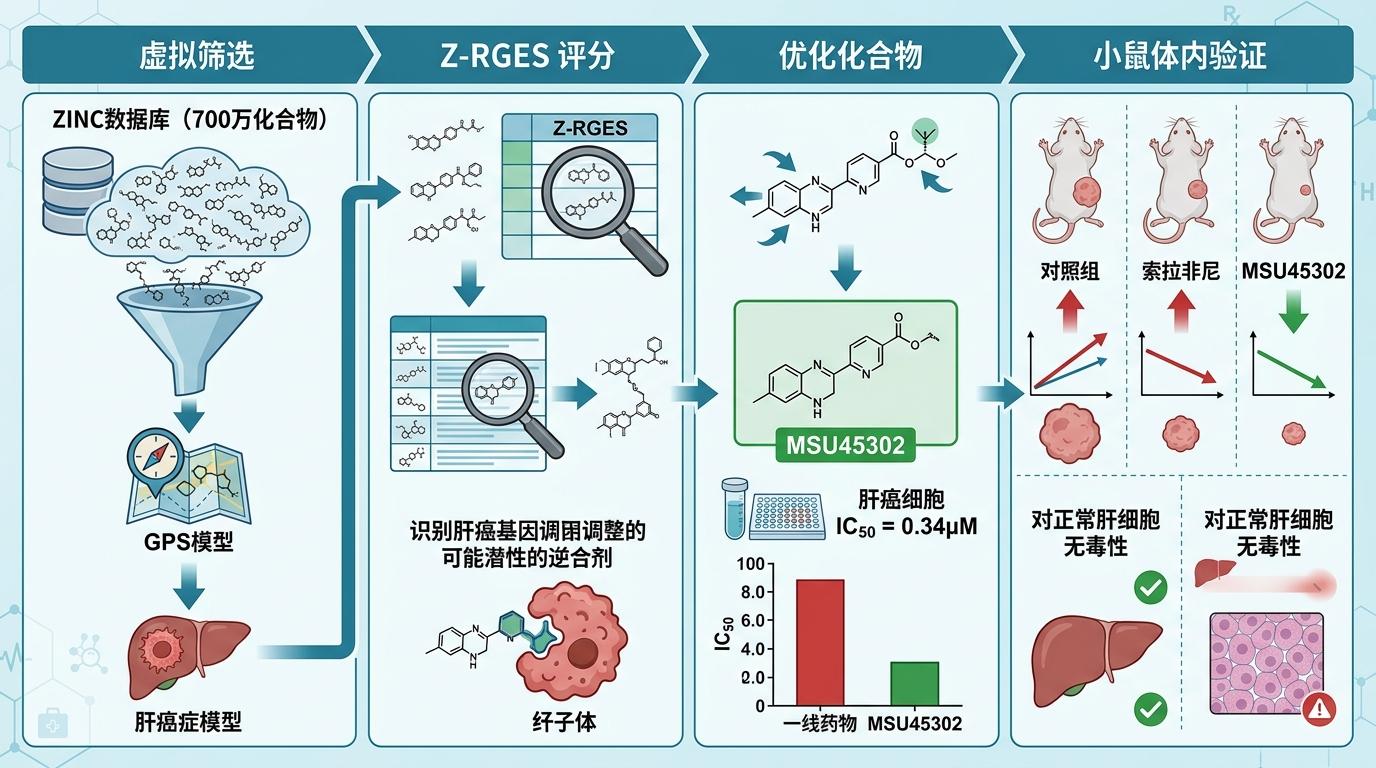
在肝癌领域,他们用GPS模型对着ZINC数据库里的700万种化合物做虚拟筛选,用一种叫Z-RGES的评分体系,找出最有可能逆转肝癌基因紊乱的分子。最终筛选出的化合物里,优化后的MSU45302在肝癌细胞中的IC50值达到0.34μM,比一线药物索拉非尼效果更好;在小鼠肿瘤模型里,它能显著缩小肿瘤体积,还对正常肝细胞没明显毒性。
而在特发性肺纤维化的战场上,他们不仅找到了1个可重定位的老药,还发现了2个全新的候选化合物。这些分子不仅在小鼠模型里展现出抗纤维化效果,还在Corewell Health提供的人类肺组织样本中得到了验证——这个密歇根州最繁忙的肺移植中心,为研究提供了珍贵的活体组织样本,让AI的预测真正落地到人类临床场景。
有意思的是,这不是某一个实验室的单打独斗:计算机科学家训练模型,药理学家合成化合物,临床医生提供样本和验证标准,20多位跨领域研究者花了数年才走完这条路。就像团队里的Edmund Ellsworth博士说的:“药物发现是团队运动,胆小的人干不了。”
更值得关注的是,这个团队没有把GPS模型攥在手里。他们公开了所有代码,还搭建了一个免费的在线平台,全球任何研究者都能用来筛选自己领域的候选药物。
这打破了传统药物研发的“黑箱”模式。过去,大型药企靠着资源垄断,把大量化合物数据锁在自己的数据库里;现在,AI工具的开放让小实验室甚至个人研究者,都能站在同样的起跑线上。比如联邦学习技术的出现,让不同机构可以在不共享原始数据的前提下,共同训练更强大的模型——既保护了商业机密,又能让AI学到更多“经验”。
当然,这场革命也不是没有隐忧:AI模型的“黑箱”特性,让我们有时候只知道它能找到答案,却不知道它是怎么找到的;训练数据的偏差,也可能让AI筛选出的化合物存在潜在风险。但这些问题,正在被不断迭代的技术解决——比如可解释AI的发展,正在一点点揭开AI决策的面纱。
从某种意义上说,这不仅是药物研发的突破,更是科研模式的转变:从闭门造车,到开放协作,AI正在把新药发现变成一场全球参与的接力赛。
当我们回望这场跨越数年的研究,会发现真正的突破从来不是某一个算法或某一个化合物,而是“让AI读懂生命语言”的可能性。它把过去需要数百万次实验才能完成的筛选,压缩到了计算机的算力里;把过去只有大型药企能承担的成本,降低到了普通实验室可以触及的范围。
分子藏密码,AI解天书,生命的答案终将被人类自己读懂。
未来,或许我们不用再为找不到治疗罕见病的药物而绝望,不用再看着亲人被癌症和慢性病折磨却束手无策。因为AI正在帮我们把生命的说明书,翻译成我们能读懂的语言——而那里面,就藏着治愈的希望。