生命最初的“隐形战场”
对于一个新生儿来说,世界充满了未知的奇迹,也潜藏着无形的挑战。当他们离开母体的无菌环境,来到这个充满微生物的世界时,体内一场至关重要的战役便已悄然打响。这场战役的主战场,正是他们娇嫩的肠道。这里是营养吸收的枢纽,也是人体最大的免疫器官,驻扎着超过七成的免疫细胞。然而,在生命最初的几个月里,这支“免疫军队”尚在组建,防御工事远未完善,使得婴幼儿极易受到病原体的侵袭,面临腹泻、肠炎乃至更严重感染的风险。如何为这支初生的军队配备精良的“武器”并教会它们如何战斗,是守护每一个新生命健康的关键。长期以来,科学家们知道母乳、益生菌等因素至关重要,但驱动免疫细胞成熟的精准分子指令,却像一本未被破译的密码书。
一把解锁免疫的“金钥匙”被发现
就在不久前的2026年2月20日,这本密码书被翻开了关键一页。华中农业大学的魏宏逵研究员团队在国际顶尖期刊《科学进展》(Science Advances)上发表了一项突破性研究,揭示了婴幼儿早期肠道免疫发育的一个核心分子调控机制。这项研究如同在复杂的免疫网络中找到一个关键的“开关”及其“钥匙”。
研究的核心发现是:
- 关键“开关”——核受体Nur77:科学家们发现,一种名为Nur77的核受体,在新生小鼠肠道免疫系统的“前线士兵”——第3组固有淋巴细胞(ILC3s)的成熟过程中扮演着“总指挥官”的角色。
- 神秘“钥匙”——天然脂质12R-HETE:团队通过精密的蛋白质-代谢物交互分析,成功鉴定出肠道中天然存在的一种脂质分子——12R-羟基二十碳四烯酸(12R-HETE),正是激活Nur77这名“指挥官”的“钥匙”。
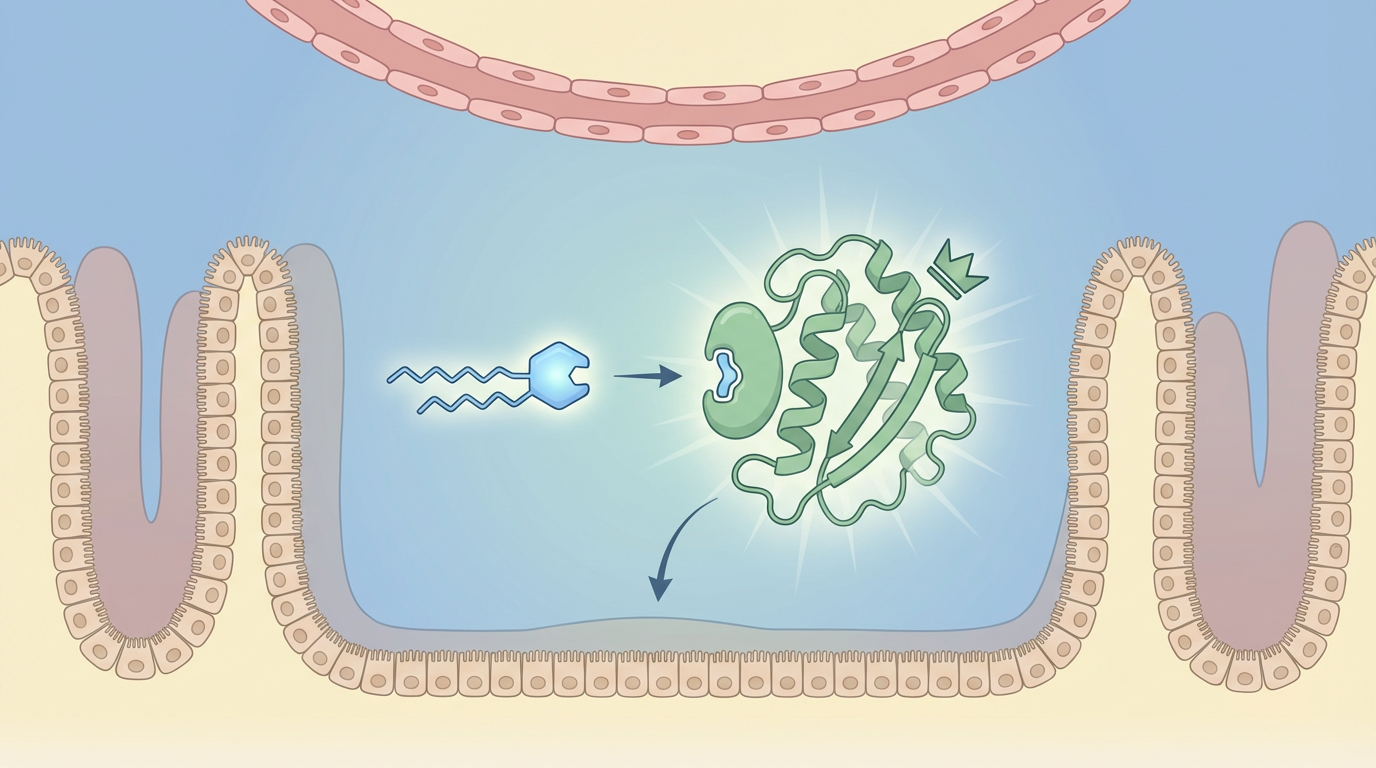
- 精准调控:当“钥匙”(12R-HETE)插入“锁孔”(Nur77)并转动时,会启动一系列指令。Nur77被激活后,会直接调控一个名为Impdh1的基因,并增强关键转录因子T-bet的表达。这套指令能高效地将一群“新兵蛋子”ILC3细胞(NKp46-亚型)训练成战斗力更强的“精英特种兵”(NKp46+亚型)。
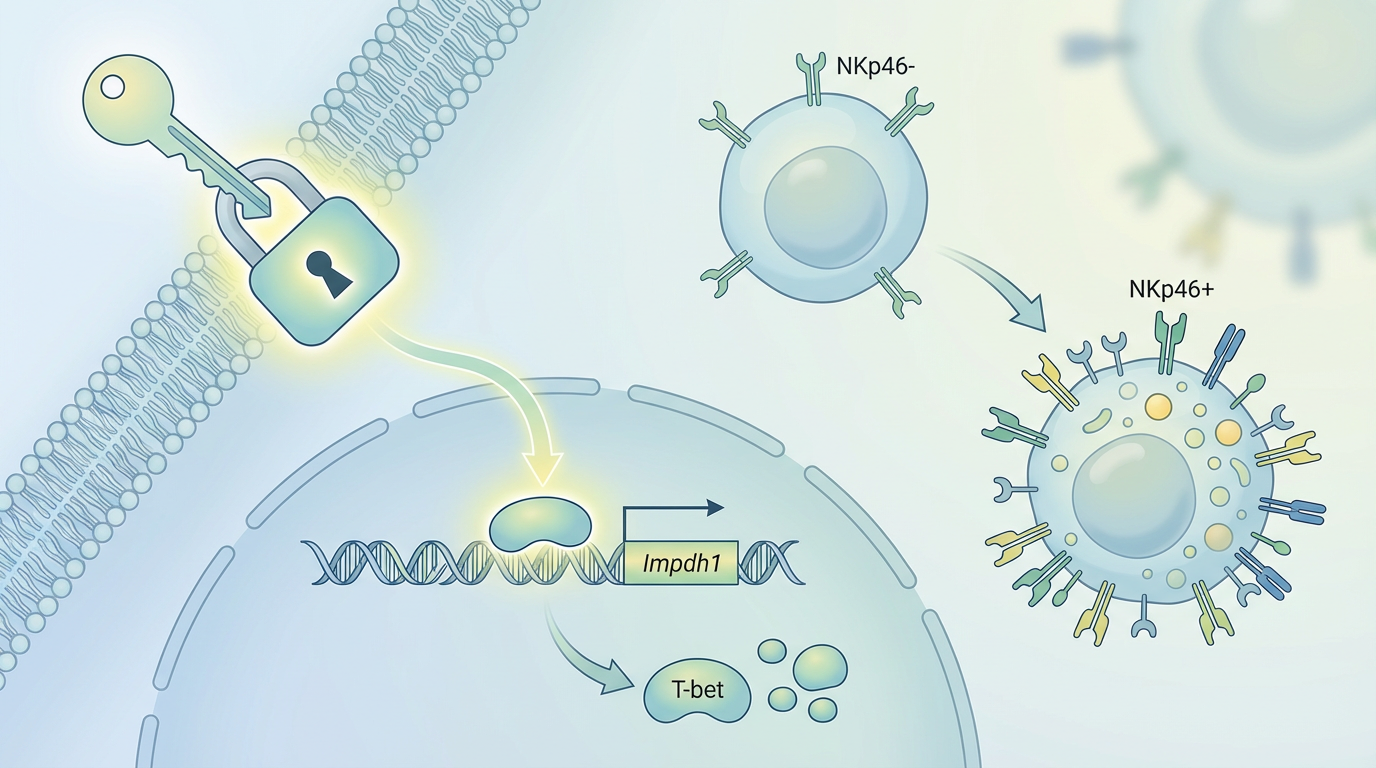
实验结果令人振奋:缺失Nur77的小鼠,其肠道内的“精英特种兵”数量锐减,面对鼠伤寒沙门氏菌等病原体入侵时,抵抗力显著下降。而当给新生小鼠补充这种关键脂质12R-HETE后,它们的肠道免疫防线变得更加坚固,能更有效地抵御感染。这一发现,首次完整描绘了一条由特定代谢物驱动、经由核受体精准调控、最终塑造先天免疫细胞功能的信号通路。
肠道免疫的“交响乐”:多重因素的协同
魏宏逵团队的发现固然是里程碑式的,但婴幼儿肠道免疫的发育并非由单一通路决定,而是一场由内外多种因素共同谱写的复杂“交响乐”。近年来的其他研究,共同揭示了这场音乐会的宏大与精妙。
内部的“遗传乐谱”与“表观调音师”:
- 基因的开关与锁定:浙江大学汪洌团队的研究发现,组蛋白去甲基化酶UTX和JMJD3就像“调音师”,通过擦除基因上的“静音”标记(H3K27me3),决定了ILC3细胞是倾向于发展成抵抗细菌的“步兵”(NKp46+ ILC3),还是抵抗真菌的“炮兵”(CCR6+ ILC3)。这说明,免疫细胞的命运不仅由基因决定,更受到精密的表观遗传调控。
- 复杂的信号网络:清华大学郭晓欢团队则揭示,经典的Wnt/β-catenin信号通路在ILC3中扮演着意想不到的“刹车”角色,它会抑制ILC3的发育和功能。这表明,免疫系统内部充满了复杂的制衡机制,以防免疫反应过度或不足。
- 蛋白质生产线的效率:此外,清华大学李华兵团队发现,tRNA(转运核糖核酸)的微小化学修饰(m1A修饰)竟能影响ILC3的蛋白质合成效率,进而决定其生存与增殖。这好比是后勤保障线,确保“士兵”能得到充足的补给。
外部的“环境指挥家”:
- 肠道菌群的塑造:从出生那一刻起,肠道菌群就开始定植,它们是这场交响乐中最重要的“客座指挥家”。特定的益生菌,如罗伊氏乳杆菌,能代谢母乳或食物成分,产生特定的信号分子(如次级胆汁酸),直接影响ILC3的发育。可以说,一个健康的菌群生态,是训练一支强大免疫军队的先决条件。
- 母乳的“黄金馈赠”:母乳不仅是食物,更是天然的“免疫启动剂”。其中富含的母乳低聚糖(HMOs)是特定益生菌(如婴儿双歧杆菌)的“专属美食”,能帮助有益菌快速占领生态位,从而间接优化ILC3的发育环境。
这些研究共同描绘了一幅壮丽的图景:在遗传蓝图的基础上,表观遗传、信号通路、RNA修饰等内部程序,与肠道菌群、母乳营养等外部环境信号相互交织、协同作用,共同指挥着婴幼儿肠道免疫系统的构建。
从实验室到摇篮:未来的新希望
揭示12R-HETE与Nur77的分子机制,不仅仅是一次科学认知上的飞跃,更重要的是,它为保护婴幼儿肠道健康打开了全新的应用之门。这一发现的现实意义和未来潜力巨大。
1. 精准营养干预成为可能:既然12R-HETE这种天然脂质能有效激活免疫系统,未来或许可以将其作为一种新型的“免疫营养素”。
- 优化婴幼儿配方奶粉:通过在奶粉中添加12R-HETE或其安全的前体物质,模拟母乳对免疫系统的天然促进作用,为无法母乳喂养或高风险(如早产、剖宫产)的婴儿提供更强的免疫支持。
- 开发功能性食品或补充剂:针对免疫发育迟缓的婴幼儿,开发基于此通路的功能性食品,主动、精准地促进其肠道免疫成熟。
2. 新型治疗靶点的出现:Nur77通路为药物研发提供了新靶点。
- 靶向激动剂:可以研发模拟12R-HETE功能的小分子药物,用于治疗严重的肠道感染或炎症性肠病(IBD)等免疫失调疾病。这种药物可以直接激活Nur77,快速动员和强化肠道的先天免疫防线。
3. 结合前沿技术的“组合拳”:
- 工程益生菌:结合基因工程技术,改造益生菌使其能高效生产12R-HETE或其它有益的免疫调节分子,实现“活体药物”在肠道内的原位、持续治疗。
- 仿生递送系统:利用纳米技术,将12R-HETE等活性分子包裹起来,实现靶向递送,提高其在肠道内的稳定性和生物利用度,最大化其功效并降低潜在风险。
未解之谜与前行之路
尽管前景光明,但从基础研究走向临床应用,依然有漫长的道路要走。眼下,几个关键问题亟待解答:
- 12R-HETE的来源之谜:研究发现12R-HETE的产生不依赖肠道菌群,那么在人体内,它究竟是由哪些细胞、通过何种途径合成的?解开这个谜团,将有助于更精准地调控其水平。
- 从鼠到人的转化:此次研究主要基于小鼠模型,Nur77通路在人类婴幼儿肠道免疫发育中是否扮演同样的角色?其调控网络是否存在物种差异?这些都需要通过更接近人体的研究模型(如类器官共培养体系)和临床研究来验证。
- 安全性与平衡性:Nur77是一个多功能分子,也参与细胞凋亡、代谢等多种过程。长期或过度激活此通路是否会带来意想不到的副作用?如何精准调控其活性,在增强免疫的同时避免引发其他问题,是临床转化前必须解决的核心安全问题。
结语
婴幼儿的肠道,这个微小却至关重要的“战场”,其宁静与健康关乎一生的福祉。华中农业大学团队的发现,如同一束光,照亮了早期免疫发育的幽深角落,让我们得以窥见一个由微小脂质分子精心编排的防御之舞。这不仅是对生命智慧的又一次深刻洞察,也为我们守护下一代的健康提供了更科学、更精准的武器。未来,随着更多未解之谜被揭开,我们有理由相信,通过驾驭这些深藏于体内的分子语言,我们将能更有效地帮助每一个新生命,打赢他们人生中的第一场关键战役。



