对抗知识焦虑,从看懂这条开始
App 下载
益生菌蛋白解锁胰腺炎治疗:免疫代谢双调控
脂质代谢紊乱|肠道屏障|TLR2受体|阿克曼氏菌|Amuc_1098蛋白|感染性疾病|分子细胞生物学|生命科学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
脂质代谢紊乱|肠道屏障|TLR2受体|阿克曼氏菌|Amuc_1098蛋白|感染性疾病|分子细胞生物学|生命科学|医学健康
当急性胰腺炎发作时,胰腺会像被自己消化的“发炎器官”,重症患者死亡率可达30%,而目前临床只能靠输液、禁食等支持疗法“熬”过急性期。但南京的三个医学团队最近找到了突破口:一种来自肠道益生菌的微小蛋白,居然能同时按住过度炎症、修复肠道屏障,还能把紊乱的脂质代谢拉回正轨。它不是抗生素,也不是激素,而是从我们体内本来就有的细菌身上“拆”下来的关键分子——这到底是怎么做到的?
你可以把Amuc_1098蛋白想象成一位精准的“炎症调解员”——它是肠道益生菌阿克曼氏菌表面的“钥匙”,专门匹配免疫细胞上的TLR2受体。
当急性胰腺炎触发全身炎症风暴时,TLR2原本会像过度敏感的警报器,拉响NF-κB通路的红色警报,召唤大量促炎因子进攻胰腺。但Amuc_1098的到来会让警报“降档”:它绑定TLR2后,不会触发过度炎症,反而启动PI3K-Akt信号通路,像给炎症踩下刹车,同时促进肠道紧密连接蛋白的表达——就像给肠道补上漏风的木板,阻止细菌和毒素跑到胰腺“火上浇油”。
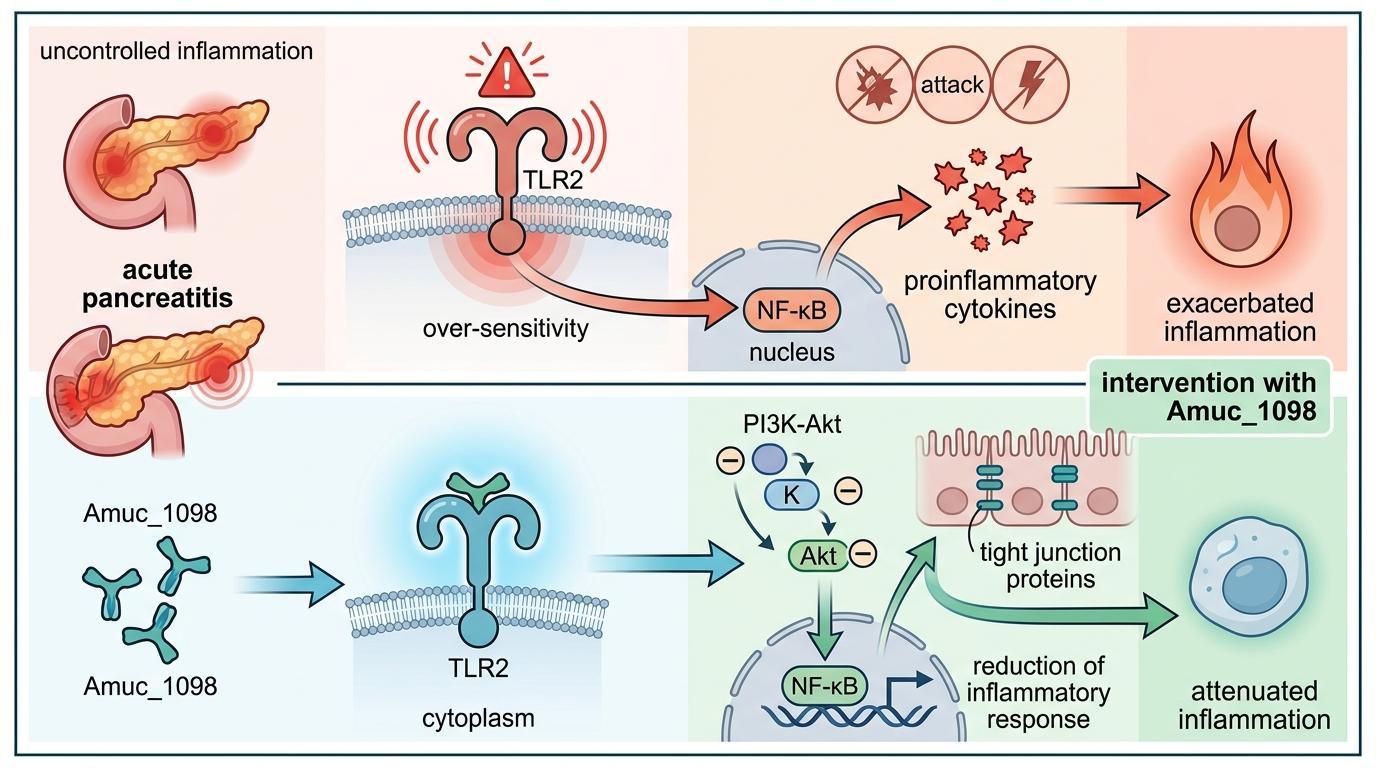
但真实的机制比这更精确:Amuc_1098通过TLR2精准调控NF-κB的活性,让促炎因子TNF-α、IL-1β的表达下降40%-60%,同时提升抗炎因子IL-10的水平,把免疫反应拉回平衡状态。
急性胰腺炎患者的血液里,甘油磷脂会像脱缰的野马——这种构成细胞膜的关键脂质一旦代谢紊乱,会产生大量促炎介质,把胰腺细胞的“细胞膜城墙”啃出窟窿。
Amuc_1098的第二个任务,就是把这些野马赶回正轨。它通过TLR2信号通路,调节甘油磷脂的代谢酶活性,让失衡的磷脂酰胆碱、磷脂酰乙醇胺重新回到正常比例。就像给受损的细胞膜“补砖”,既恢复了细胞的稳定性,又减少了促炎脂质的产生。
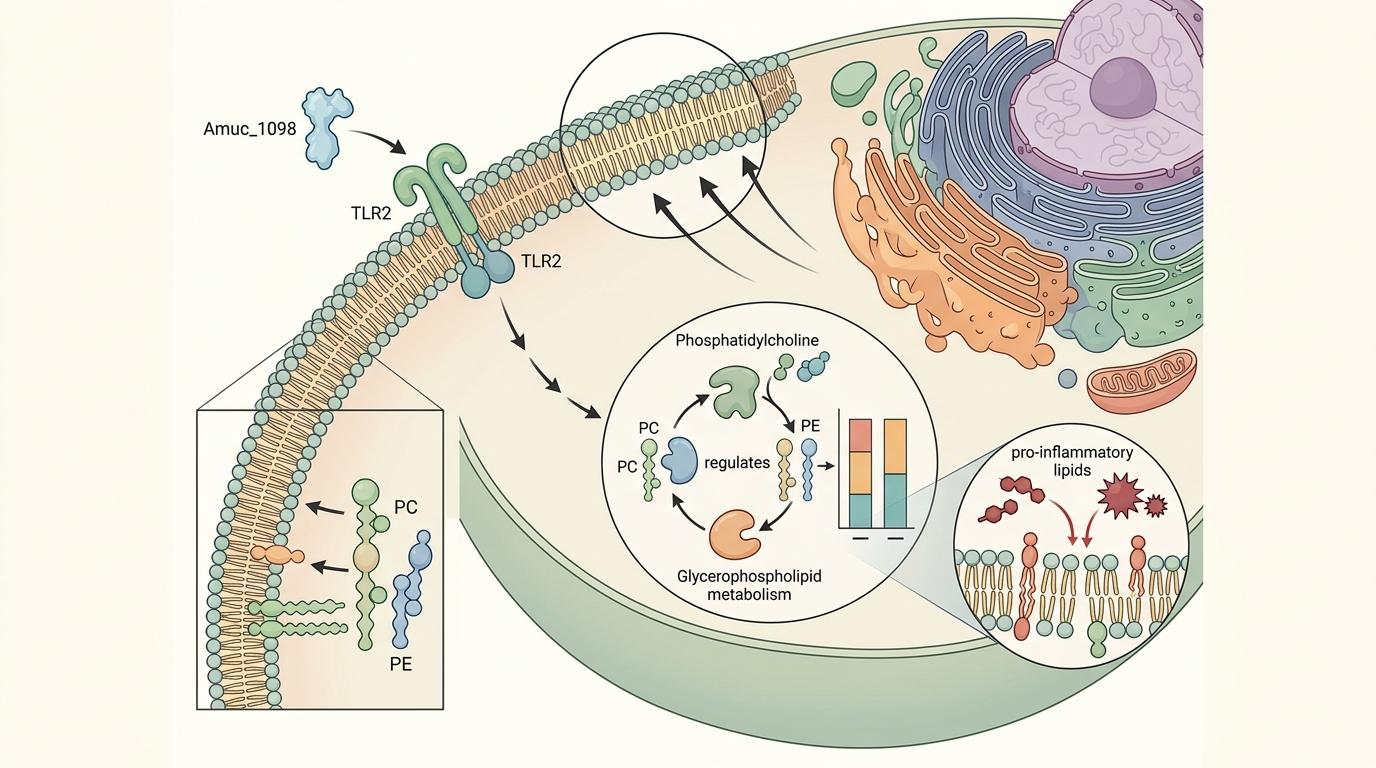
临床数据显示,急性胰腺炎患者血清中甘油磷脂类代谢物的含量显著升高,而Amuc_1098干预后,这些异常指标能恢复近60%。在小鼠模型中,补充Amuc_1098的胰腺炎小鼠,胰腺水肿和坏死程度下降了一半以上,血清淀粉酶水平降低了30%。
这项研究的突破,离不开三个团队的跨学科协作:南京中医药大学的基础研究者负责解析蛋白的分子机制,南京鼓楼医院和江苏省中医院的临床医生提供患者样本和临床需求,甚至还融入了中医对“肠道-胰腺轴”的理解。
他们解决了一个关键难题:过去益生菌治疗胰腺炎的效果不稳定,因为活菌的活性受肠道环境影响太大。而Amuc_1098是提纯的蛋白,70℃巴氏杀菌后还能保持活性,口服后能稳定到达肠道发挥作用。目前团队正在优化重组蛋白的递送系统,比如用纳米颗粒包裹,让它能更精准地到达炎症部位。
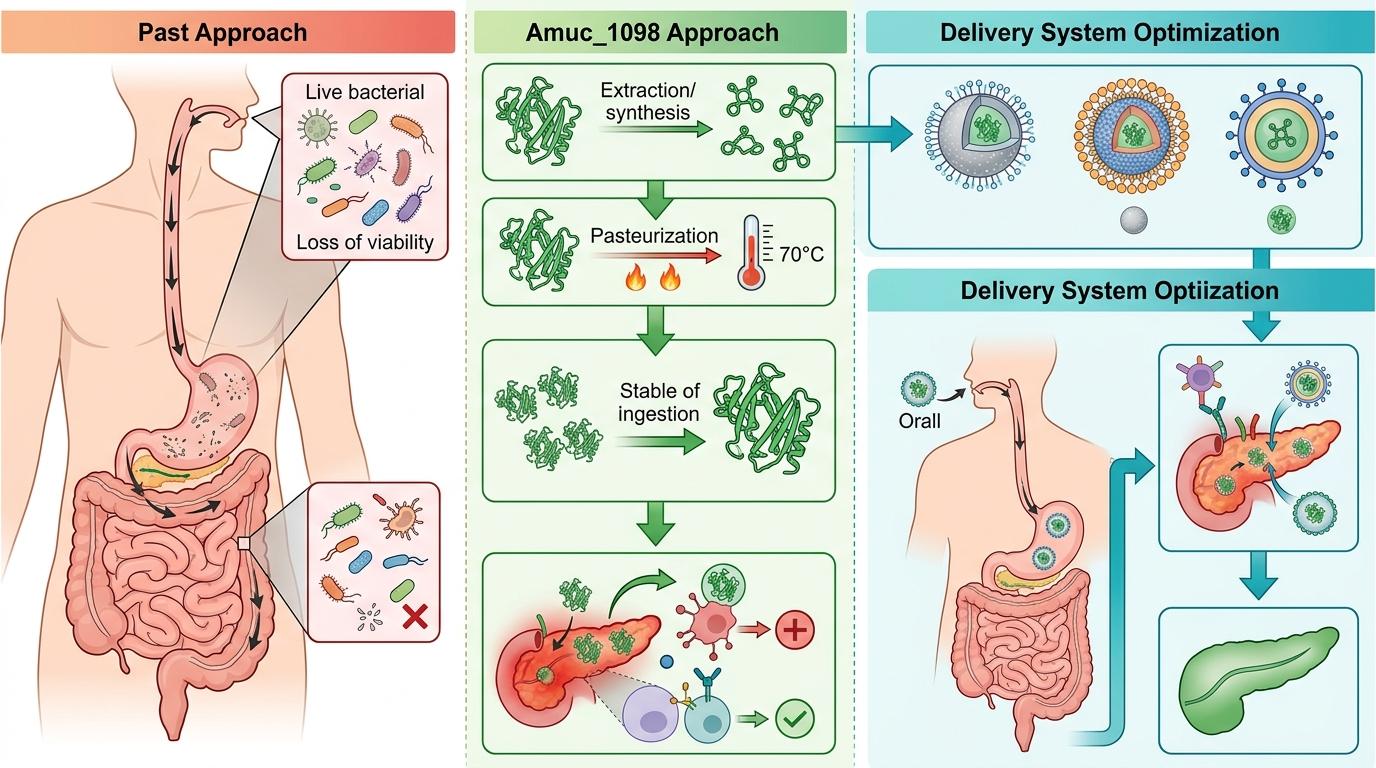
不过也有需要警惕的地方:Amuc_1098的作用依赖于TLR2受体的正常功能,对于TLR2表达异常的患者,效果可能打折扣。未来还需要更大规模的临床试验,确定不同人群的最优剂量。
我们总把细菌当成敌人,却忘了肠道里的益生菌是我们最古老的“共生伙伴”。Amuc_1098的发现,其实是重新读懂了这种共生关系:细菌不是靠“活着”来保护我们,而是靠它们分泌的微小分子,精准调控我们的免疫和代谢。
“肠道里的蛋白,能救发炎的胰腺”——这不仅是急性胰腺炎治疗的新方向,更提醒我们:从自身菌群里寻找治疗靶点,可能比发明全新的药物更安全、更有效。未来的炎症性疾病治疗,或许就藏在我们每个人的肠道里。