
19 天前

19 天前
当ICU里的急性肺损伤患者插着呼吸机挣扎,当肺纤维化病人看着CT上越来越密的白色阴影无能为力,医生手里的武器始终有些尴尬:要么盯着炎症猛压,要么对着纤维化硬堵,从来没有一种药能同时按住肺损伤的两头。直到2026年3月,南方科大、中山大和南洋理工的团队联合掏出了一款吸入式RNA药物——它瞄准了肺里一个叫ANGPTL4的蛋白,在小鼠身上既治好了细菌性肺炎,又逆转了纤维化,甚至连病毒感染的肺损伤也能缓解。这不是某条通路的小修小补,而是直接掐住了肺损伤的总开关。为什么一个蛋白能管这么多?
你可以把ANGPTL4想象成肺里的「应急总指挥」——平时它是个好好先生,帮着调节脂质代谢、维护血管稳定;但一旦肺里出现损伤,不管是细菌病毒入侵,还是毒素引发的纤维化,它都会立刻变身成「混乱制造者」。
它是个结构特殊的分泌型糖蛋白,被蛋白酶切成两半后各干各的:N端片段管脂质代谢,能抑制脂肪细胞摄取脂肪酸;C端片段则专搞破坏——在肺炎时它会拆毁肺泡和血管之间的紧密连接,让体液漏进肺里形成水肿,还会招引炎症细胞疯狂浸润;到了纤维化阶段,它又会推着胸膜间皮细胞「变身」成成纤维细胞,玩命分泌胶原蛋白,把肺变成硬邦邦的纤维块。
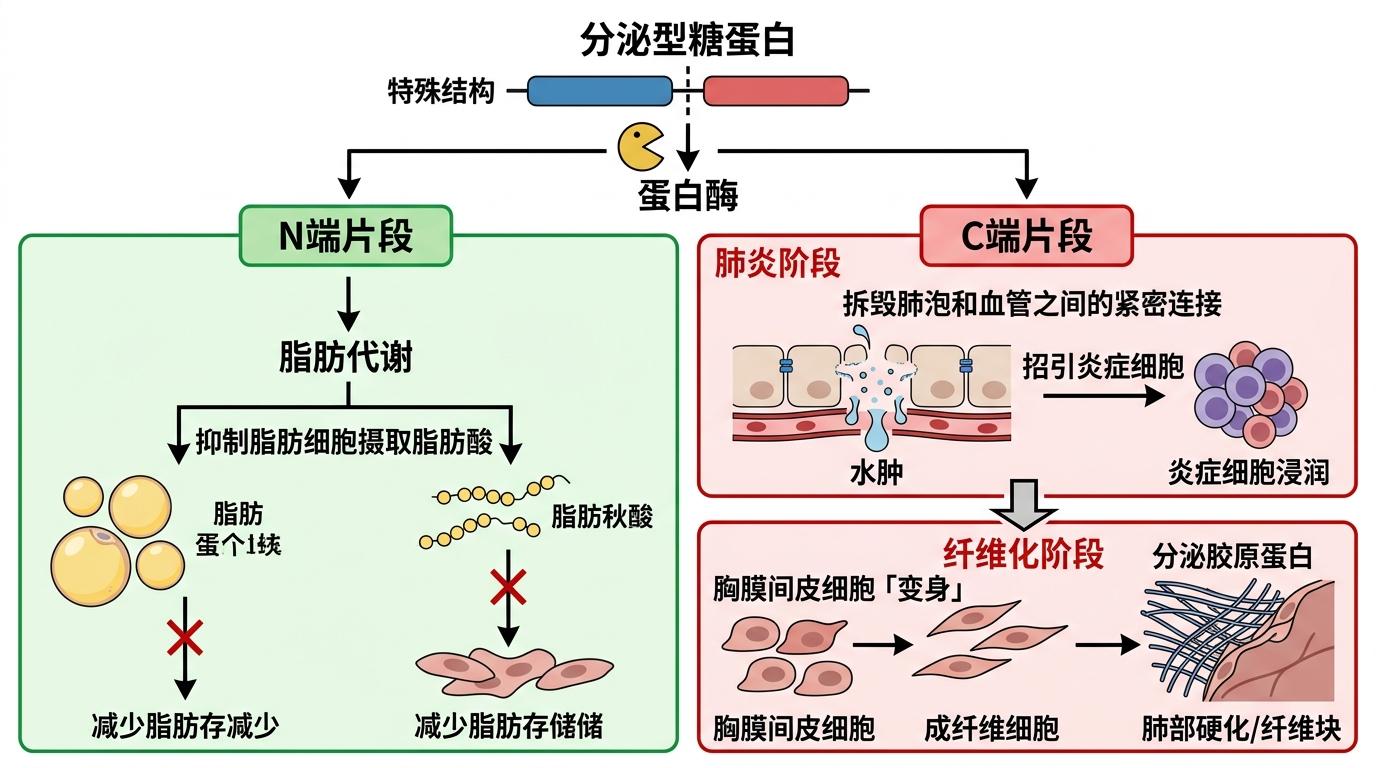
更关键的是,不管肺损伤的起点是什么,ANGPTL4都会成为核心调控者:肺炎时它牵着免疫和氧化应激的线,纤维化时它攥着细胞外基质重塑的闸,近半数差异表达的基因都在它的掌控之下。就像不管是火灾还是洪水,现场指挥的都是同一个人——只要按住它,就能同时扑灭不同的火情。
既然ANGPTL4是总开关,那直接让它「闭嘴」不就行了?但难就难在怎么精准地让肺里的ANGPTL4闭嘴,又不影响身体其他部位的正常功能——毕竟它在肝脏、脂肪组织里还是个好蛋白。
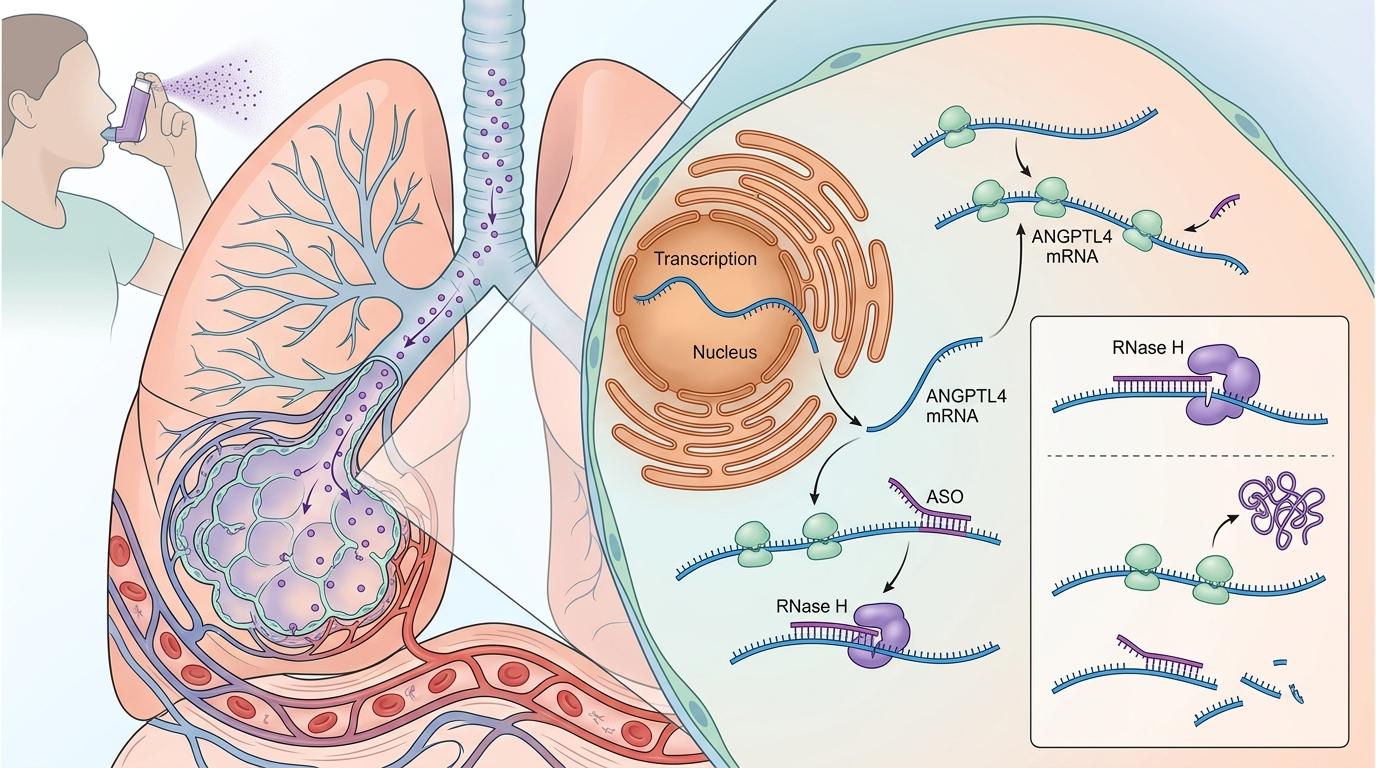
研究团队用的是反义寡核苷酸(ASO)技术,简单说就是一段能和ANGPTL4的mRNA精准配对的小RNA,一旦配对成功,就能阻止mRNA翻译成蛋白,相当于在基因转录的最后一步给它踩了刹车。为了让这款ASO只去肺里,他们选择了吸入给药的方式——就像哮喘病人吸激素一样,药物直接沉积在肺泡表面。
动物实验的结果相当惊艳:
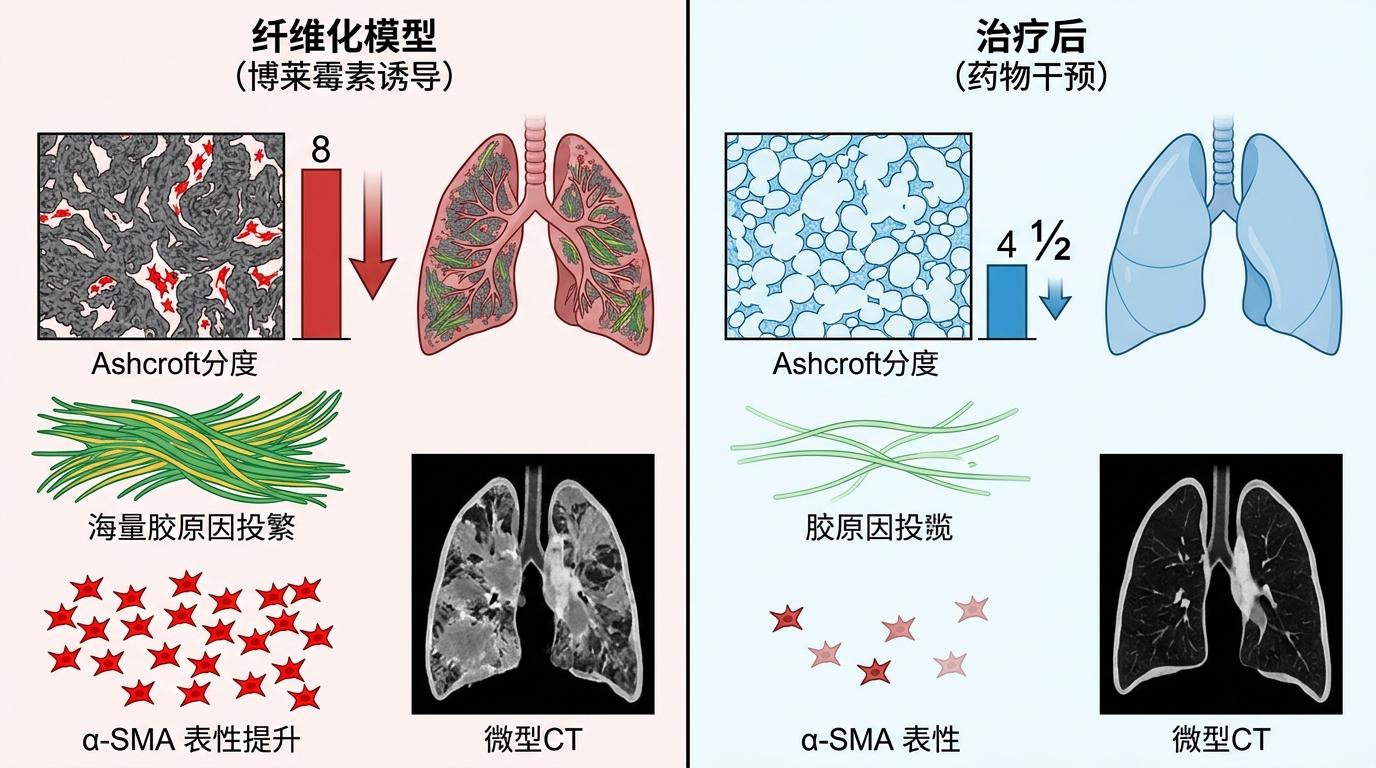
更妙的是,Cy5标记的ASO在肺里一待就是144小时,全身扩散极少——相当于给肺做了个局部的基因手术,其他器官完全没感觉。
这款药物的广谱疗效确实让人兴奋,但有个容易被忽略的细节必须提:ANGPTL4的双重性。
它在肺损伤时是坏蛋白,但在正常生理状态下,它能帮着调节血脂、维持血管屏障,甚至在某些炎症场景里还能发挥抗炎作用——比如在结肠炎模型里,它会抑制过度的炎症反应。如果长期用ASO抑制它,会不会影响肺的正常脂质代谢?会不会在某些特殊情况下反而削弱了肺的防御能力?
目前的动物实验只做了短期观察,还没有长期抑制的安全性数据;而且不同人种的ANGPTL4表达水平可能存在差异,药物剂量也需要精准调整。更重要的是,它只是按住了损伤的总开关,但肺损伤背后的缺氧、代谢重编程等深层问题,还需要更多研究来破解。
说白了,这不是一劳永逸的「神药」,而是给肺损伤治疗打开了一扇新的门——从「单靶点救火」转向「多通路调控」的门。
当我们习惯了用「对抗」的思路治病——用抗生素杀细菌,用激素压炎症,用抗纤维化药堵胶原——这款ANGPTL4-ASO给了我们一个新的视角:有时候不用忙着消灭敌人,只要按住那个制造混乱的总指挥,身体自己就能恢复秩序。
「精准调控,比强力对抗更重要。」这句话不仅适用于肺损伤治疗,也适用于越来越多的复杂疾病。未来的药物或许不再是单一的「武器」,而是能精准调节身体内环境的「调节器」——就像给紊乱的系统重新校准,让它回到本该有的平衡状态。而这款小小的吸入式RNA药,就是这个方向上的一块重要路标。
点击充电,成为大圆镜下一个视频选题!