对抗知识焦虑,从看懂这条开始
App 下载
两种酶的异动,揭开胰腺癌的隐秘序曲
罗斯威尔帕克癌症中心|癌前病变|代谢酶|KRAS基因突变|胰腺癌|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
罗斯威尔帕克癌症中心|癌前病变|代谢酶|KRAS基因突变|胰腺癌|肿瘤学|医学健康
当医生在CT影像上看到胰腺上的阴影时,往往已经错过了阻止胰腺癌的最佳时机——这种癌症的五年生存率不足13%,超过80%的患者确诊时已是晚期。但很少有人知道,胰腺癌的种子早在肿瘤形成前数年就已埋下:胰腺腺泡细胞会在炎症或损伤后转变成导管样细胞,这是一种可逆的修复状态,可一旦碰上KRAS基因突变,它就可能滑向不可逆的癌前病变。
罗斯威尔帕克癌症中心的Megan Radyk博士团队,最近在《Nature Metabolism》上发表的研究,终于抓住了这场隐秘癌变的关键开关——两种不起眼的代谢酶,正在悄悄操控着癌前病变的生死走向。为什么有的修复会变成癌变的温床?这正是他们要解开的谜题。
研究团队首先对胰腺化生组织和癌前病变组织做了RNA测序,结果锁定了两个异常升高的酶:葡萄糖-6-磷酸脱氢酶(G6PD)和苹果酸酶1(ME1)。这两种酶的共同作用,是制造一种叫NADPH的分子——你可以把它看成细胞的“后勤总管”:一方面给细胞合成脂质、DNA等“建筑材料”提供能量,另一方面还能清除细胞里的活性氧(ROS),这种物质就像细胞里的“自由基垃圾”,积累过多会损伤DNA,催生病变。
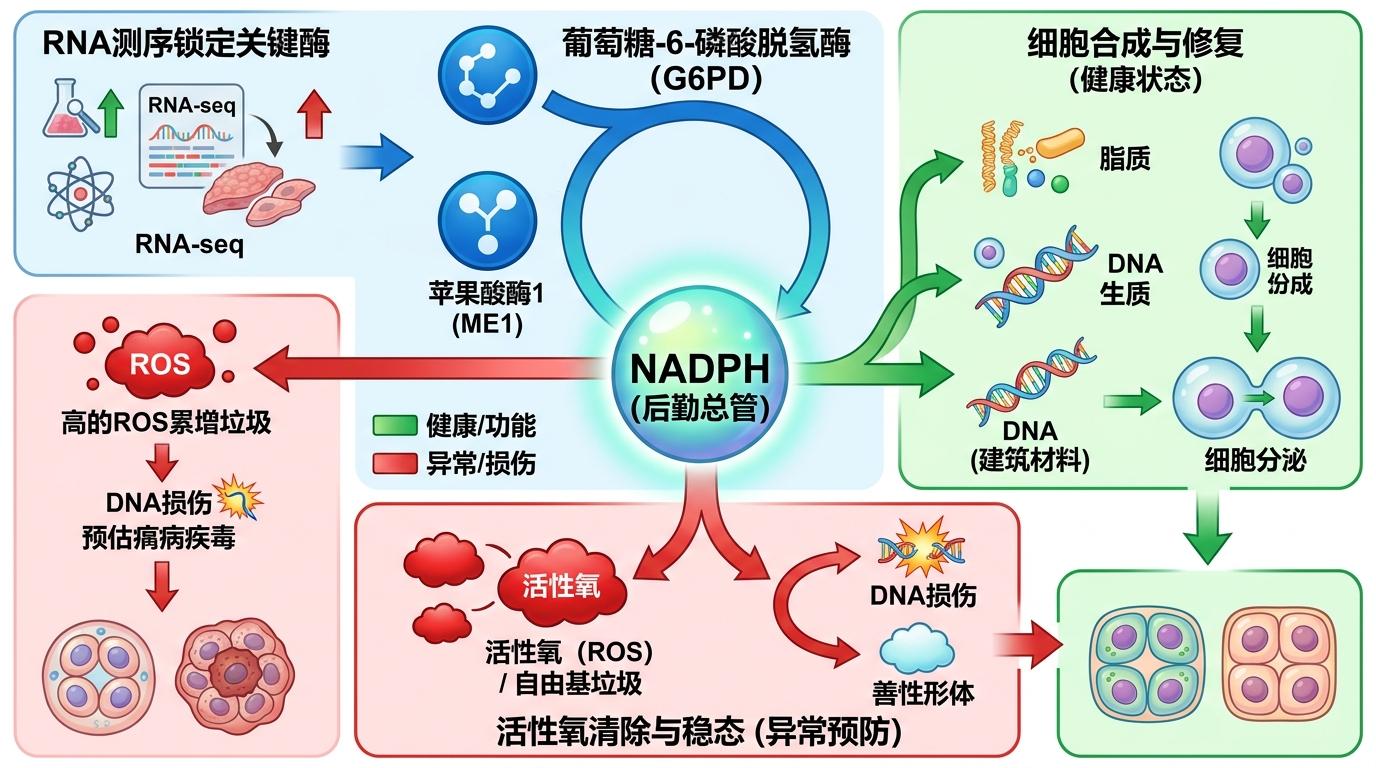
为了验证这两种酶的作用,团队做了一组对比实验: 在携带KRAS突变的小鼠模型中,降低G6PD的活性后,癌前病变的数量明显增加;完全敲除ME1的小鼠,也出现了同样的结果。进一步检测发现,当这两种酶的水平下降时,细胞里的活性氧水平会飙升,就像后勤总管罢工后,垃圾堆满了车间。
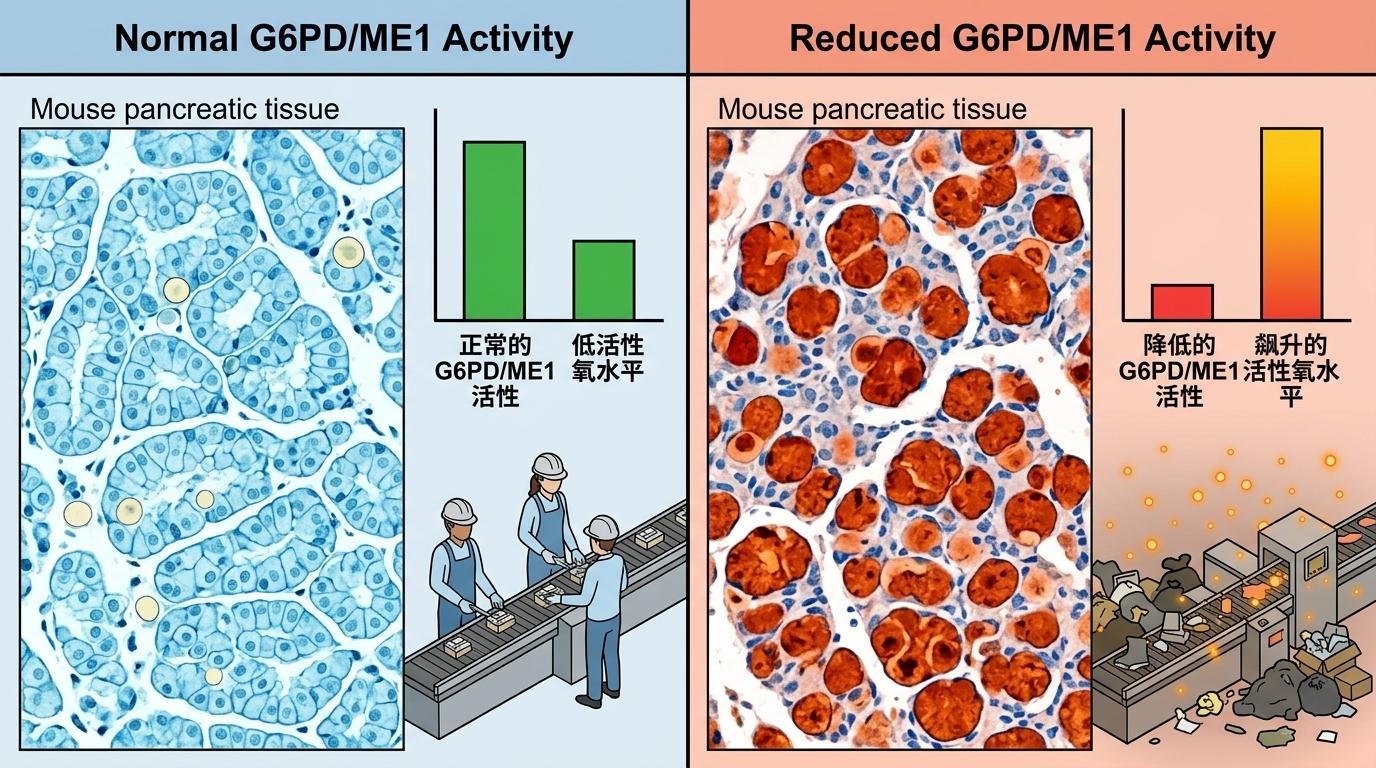
更关键的是,用抗氧化剂谷胱甘肽处理细胞,或是给小鼠喂抗氧化剂N-乙酰半胱氨酸,就能阻止这种癌前病变的爆发——这直接坐实了活性氧堆积是癌变加速的核心推手。
有意思的是,虽然G6PD和ME1都能制造NADPH、清除活性氧,但它们在癌变过程中的角色却截然不同。
研究发现,G6PD的缺失只会增加癌前病变的数量,却不会直接推动病变向恶性肿瘤转化;但ME1的缺失,不仅会让癌前病变增多,还会显著加速它向侵袭性胰腺癌的进展。这背后的差异,藏在NADPH的另一个作用里:除了抗氧化,它还能通过调节脂质过氧化和铁死亡通路,影响肿瘤细胞的耐药性和恶性程度。ME1除了制造NADPH,还能直接调控这条通路,而G6PD则只专注于抗氧化。
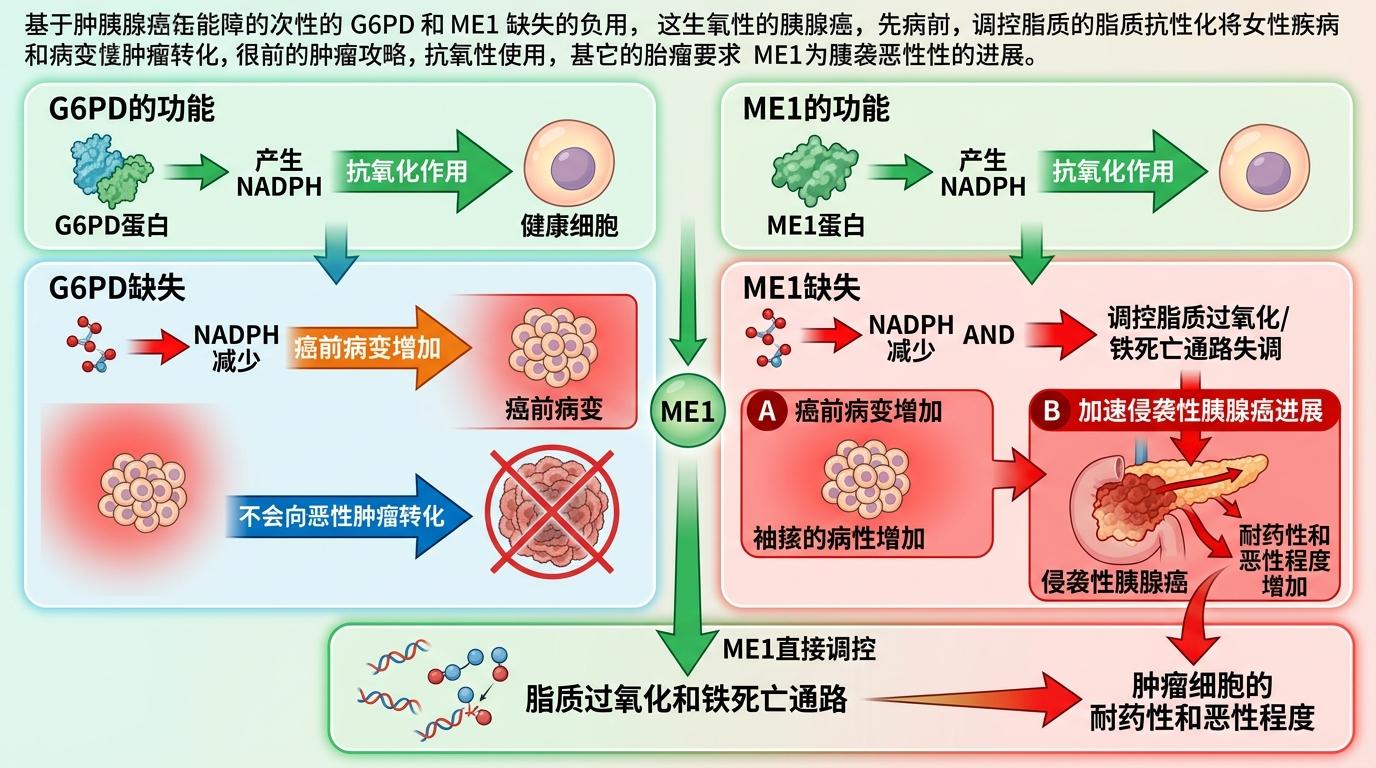
这种“阶段特异性”的作用,也在人类胰腺组织样本中得到了验证:在癌前病变阶段,两种酶的水平都会升高,但到了恶性肿瘤阶段,ME1的表达变化会更显著。这意味着,针对ME1的干预,可能不仅能阻止癌前病变,还能在早期阻断癌变的进程。
说句大白话,G6PD是“病变消防员”,只管灭火减少隐患;而ME1则是“癌变刹车”,既能灭火,还能防止车子失控冲下山。
现在的问题是,这些发现离真正帮到患者还有多远?
首先,这两种酶的表达水平,有可能成为胰腺癌早筛的生物标志物。目前常用的CA19-9标志物,不仅在慢性胰腺炎等良性疾病中会出现假阳性,还无法在癌前病变阶段发挥作用。如果能通过血液检测G6PD和ME1的水平,再结合影像学检查,或许能更早地揪出那些处于癌变边缘的患者。
其次,针对这两种酶的靶向药物,也有了研发的方向。比如,通过激活G6PD或ME1的活性,增强细胞的抗氧化能力,阻止癌前病变的进展;或是在癌变早期,抑制ME1的功能,阻断恶性转化的通路。不过,代谢酶在正常细胞中也发挥着重要作用,如何做到只针对病变细胞,避免影响正常组织,是研发时需要解决的核心问题。
目前,已有针对谷氨酰胺代谢、糖酵解等通路的胰腺癌靶向药物进入临床试验,而G6PD和ME1的发现,相当于给这个“代谢治疗工具箱”又加了两件新工具。
过去我们总把胰腺癌看成“突然降临的恶魔”,但这项研究让我们看到,它更像一场缓慢酝酿的火灾——从最初的细胞损伤,到化生,再到癌前病变,每一步都有代谢信号在悄悄操控。
早一步抓住代谢信号,就能早一步掐灭癌变的火苗。
未来,当医生再面对胰腺癌高危人群时,或许不用再等到影像上出现阴影,只要通过血液里的酶水平变化,就能判断出“火灾隐患”的等级,甚至提前出手,把癌变的可能扼杀在萌芽状态。而这,正是这场研究最动人的地方:它没有给我们带来治愈晚期癌症的奇迹,却给了我们一个阻止癌症发生的机会。