对抗知识焦虑,从看懂这条开始
App 下载
从麻疹药到尼帕克星,结构生物学撬开病毒命门
中国科学家团队|原子分辨率结构|RNA聚合酶|ERDRP-0519|尼帕病毒|感染性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
中国科学家团队|原子分辨率结构|RNA聚合酶|ERDRP-0519|尼帕病毒|感染性疾病|医学健康
2026年1月,印度西孟加拉邦的两名医护人员被送进ICU——他们感染了尼帕病毒,这种被列为最高生物安全等级的病原体,致死率最高可达90%,至今没有特效药。就在人们以为又要重演无药可医的困境时,一个意外的线索出现:一款原本针对麻疹的口服药ERDRP-0519,居然能轻微抑制尼帕病毒的复制。为什么一款麻疹药能跨界对抗致命病毒?它的效力又为何如此有限?中国科学家团队用三年时间,在原子层面找到了答案。
你可以把病毒的RNA聚合酶想象成一台高速运转的复印机——它负责复制病毒的遗传物质,是病毒繁殖的核心机器。而ERDRP-0519,就是试图卡住这台复印机的“异物”。
研究团队首次解析了ERDRP-0519与麻疹、小反刍兽疫、尼帕三种病毒聚合酶的三维复合物结构,分辨率达到原子级别。他们发现,这款药物能精准卡进三种病毒聚合酶的同一个“口袋”——这个口袋位于聚合酶的掌状结构域,是病毒复制时RNA模板和核苷酸原料的必经通道。这就解释了它为何能跨界抑制尼帕病毒。
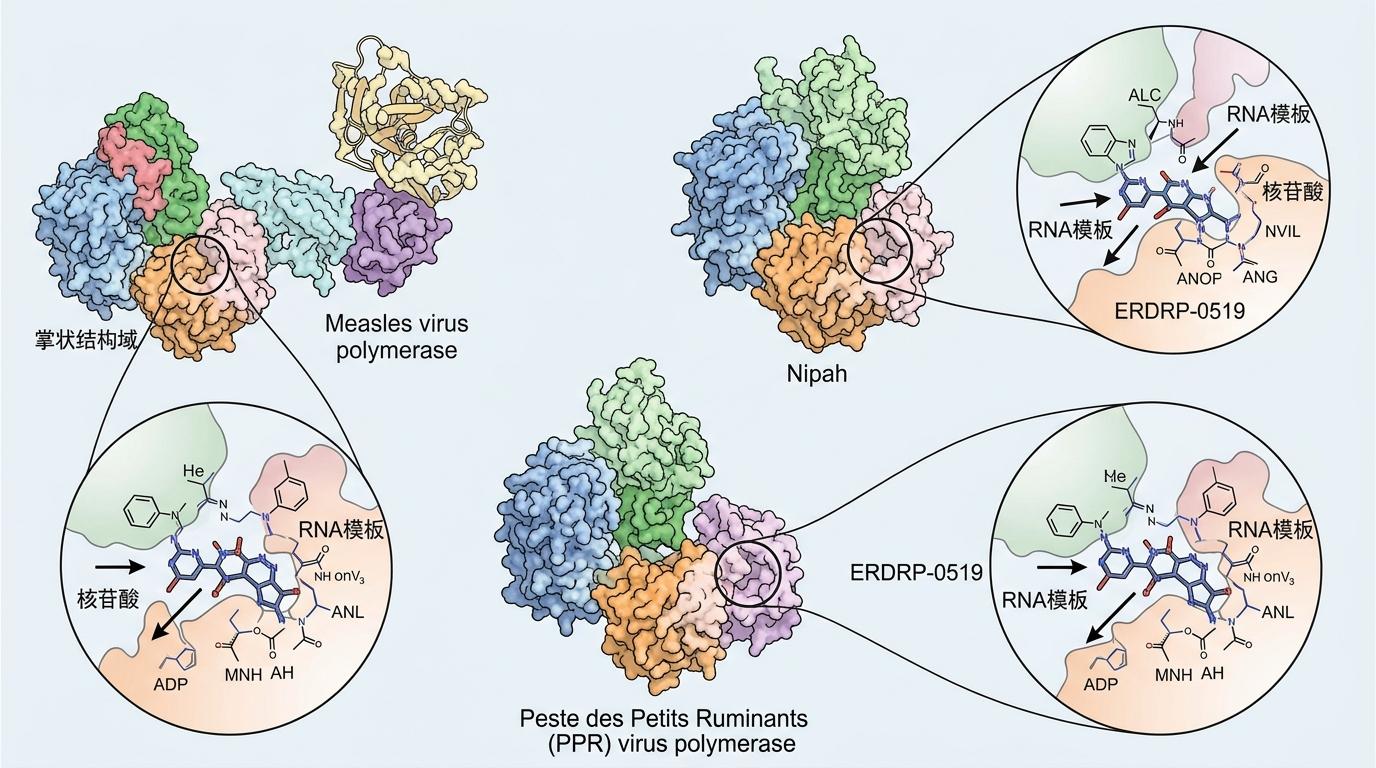
但细节里藏着差异的秘密。在麻疹病毒的聚合酶中,ERDRP-0519能和周围的氨基酸残基形成紧密的氢键和疏水作用,像钥匙插进匹配的锁芯一样稳固;而在尼帕病毒的聚合酶中,这个口袋的形状略有不同,药物要卡进去,必须迫使局部结构发生“变形”,这种“费力”的结合导致它的抑制效力大幅降低——就像一把钥匙能插进不同的锁,但有的锁转不动,有的只能勉强拧半圈。
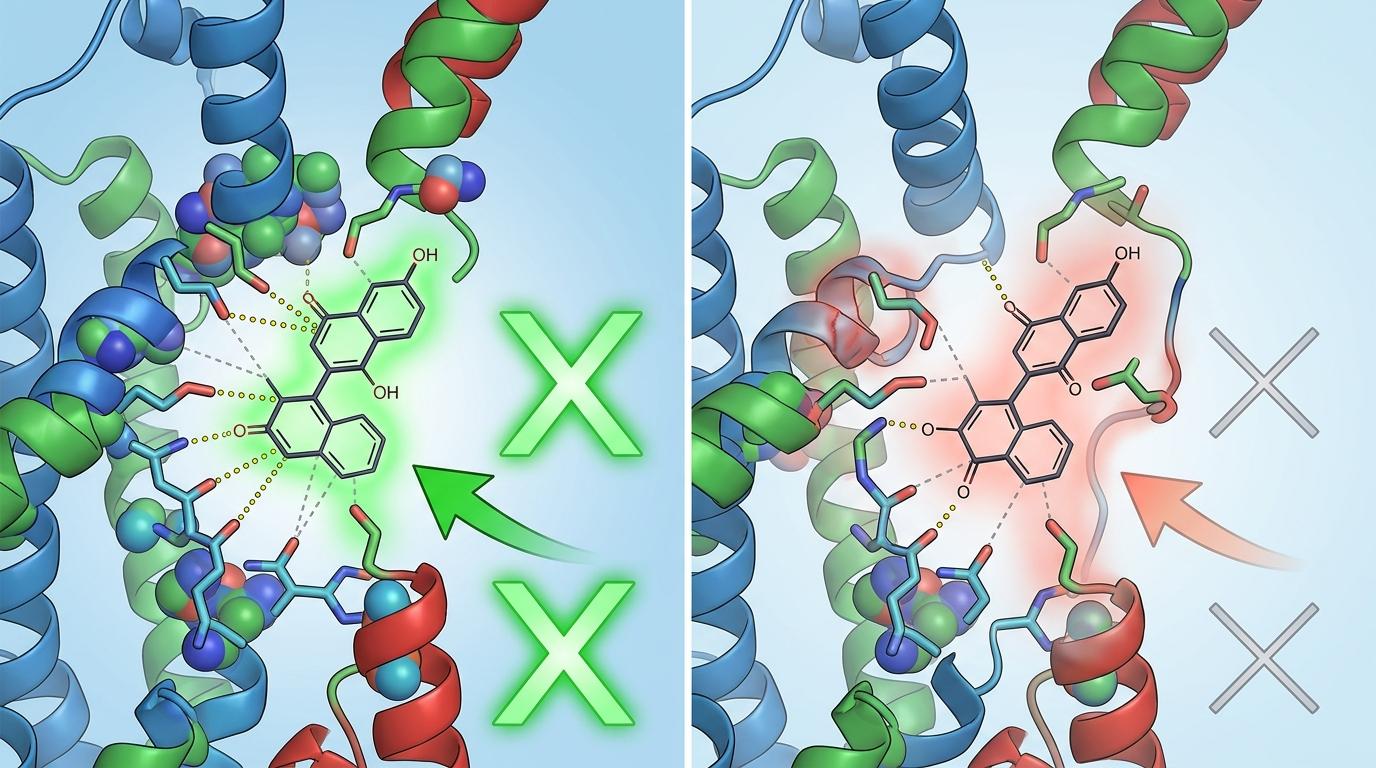
既然找到了尼帕病毒聚合酶的“偏心”所在,科学家们开始对ERDRP-0519进行“定制化改造”——这就是基于结构的理性药物设计:先看清靶点的精确形状,再针对性地修改药物分子。
他们在原药物的分子骨架上,延伸出两个新的化学基团,就像给钥匙加了两个“防滑纹”,专门用来贴合尼帕病毒聚合酶口袋边缘的额外位点。新衍生物GL22和G671就此诞生。
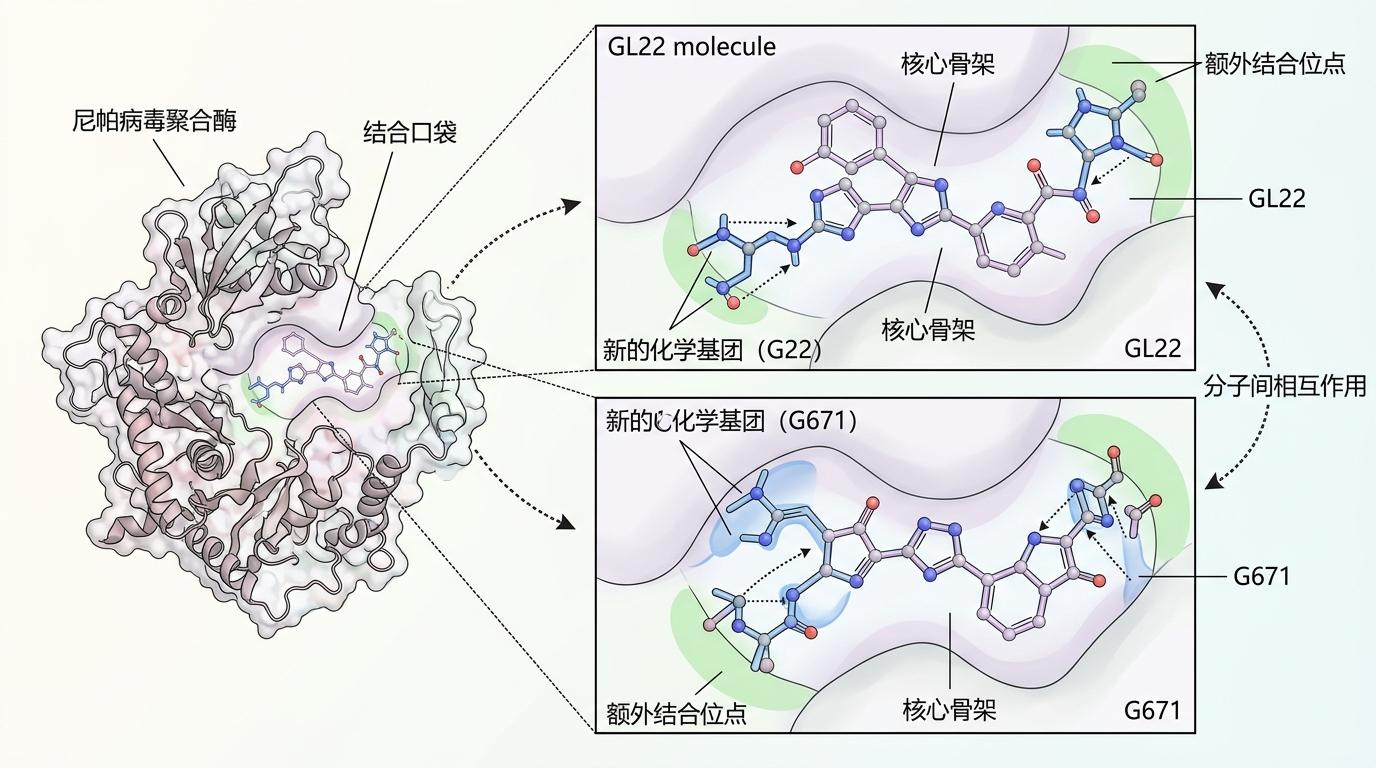
实验结果印证了设计的精准:GL22对尼帕病毒聚合酶的结合亲和力提升了数倍,而G671的表现更为突出——它对活尼帕病毒的抗病毒效力,比原药ERDRP-0519提升了近百倍。这就像把原本勉强能拧动的钥匙,改造成了完全匹配的专用钥匙,一插进去就能牢牢锁住病毒的复制机器。
更重要的是,这种改造不是碰运气的试错,而是基于原子级结构的精准操作。过去开发抗病毒药物,可能需要筛选成千上万种化合物,成功率不足万分之一;而现在,结构生物学就像给科学家安了一双“透视眼”,让他们能直接在分子层面“打磨”药物。
不过,这款新药物距离成为尼帕病毒的“特效药”,还有很长的路要走。
首先是安全性和有效性的验证。目前的实验还停留在细胞和动物层面,要进入临床试验,还需要证明它在人体内的安全性,以及能真正降低患者的死亡率。其次是病毒的耐药性风险——尼帕病毒的聚合酶可能会通过突变改变口袋的形状,让新药物再次失效。研究团队已经在实验室中发现了可能的耐药突变位点,这意味着未来的药物可能需要组合使用,或者持续迭代。
更现实的挑战是可及性。尼帕病毒的主要流行区是南亚的低收入国家,一款新药如果价格高昂,最终还是会被挡在病床之外。这也是全球抗病毒药物研发的共同困境:高致死率的病原体往往流行在贫困地区,市场回报有限,导致研发动力不足。
但这次的突破,至少给了人们一个方向:结构生物学正在把抗病毒药物的研发,从“碰运气”变成“精准制导”。
当我们在显微镜下看清病毒聚合酶的原子结构时,我们其实在和自然的精巧博弈中,多了一分胜算。过去,人类对抗病毒只能依赖疫苗和广谱药物,被动等待病毒的“放过”;现在,我们终于能主动拆解病毒的核心机器,针对性地制造“扳手”和“锁具”。
看见结构,才能精准出击。 这不仅是对抗尼帕病毒的关键,也是未来应对所有新发传染病的核心思路。毕竟,在看不见敌人的战场上,我们首先要做的,就是让敌人现出原形。