对抗知识焦虑,从看懂这条开始
App 下载
戳破视网膜薄膜,失明小鼠重见微光
酶消融技术|失明小鼠|约翰·霍普金斯大学|干细胞移植|视网膜内界膜|再生医学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
酶消融技术|失明小鼠|约翰·霍普金斯大学|干细胞移植|视网膜内界膜|再生医学|医学健康
想象一下:把40万个能感光的“视觉种子”注射进失明的眼睛,本该长出新的视觉神经,结果99.99%的种子都卡在了一层看不见的薄膜上,连发芽的机会都没有——这就是过去干细胞治疗视神经病变的真实困境。直到约翰·霍普金斯大学的团队把目光对准了这层叫视网膜内界膜(ILM)的薄膜:它本该是视网膜的“防护墙”,成年后却成了细胞移植的“拦路虎”。当他们用酶轻轻溶开这层膜的一角,奇迹发生了。
你可以把视网膜想象成贴在眼球内壁的“感光胶片”,而视网膜内界膜就是胶片最外层那层薄得几乎看不见的保护膜——它由胶原蛋白和糖蛋白编织而成,厚度只有0.4到1.4微米,比头发丝细100倍。在胚胎发育时,它是引导神经细胞“安家落户”的“导航牌”;但成年后,它的主要任务就变成了“站岗”,把视网膜和眼球里的玻璃体隔开,同时也把外来的细胞、病毒甚至药物都挡在外面。
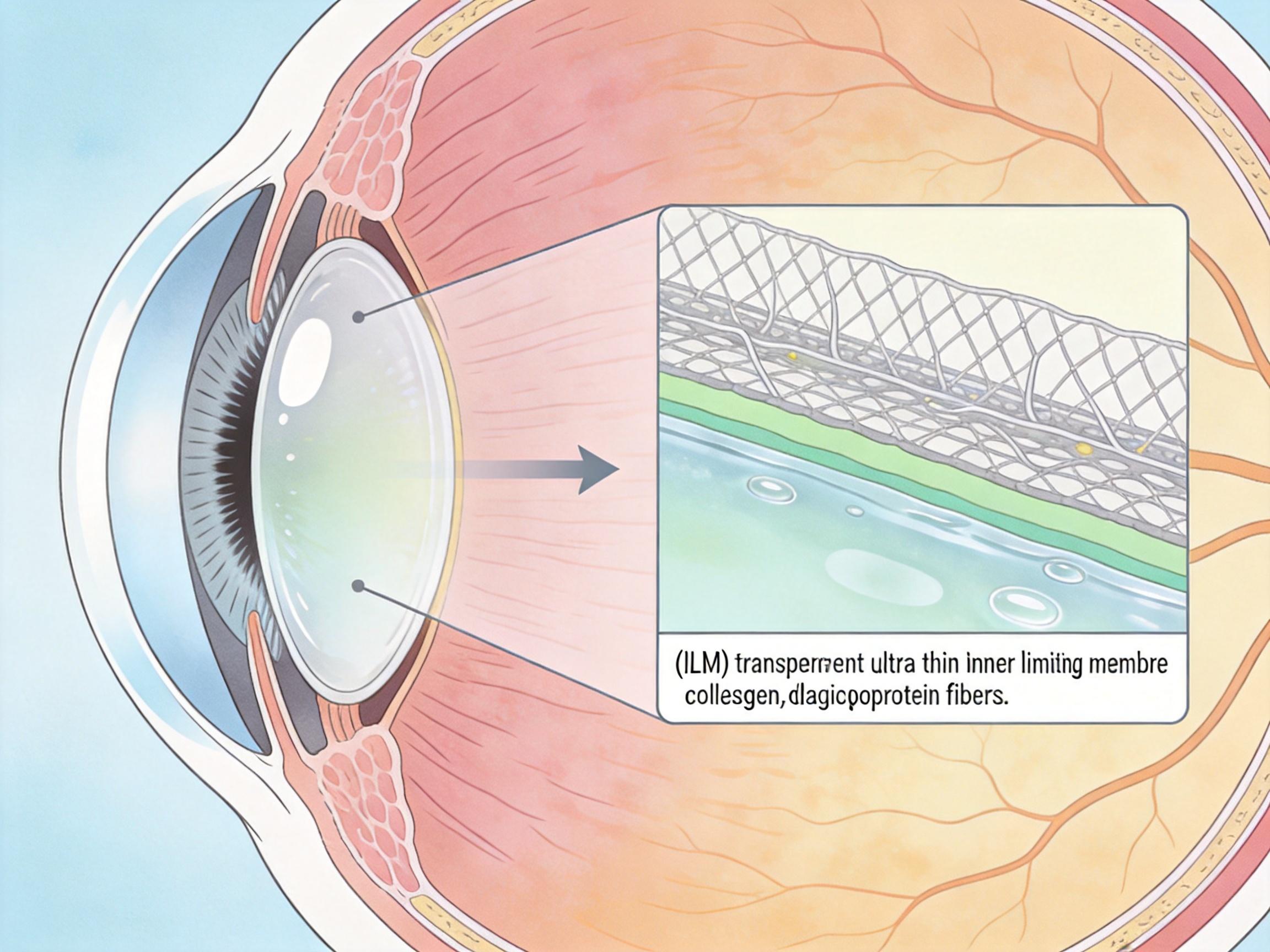
这层膜的“尽责”恰恰成了治疗的死穴。当医生把干细胞培养的视网膜神经节细胞注射进玻璃体,这些本该钻进视网膜深处的细胞,全被这层膜牢牢挡在外面,要么死亡,要么抱团堆积,连0.01%的细胞都没法长出连接大脑的神经突起。
研究团队做了三组对照实验:给天生内界膜发育不全的小鼠注射细胞,给用酶溶开部分内界膜的小鼠注射细胞,再给内界膜完整的小鼠注射细胞。结果让所有人意外:
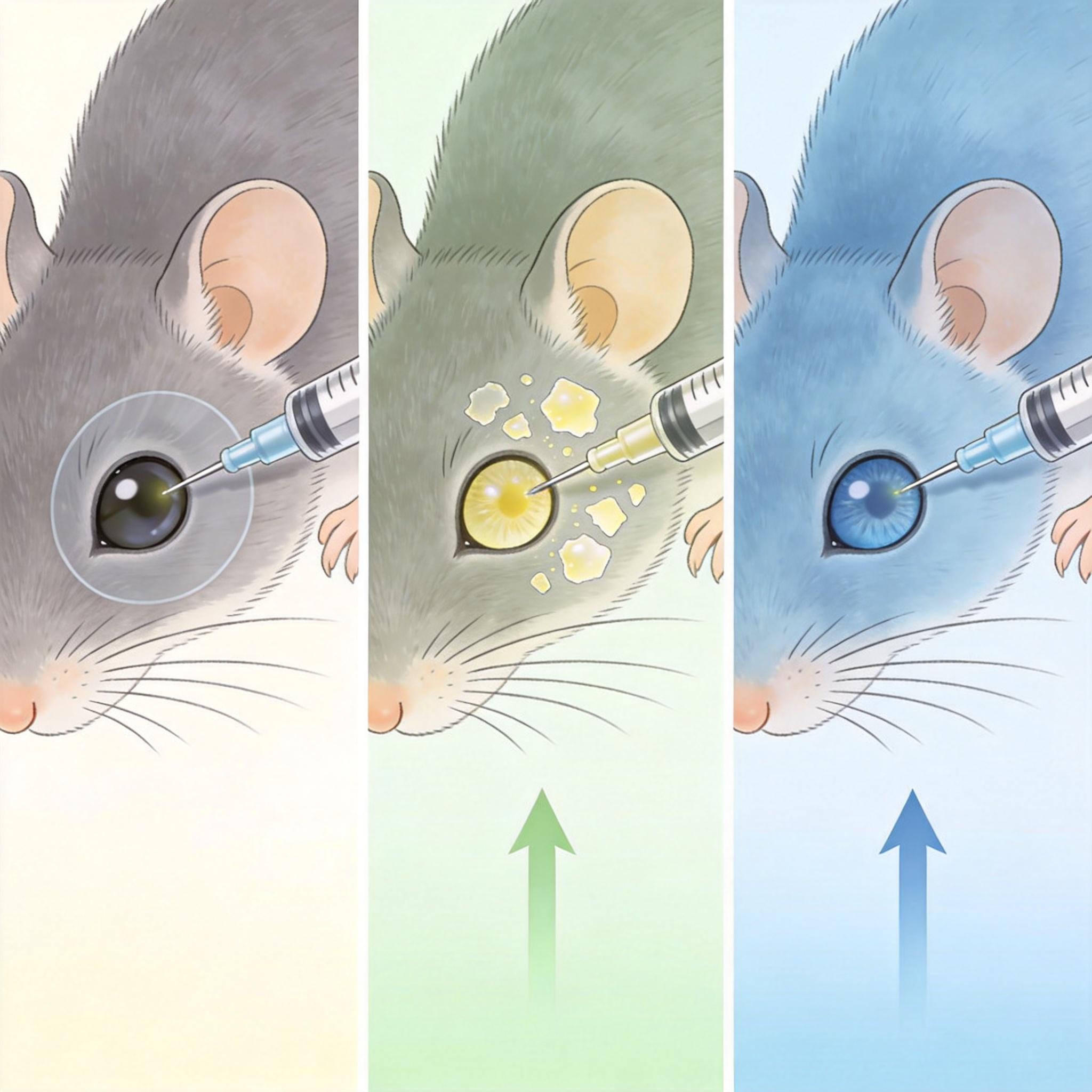
更关键的是,这些成功“安家”的细胞真的能工作了。在行为学测试中,原本对光线毫无反应的失明小鼠,开始会避开强光——它们真的通过移植的细胞,重新感受到了光。
当然,这还不是能直接用于人类的成熟疗法。目前的研究还停留在动物实验和人体视网膜组织的体外测试阶段,要走进临床,至少还要闯三道关:
第一关是精准度。内界膜不能全拆,它毕竟还有维持视网膜结构的作用,必须像用针戳破窗户纸一样,只在需要的地方开小孔。现在的酶解法还不够精准,未来可能要用上光生物技术——用激光配合光敏剂,在膜上打出大小可控的微孔。
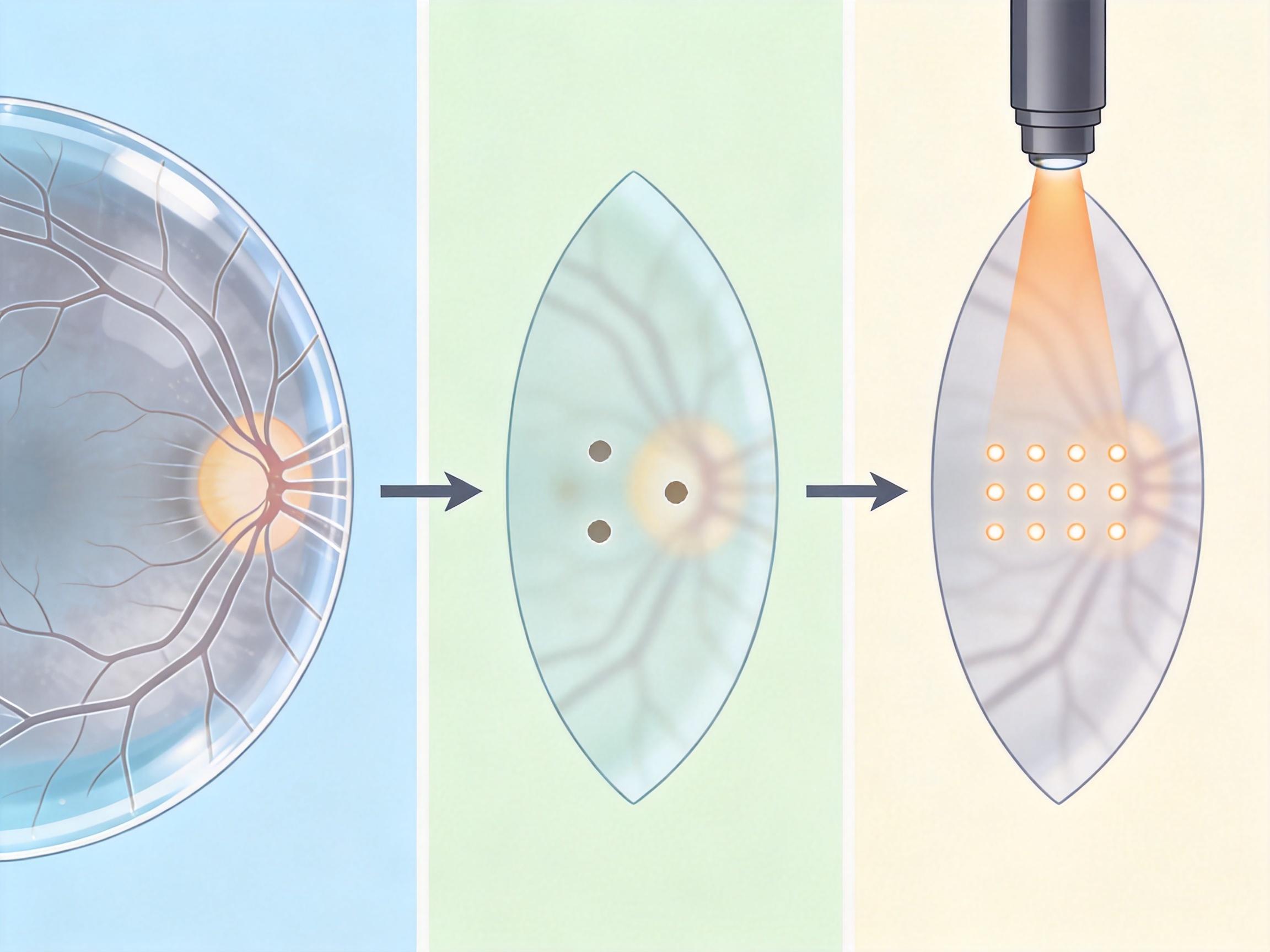
第二关是安全性。酶会不会损伤视网膜其他细胞?拆膜后会不会引发炎症?这些都需要在非人灵长类动物身上做长期观察。目前的实验显示,低剂量酶处理不会造成视网膜损伤,但长期影响还未知。
第三关是细胞成熟度。现在只有2%-7%的移植细胞能完成功能整合,剩下的大部分还是“半成品”,怎么让更多细胞长出正确的神经连接,直接决定了未来患者能恢复多少视力。
对于那些因为青光眼、视神经炎而彻底失去视力的人来说,这层薄膜的突破,是黑暗里透出的第一缕微光。过去我们总想着怎么培养出更完美的干细胞,却忘了最关键的障碍,可能只是一层看不见的“窗户纸”。
有时候,医学的突破不是创造新东西,而是拆掉那些不该存在的“墙”——这层挡在光明和黑暗之间的薄膜,终于要被戳破了。