
3 个月前

3 个月前
细胞膜上,成百上千个GPCR像一排排插口,决定细胞如何听见世界。我们看得见它们,却对近四分之一“孤儿受体”的钥匙一无所知:它们究竟在感知什么?当饥饿、寒冷或激素风暴来临时,谁在敲门?
2026年,来自北京脑科学与类脑研究所、北京大学与中国农业大学的联合团队,在Nature Chemical Biology在线发表成果:首次用“光交联辅助解孤”平台,在接近生理条件下捕获到孤儿受体GPR50的内源性配体——神经肽L-LEN,并在小鼠体内证明这对“受体–配体”是能量代谢与体温调控的关键开关。方法学的要义很直白:把受体与配体那次极短的相遇,定格为可分析的共价整体。审稿人称其“实现了GPCR研究者长期以来的梦想”,同期评论直言这束光或将点亮更多暗区。那么,这盏灯能照多远?
2019年,年轻的课题组负责人井淼抛出一个朴素判断:解孤的核心不是扩大筛库,而是保留真实发生的受体–配体互作本身。他与化学家陈鹏一拍即合——把可光激活的非天然氨基酸DiZPK像坐标钉一样,遗传编码到GPCR的结合口袋;紫外光一闪,近距离接触的分子被“粘”在一起,随后交给质谱去读档。团队先在已知受体–配体(如NPY–NPY1R)上打样,证据漂亮。但当把爪子伸向代谢相关的GPR50时,麻烦来了:成熟神经肽在传统蛋白酶切里“隐身”。研究者转身换刀,直接用交联肽搜索算法pLink2去找“拼在一起”的证据,L-LEN跃然纸上。技术的胜利,故事才刚开场。
这套平台的三个关键点:
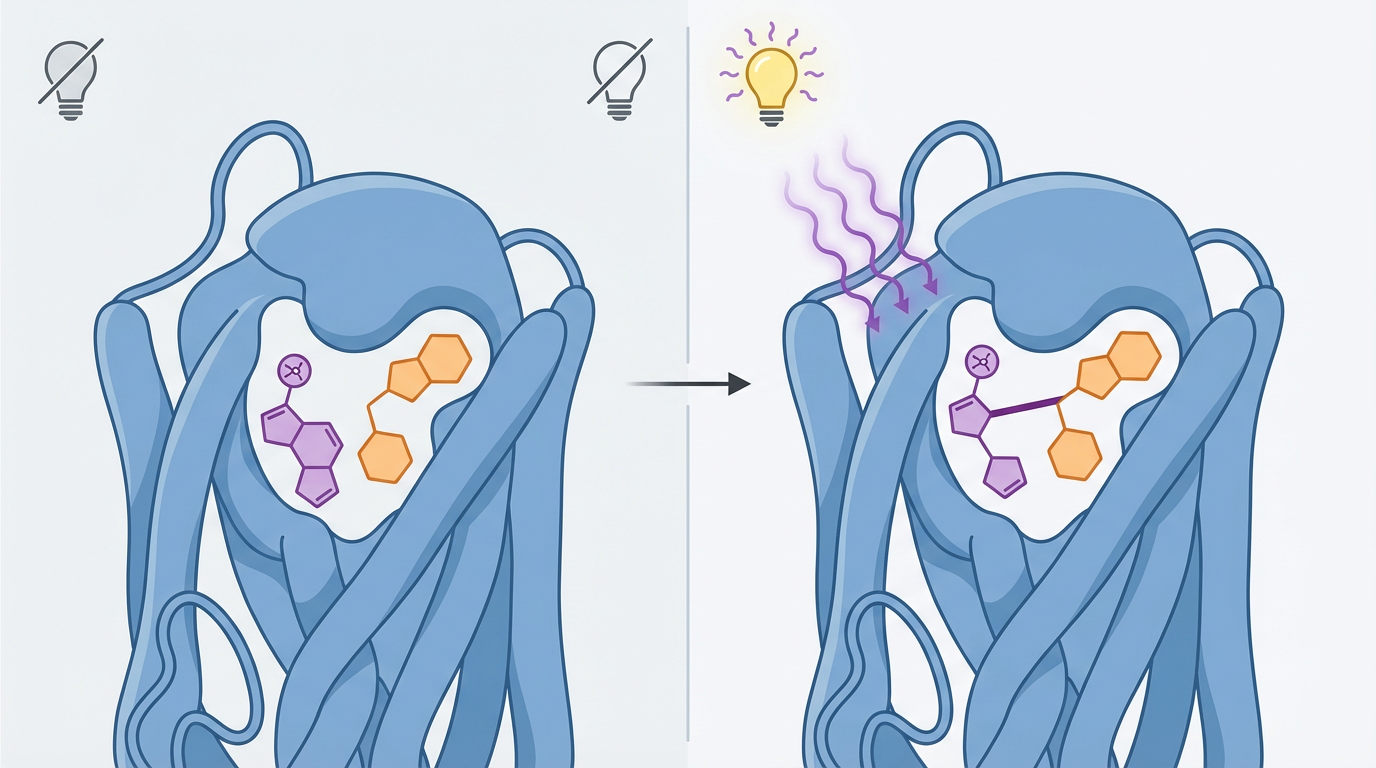
团队没有把“配上对象”当终点,而是追到小鼠体内:
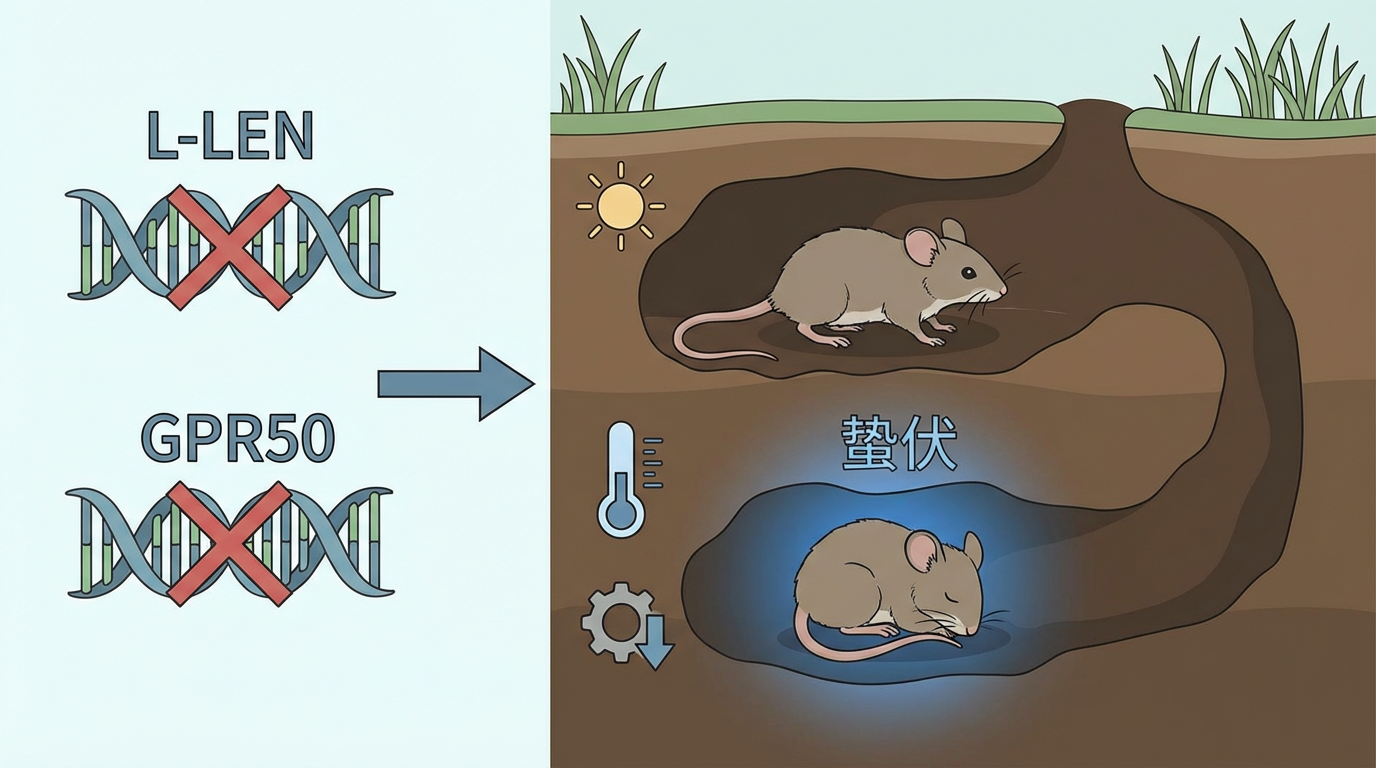
这束光并非孤例。黏附类孤儿受体ADGRD1/ADGRF1被解析出“stalk”自激活机制,脂质LPC还能作别构调节;中枢受体GPR88的结构揭示独特变构位点与可能的脂质样内源配体;GPR39被证实能响应特定胆汁酸,连接到急性胰腺炎的分子根由。不同学科的灯光——光化学、冷冻电镜、交联质谱、计算与筛选——在同一块功能暗区交叠,勾勒出“配体类型更杂、激活方式更多、调控位点更分散”的新地形图。地图渐清,但通往药物的路,哪一条最稳?
可以预见的路线图:
这项工作让人记住两句话:把瞬间变成证据,把证据带回体内。孤儿GPCR的解孤,不只是为药物找新靶点,更是在生命复杂网络里寻找可以被人类温柔干预的按钮。当功能暗区被一点点点亮,我们对“何为健康”的理解,也在被悄悄改写。故事未完,但方向已定。
点击充电,成为大圆镜下一个视频选题!