
1 个月前

1 个月前
当医生给银屑病患者注射抗IL-17药物时,多数人的红斑会慢慢消退,但总有一部分人,皮疹会在几个月后重新爬满四肢。这种「疗效衰减」像个挥之不去的阴影——我们明明瞄准了银屑病的「核心靶点」IL-17,为什么炎症还是会卷土重来?
中山大学的研究团队最近在皮肤上找到了答案:一种叫NMI的分子,正在偷偷给Th17细胞「加油」,让它们源源不断分泌IL-17,就算直接阻断IL-17,只要NMI还在,炎症的火苗就灭不干净。更关键的是,这种分子就藏在患者的皮损里,和IL-17的水平几乎同步飙升。
你可以把NMI想象成细胞受伤后发出的「SOS信号弹」——它本来是细胞内的调控蛋白,当细胞被炎症损伤或感染时,会被主动释放到细胞外,变成一种叫DAMP的「危险信号分子」。DAMP就像免疫系统的警报器,一旦被免疫细胞的受体识别,就会触发炎症反应,召唤更多免疫细胞来「救火」。
但自然不在乎我们的假设。
这次发现的NMI,不仅是个「警报器」,更是个「纵火犯」。它会直接找到Th17细胞表面的TLR4受体——相当于撬开了Th17细胞的「油门」,激活细胞内的NF-κB信号通路,让Th17细胞疯狂分泌IL-17A和IL-17F。更麻烦的是,NMI还会让Th17细胞变得更「顽固」,就算没有IL-23的维持,也能保持高度活跃的促炎状态。
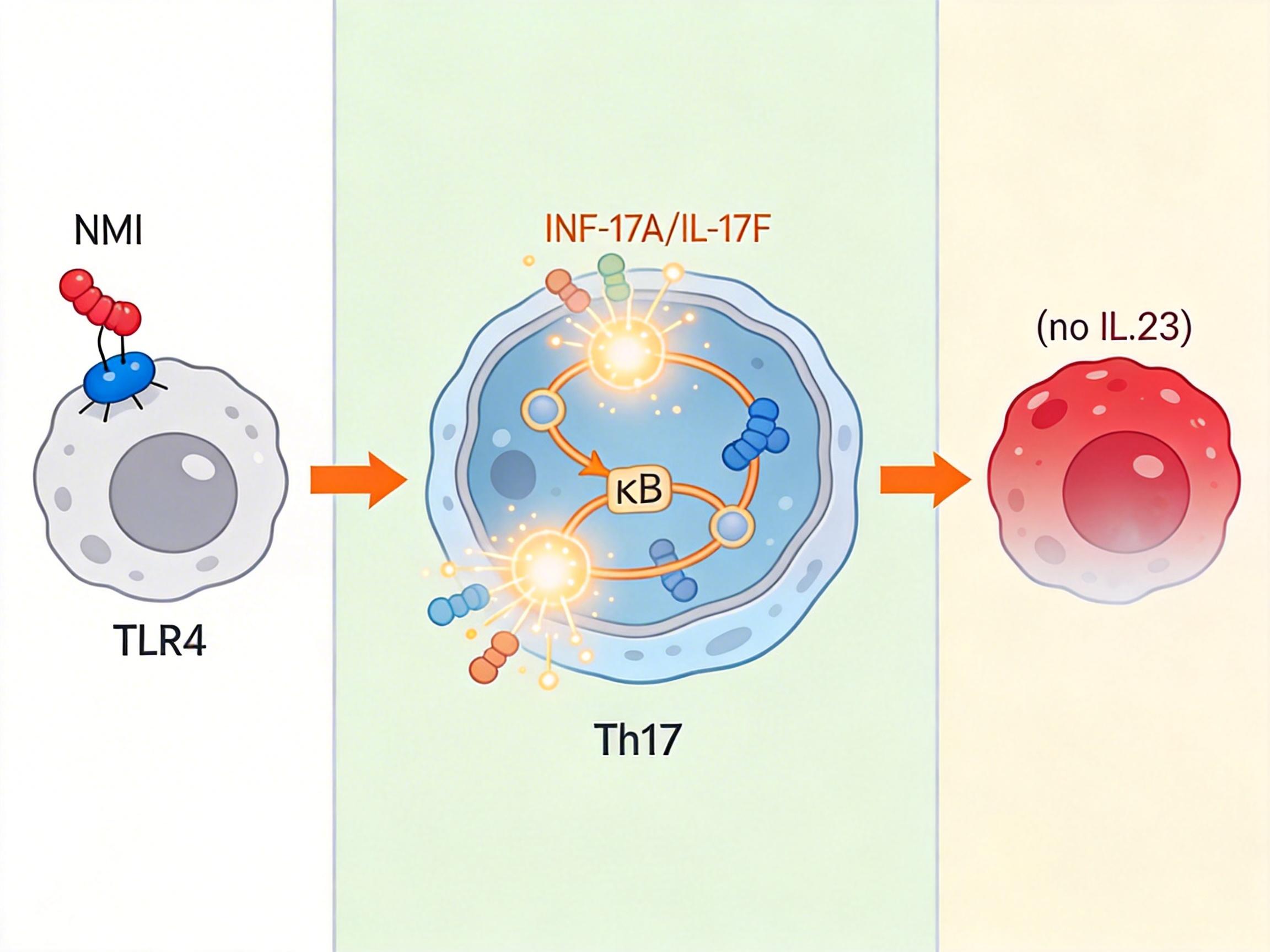
实验室里的实验直白得像在给答案:把NMI基因敲除的小鼠做成银屑病模型,它们的皮肤红斑变薄了80%,IL-17的水平直接降到了正常小鼠的1/5;而给正常小鼠注射NMI蛋白,原本轻微的皮疹会在3天内变得红肿增厚。
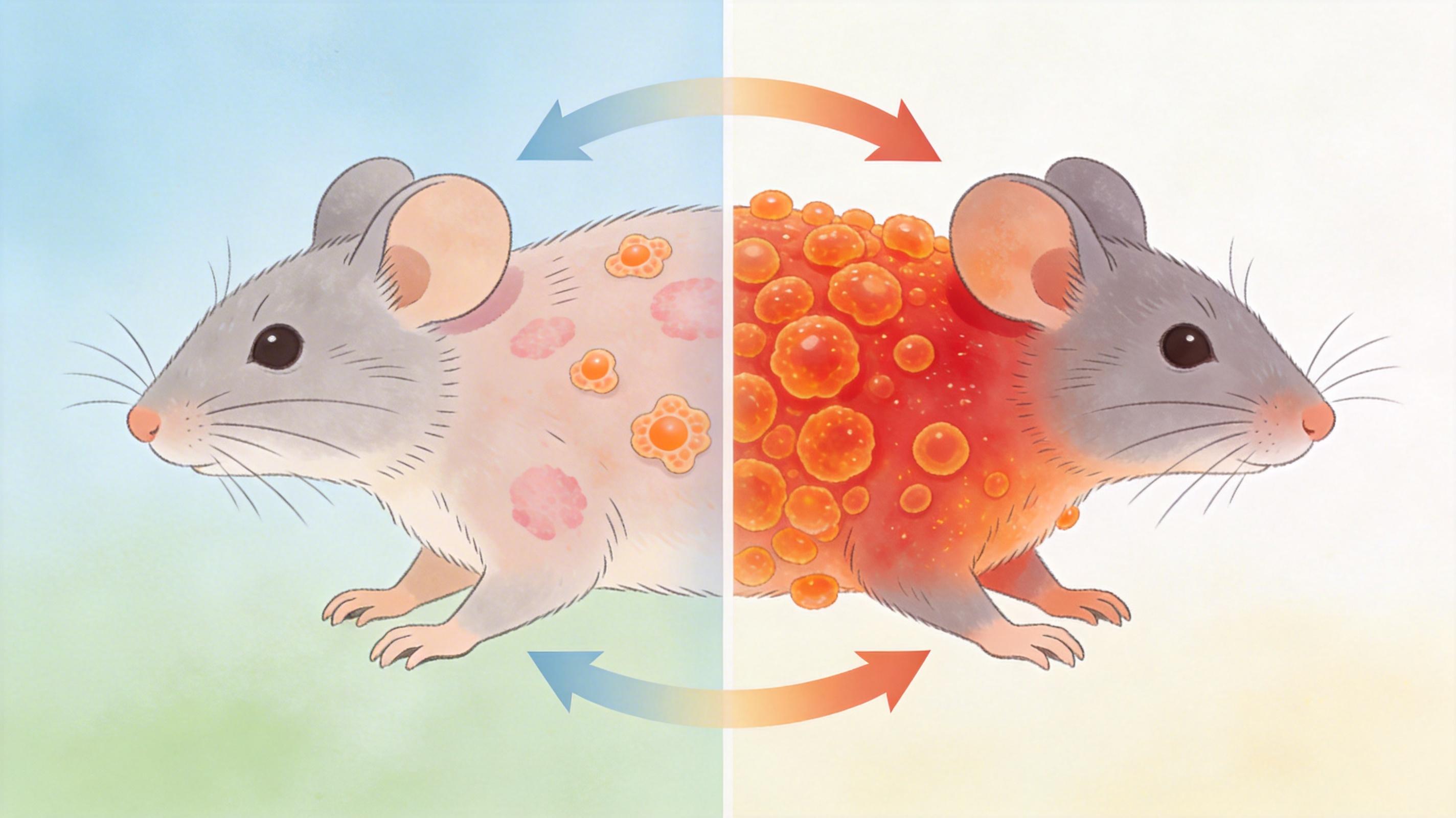
现在的银屑病治疗,几乎都盯着IL-23/IL-17轴——要么阻断IL-23不让Th17细胞成熟,要么直接中和IL-17不让它搞破坏。但问题在于,Th17细胞的「坏心眼」不止这一个:就算IL-17被阻断,它们还能分泌GM-CSF等其他促炎因子,而且长期用药会让Th17细胞产生「耐药性」,慢慢变成更难对付的亚型。
NMI的出现,给了我们一个绕开这个死循环的机会。
研究团队用中和抗体「抓住」小鼠体内的NMI后发现,不仅IL-17的水平降了,Th17细胞的数量也明显减少,就连皮肤里的巨噬细胞和中性粒细胞也跟着「撤退」了。这是因为NMI是在炎症的上游「煽风点火」:它既会激活先天免疫细胞释放促炎因子,又会直接增强Th17细胞的功能,相当于同时掐断了炎症的「燃料」和「发动机」。
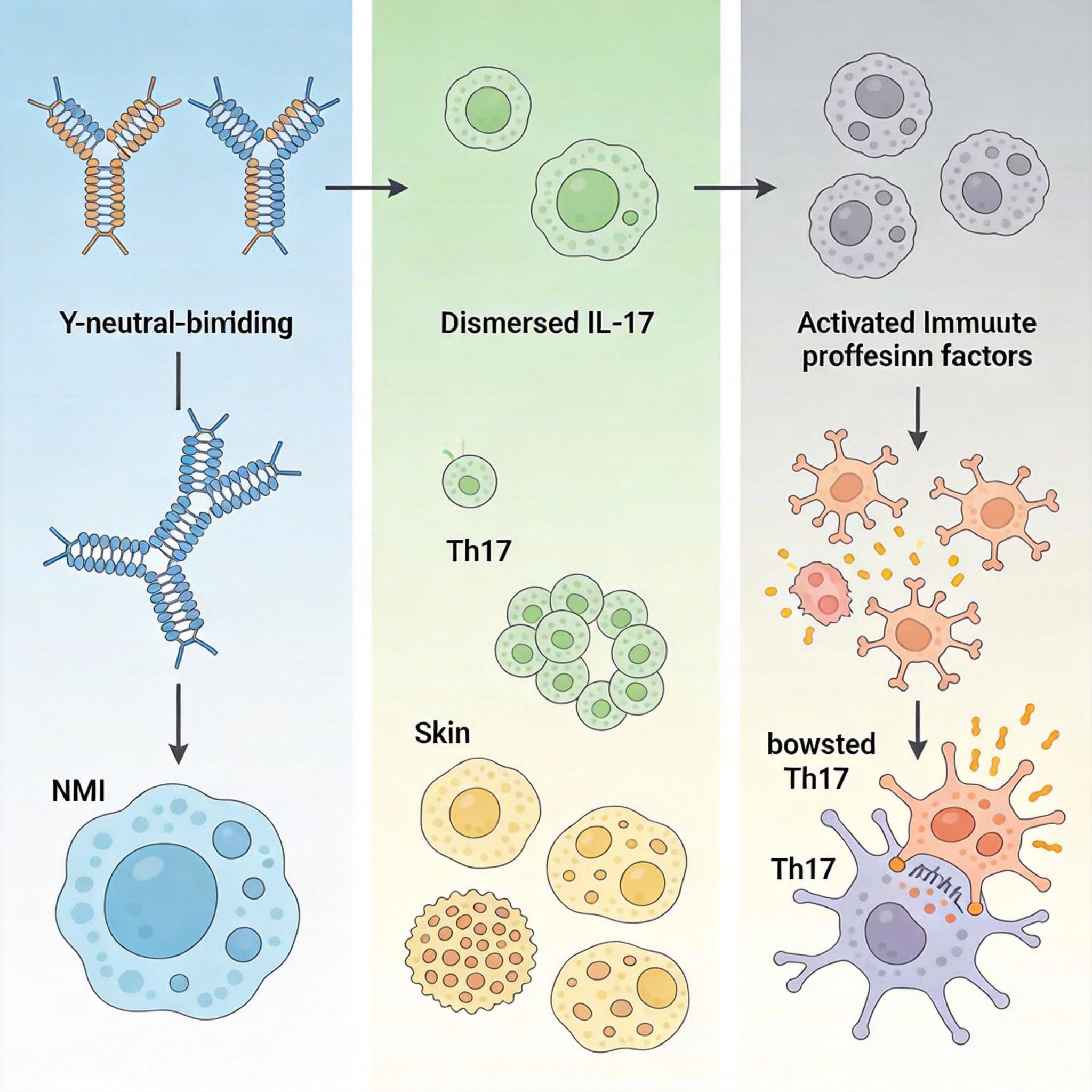
我认为,这才是这项研究最有价值的地方——它不是给现有的治疗方案「补漏」,而是找到了一个能同时调控先天免疫和适应性免疫的节点。相比直接阻断IL-17,靶向NMI可能更接近「釜底抽薪」,从源头减少炎症的复发概率。
当然,现在就说NMI能成为银屑病的「救星」还太早。从实验室的小鼠模型到临床应用,至少还有三道关要过。
第一道是「特异性」关。NMI不仅在皮肤里表达,在肝脏、肺部等器官的炎症中也会出现,如何确保药物只阻断皮肤里的NMI,不会影响其他器官的免疫功能,是个不小的挑战。
第二道是「安全性」关。敲除NMI基因的小鼠虽然炎症减轻了,但在应对病毒感染时,它们的干扰素反应会变慢——这说明NMI在抗病毒免疫中也有作用。长期阻断NMI会不会增加感染风险,还需要更多动物实验和临床数据来验证。
第三道是「精准性」关。银屑病有不同的亚型,比如斑块型、脓疱型、红皮病型,NMI在这些亚型中的表达水平是否一样?是不是所有患者都能从NMI靶向治疗中获益?这些问题都需要大规模的临床样本研究来回答。
不过,至少我们已经找到了新的方向。就像之前从TNF-α到IL-17的跨越一样,NMI的发现,让我们对银屑病的炎症网络又多了一层理解。
当我们把炎症拆解成一个个分子信号时,会发现免疫系统从来不是简单的「开关」,而是一张相互交织的网——一个分子的激活,可能会牵动整张网的反应。NMI的发现,就是这张网上的一个新节点,它让我们看到,银屑病的炎症不止有IL-17的「明火」,还有NMI在背后添的「暗柴」。
「治炎先治因,除根先断源」,这不仅是银屑病治疗的方向,也是所有慢性炎症疾病的破局之道。未来的某一天,当医生给患者注射的不再是单纯的抗IL-17药物,而是能同时阻断NMI的联合疗法时,那些反复出现的皮疹,或许就能真正安静下来。
点击充电,成为大圆镜下一个视频选题!