对抗知识焦虑,从看懂这条开始
App 下载
致命融合:肺炎克雷伯菌如何进化为“超级病原体”?
基因融合|高毒力|多重耐药性|超级病原体|肺炎克雷伯菌|感染性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
基因融合|高毒力|多重耐药性|超级病原体|肺炎克雷伯菌|感染性疾病|医学健康
在人类肉眼无法企及的微观世界,一场关乎生存的军备竞赛正以前所未有的速度升级。主角,是一种名为肺炎克雷伯菌(Klebsiella pneumoniae)的细菌。它既是我们肠道中的寻常“居民”,也可能化身为致命的“杀手”。如今,这位昔日的“机会主义者”正通过一场危险的基因融合,加速进化为一种兼具高毒力与多重耐药性的“超级病原体”,向全球公共卫生防线发起了空前挑战。
长期以来,微生物学家对肺炎克雷伯菌的认知存在一条清晰的界线:要么是具备强大耐药性、主要在医院内作乱的经典型(cKp);要么是毒力凶猛、能在社区感染健康人群的高毒力型(hvKp)。前者“铠甲坚厚”但“攻击力”有限,后者“武器锋利”却“防御脆弱”。这种“高毒力但不耐药,耐药但不高毒力”的平衡,曾是人类应对它的重要依据。
然而,这道防线正在崩塌。2024年7月,**世界卫生组织(WHO)**罕见地发布全球警报,指出携带“最后防线”抗生素——碳青霉烯类——耐药基因的高毒力肺炎克雷伯菌ST23型克隆,正在全球多地悄然崛起。欧洲疾病预防与控制中心(ECDC)的报告也证实了这一趋势,一个前所未见的敌人已然出现。
警报的背后,是一项由浙江大学医学院附属邵逸夫医院阮陟研究员团队领衔的突破性研究。他们联合多家机构,通过分析全球超过7万株肺炎克雷伯菌的基因组数据,在国际顶尖期刊《自然·通讯》上揭开了一个惊人的秘密:在欧洲流行的新兴高毒力耐药菌株(ST23-KL57),并非传统高毒力菌株的简单升级,而是一个“混血儿”。
这项研究如同一部基因侦探小说,追溯了这个“超级病原体”的起源。原来,它是一场跨越大陆的基因重组事件的产物。
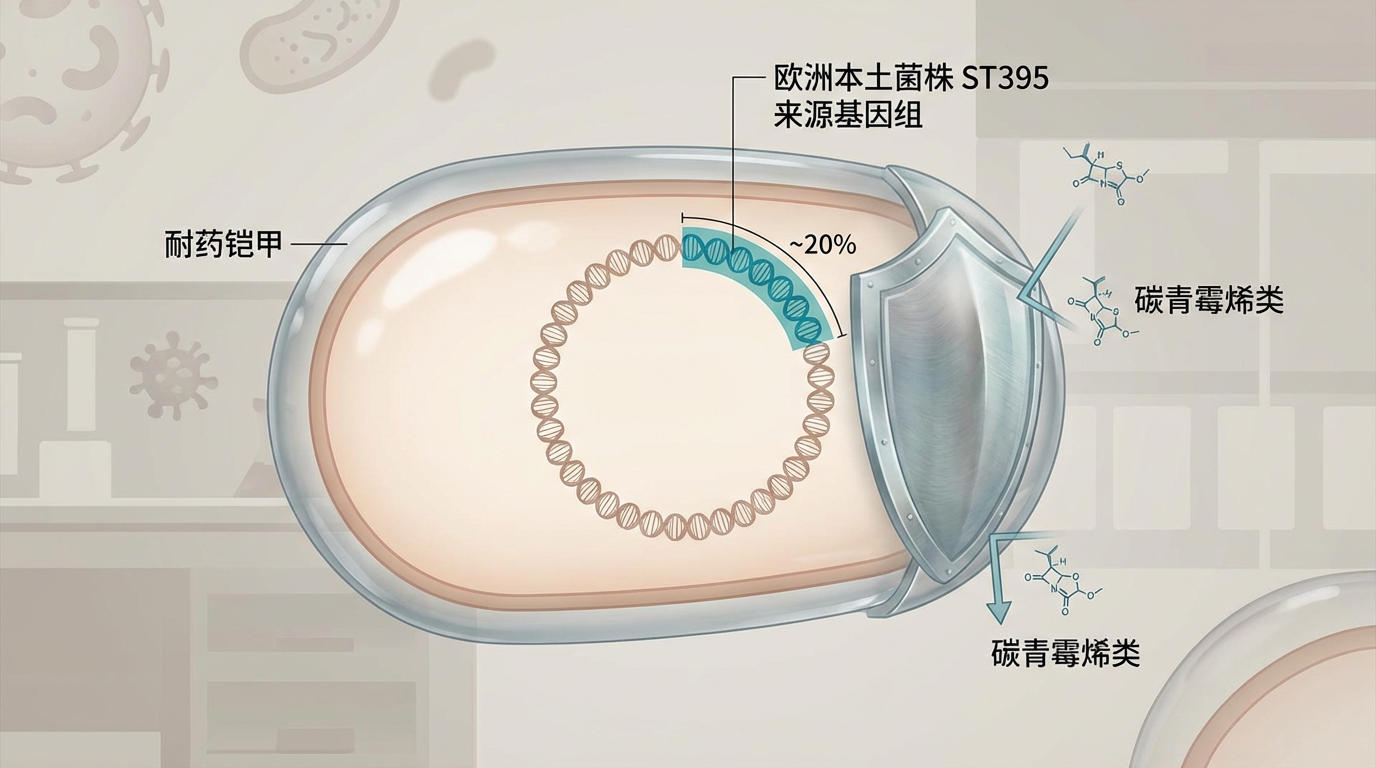
这场在微观世界里发生的“联姻”,催生了一个兼具双方“优点”的危险后代。它既有亚洲菌株的“矛”,又有欧洲菌株的“盾”。更值得警惕的是,研究发现,这个新谱系在获得耐药性的过程中,似乎付出了微小的“适应性代价”——丢失了部分毒力基因簇(iroBCDN)。这表明,在抗生素的持续筛选压力下,细菌正在进行精密的“计算”,以最小的代价换取最大的生存优势。
这场融合得以实现,关键在于细菌世界中一种高效的基因交换机制——质粒介导的水平基因转移。质粒,是细菌染色体之外的环状DNA,如同一个个微小的“基因U盘”,储存着各种生存“软件”,如耐药基因和毒力基因。
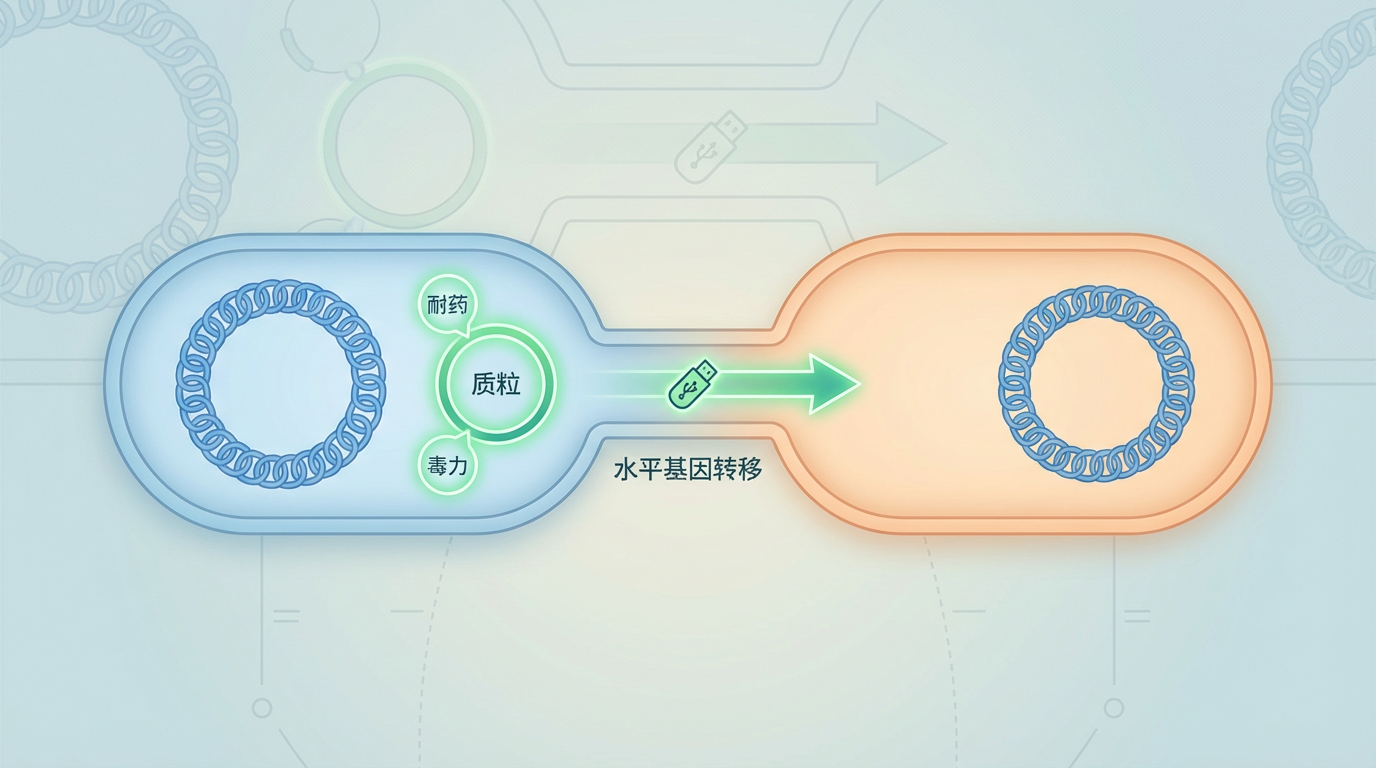
复旦大学华山医院王明贵教授等团队的研究进一步揭示了其中的细节:
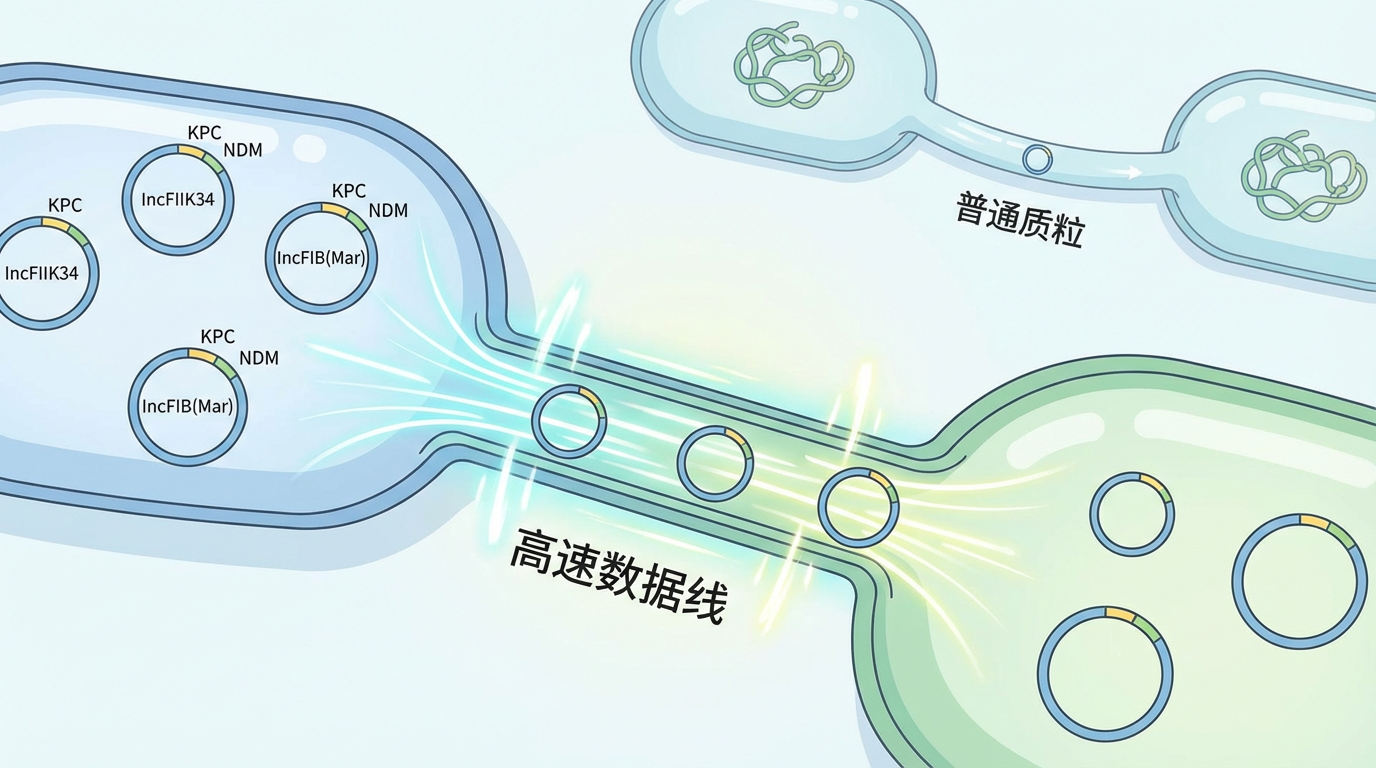
正是通过这种方式,原本“安分”的高毒力菌株获得了耐药武器,而原本“笨拙”的耐药菌株则学会了致命的攻击手段。这种“强强联合”的进化模式,让肺炎克雷伯菌的威胁性呈指数级增长。
这个新生的“超级病原体”并未停留在实验室的培养皿中。WHO的数据显示,截至2024年,全球六大区域中至少16个国家和地区已报告了高毒力肺炎克雷伯菌的存在。中国疾病预防控制中心的研究也表明,高风险的ST23型在我国的检出比例已高于全球平均水平,并呈现显著扩张趋势。
在临床一线,其破坏力触目惊心。在中国,ST11-KL64型已成为院内感染的优势克隆,部分ICU暴发的耐碳青霉烯高毒力肺炎克雷伯菌感染,病死率高达100%。它不再局限于免疫力低下的住院患者,甚至能感染健康的社区人群,使得感染防控的边界变得模糊,挑战巨大。
面对这个加速进化的敌人,人类并非束手无策。一场围绕诊断、治疗和预防的科技攻坚战已经打响。
精准诊断:传统的“拉丝试验”已无法满足需求,基于基因测序的分子诊断技术正成为主流,能快速识别菌株的“身份”(序列分型)和“装备”(毒力与耐药基因),为精准治疗提供依据。
创新疗法:
肺炎克雷伯菌的致命融合,是抗生素滥用驱动下微生物进化的一个缩影。据统计,2021年全球与细菌耐药相关的死亡人数已高达471万。这场人与细菌的战争,远未结束。
从实验室的基因测序到病床前的精准用药,从“同一个健康”(One Health)理念的推行到全球监测网络的构建,应对“超级病原体”的威胁,需要基础研究、临床医学、公共卫生乃至社会各界的协同作战。这不仅是一场科学的较量,更是一场关乎人类未来、需要全球共同参与的持久战役。