对抗知识焦虑,从看懂这条开始
App 下载
马尔堡比埃博拉致命3倍,秘密藏在这把钥匙里
明尼苏达大学|病毒糖蛋白|冷冻电镜|埃及果蝠|马尔堡病毒|感染性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
明尼苏达大学|病毒糖蛋白|冷冻电镜|埃及果蝠|马尔堡病毒|感染性疾病|医学健康
1967年德国马尔堡的实验室里,几名接触过非洲绿猴的工作人员突然倒下——高热、出血、器官衰竭,短短几天内7人死亡。这种后来以城市命名的病毒,在半个多世纪里累计制造了563例感染,夺走409条生命,致死率高达73%,是埃博拉病毒的1.6倍。更恐怖的是,它的自然宿主埃及果蝠,每晚都会飞到人类聚居区的果树上觅食,病毒就潜伏在它们的唾液和粪便里。半个世纪来,科学家始终卡在一个问题上:同样是丝状病毒,马尔堡凭什么比埃博拉更致命?直到明尼苏达大学的团队用冷冻电镜,拍下了它入侵细胞的关键瞬间。
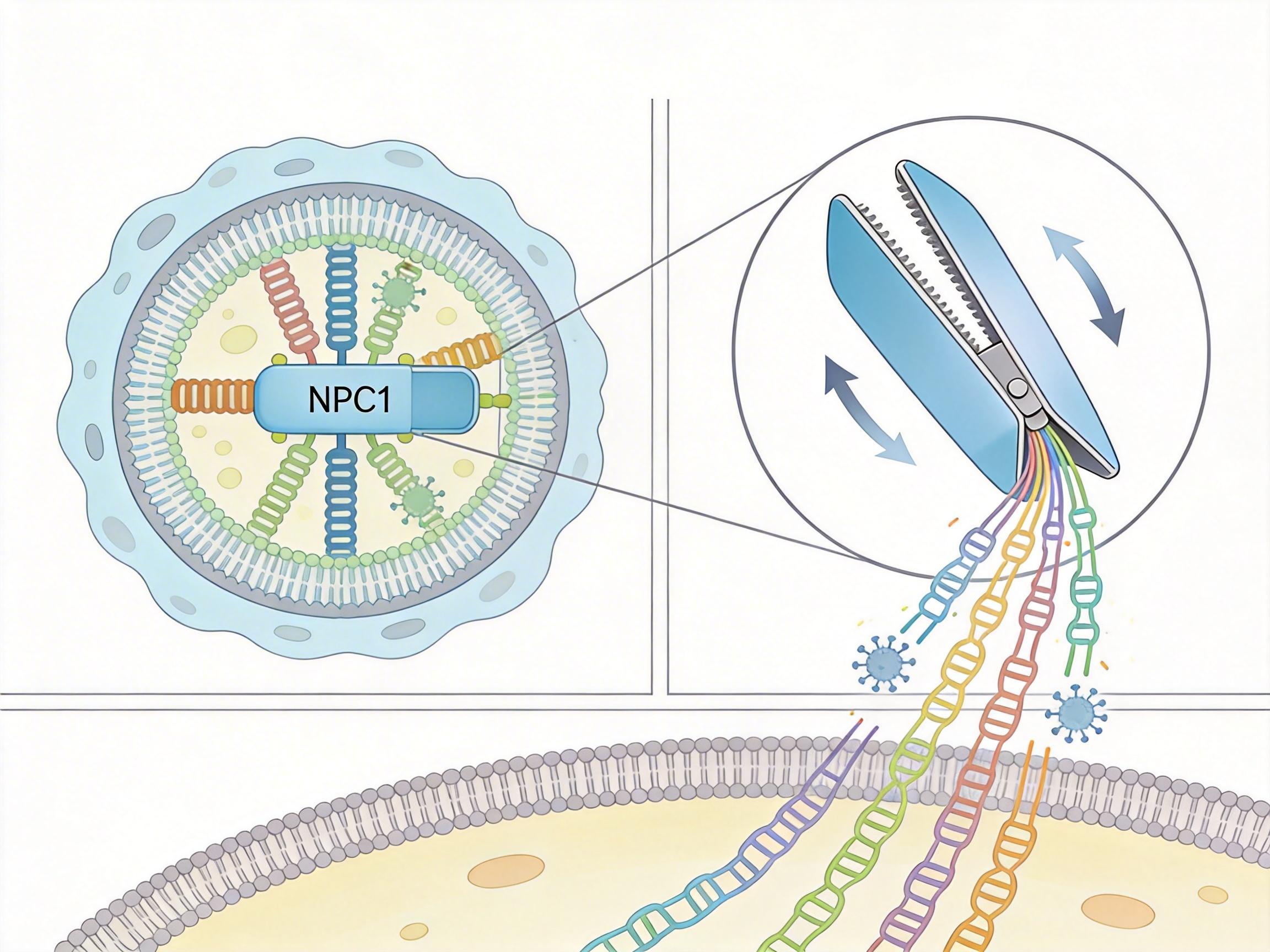
病毒入侵细胞,本质是“钥匙开钥匙孔”——病毒表面的糖蛋白(GP)是钥匙,人类细胞内的NPC1蛋白是锁孔。但这把钥匙藏得极深:先是被一层叫“聚糖帽”的糖链包裹,像钥匙套了个塑料壳;就算聚糖帽被溶酶体里的蛋白酶切掉,马尔堡病毒的钥匙上还留着个9氨基酸的小环,死死盖住最核心的齿纹。
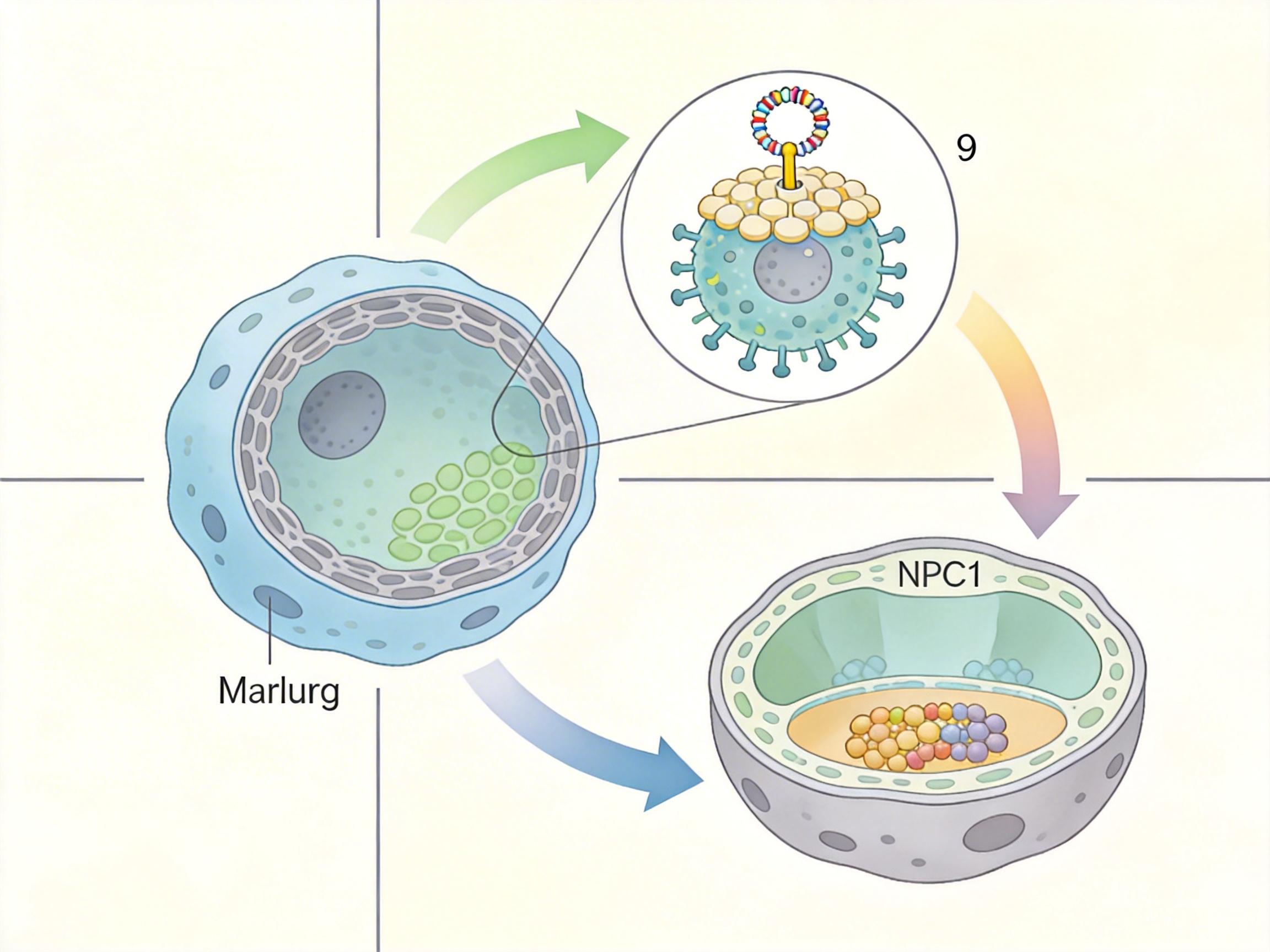
过去科学家以为,埃博拉的聚糖帽是严丝合缝的,而马尔堡的是松散的——这解释了为什么马尔堡更容易被抗体识别。但冷冻电镜的图像推翻了这个假设:马尔堡的聚糖帽其实是半紧半松的,既能在血液里躲避免疫系统的扫描,又能在进入溶酶体后快速脱落,露出钥匙齿纹。
这是一种精妙的平衡:既不像埃博拉那样把钥匙捂得太严,耽误开锁效率;也不会完全暴露,被免疫系统直接摧毁。
真正的差距出现在开锁的瞬间。
埃博拉病毒的钥匙插进NPC1锁孔时,只靠两个环结构固定;而马尔堡的钥匙,不仅把这两个环卡得更紧,还多借了NPC1的第三个环当“锚点”——相当于用三只手抓住锁孔,比埃博拉的两只手稳得多。冷冻电镜测量出,这个额外的锚点让马尔堡的结合角度比埃博拉旋转了39度,刚好卡进锁孔最深处。
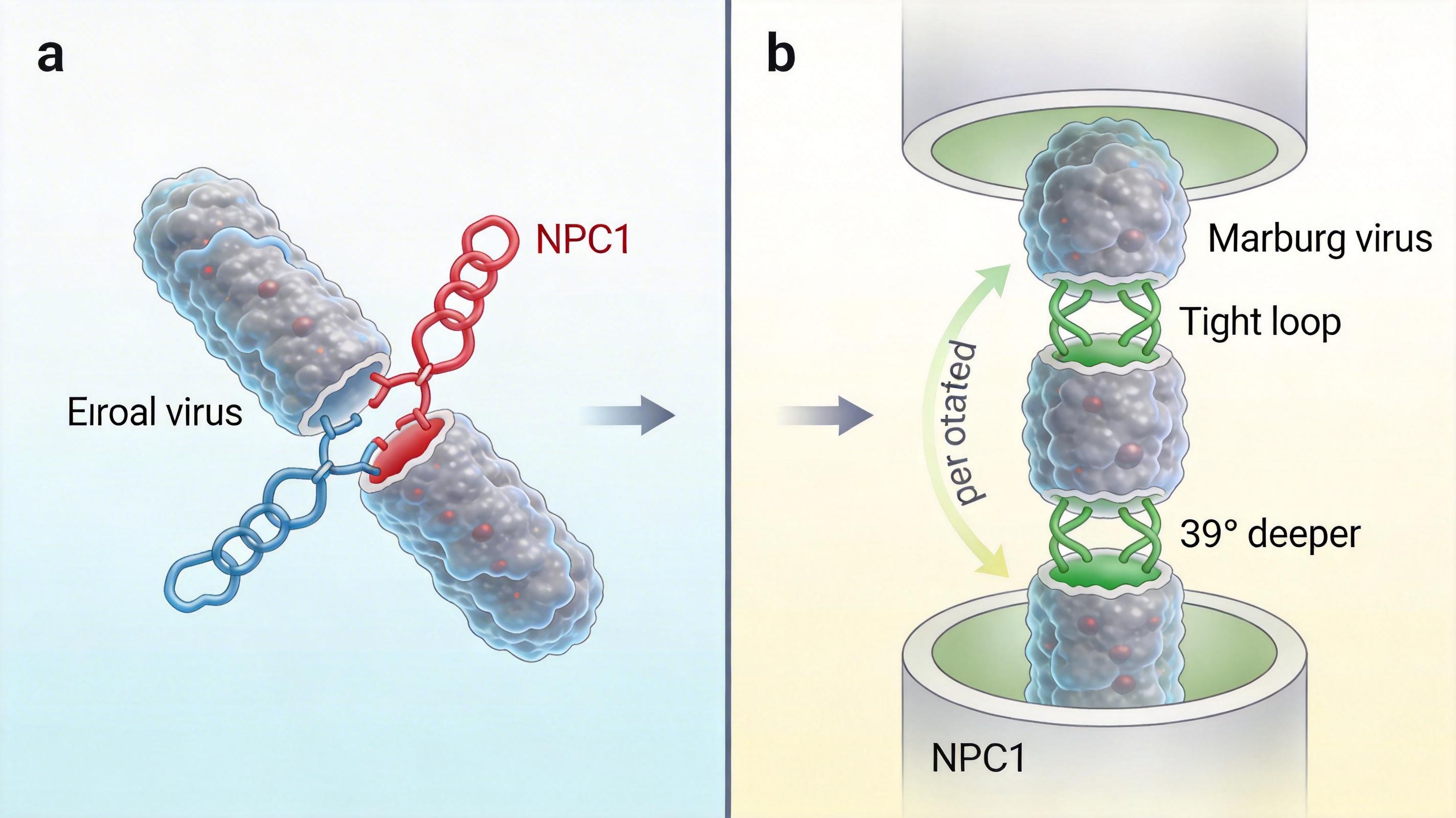
表面等离子体共振实验给出了精确的数字:马尔堡糖蛋白与NPC1的结合力,是埃博拉的11倍。更关键的是,结合后马尔堡的糖蛋白三聚体结构会迅速松散,像打开的折叠刀,直接把病毒的遗传物质送进细胞。
在肝癌细胞、血管内皮细胞和巨噬细胞——这些丝状病毒最爱的靶细胞里,马尔堡的入侵效率是埃博拉的12到300倍。同样100个病毒颗粒,埃博拉只能感染1个细胞,马尔堡能感染300个。
这就是它致死率更高的核心:同样的病毒载量,马尔堡能在更短时间内占领更多器官,让免疫系统来不及反应。
研究团队在解析结构时,意外找到了破解这把钥匙的方法。他们给羊驼注射了马尔堡的糖蛋白,从羊驼的抗体里筛选出一种纳米抗体——Nanosota-MB1。
这个纳米抗体的形状,刚好和NPC1锁孔的结构一模一样,能精准插进马尔堡糖蛋白的疏水凹槽里,比NPC1本身结合得还紧——亲和力高出数个数量级。就像给钥匙孔塞了个橡胶堵头,让病毒的钥匙根本插不进去。
在伪病毒实验里,这种纳米抗体对Ravn株、Musoke株和Angola株这三种主要的马尔堡病毒,半数抑制浓度只有0.5微克每毫升,比之前的人源抗体效果好得多。更重要的是,它的结合位点是病毒高度保守的区域,很难通过变异逃逸。
当我们盯着冷冻电镜下那些原子级的结构时,会突然意识到:病毒的致命性,从来不是什么“邪恶的阴谋”,只是亿万年进化里的一次精准微调——多一个锚点,转一个角度,就能让致死率飙升。
马尔堡病毒的威胁从未远离:埃及果蝠还在非洲的洞穴里群居,每晚准时飞到果园觅食;非洲的矿工仍会钻进蝙蝠栖息的矿井,没有任何防护。但这次结构生物学的突破,终于给了我们一把对抗它的钥匙。
真正的致命,从来不是强大,而是精准。 而人类对抗病毒的终极武器,同样是精准——精准地找到它的弱点,精准地卡住它的命门。