
1 个月前

1 个月前
想象一下:你的免疫系统里有一群“内奸”——它们本该帮身体抵御外敌,却转头勾结其他细胞,持续攻击你的肝脏。这就是自身免疫性肝炎(AIH)的真相:滤泡辅助性T细胞(Tfh细胞),这个本该辅助B细胞产生抗体抗感染的“免疫智囊”,在AIH患者体内彻底失控,疯狂催生攻击肝细胞的自身抗体,最终把肝脏拖入慢性炎症的深渊。
更糟的是,现有治疗只能靠长期吃大剂量免疫抑制剂,要么副作用大到患者撑不住停药,要么最后只能等着肝移植。但2026年3月,山东大学的团队在《Cell Stem Cell》上发表的研究,给了这群“内奸”一个全新的结局——他们直接在患者体内,把叛变的Tfh细胞改造成了守护肝脏的“免疫警察”。这怎么可能做到?
要理解这项技术,得先搞懂Tfh细胞的“双面人生”——正常情况下,它们是淋巴滤泡里的“导师”,引导B细胞生成精准对抗外敌的抗体;但在AIH患者体内,它们会过度激活,像疯长的杂草一样催生大量攻击肝细胞的自身抗体,还会拉着T细胞、树突状细胞一起搞破坏。
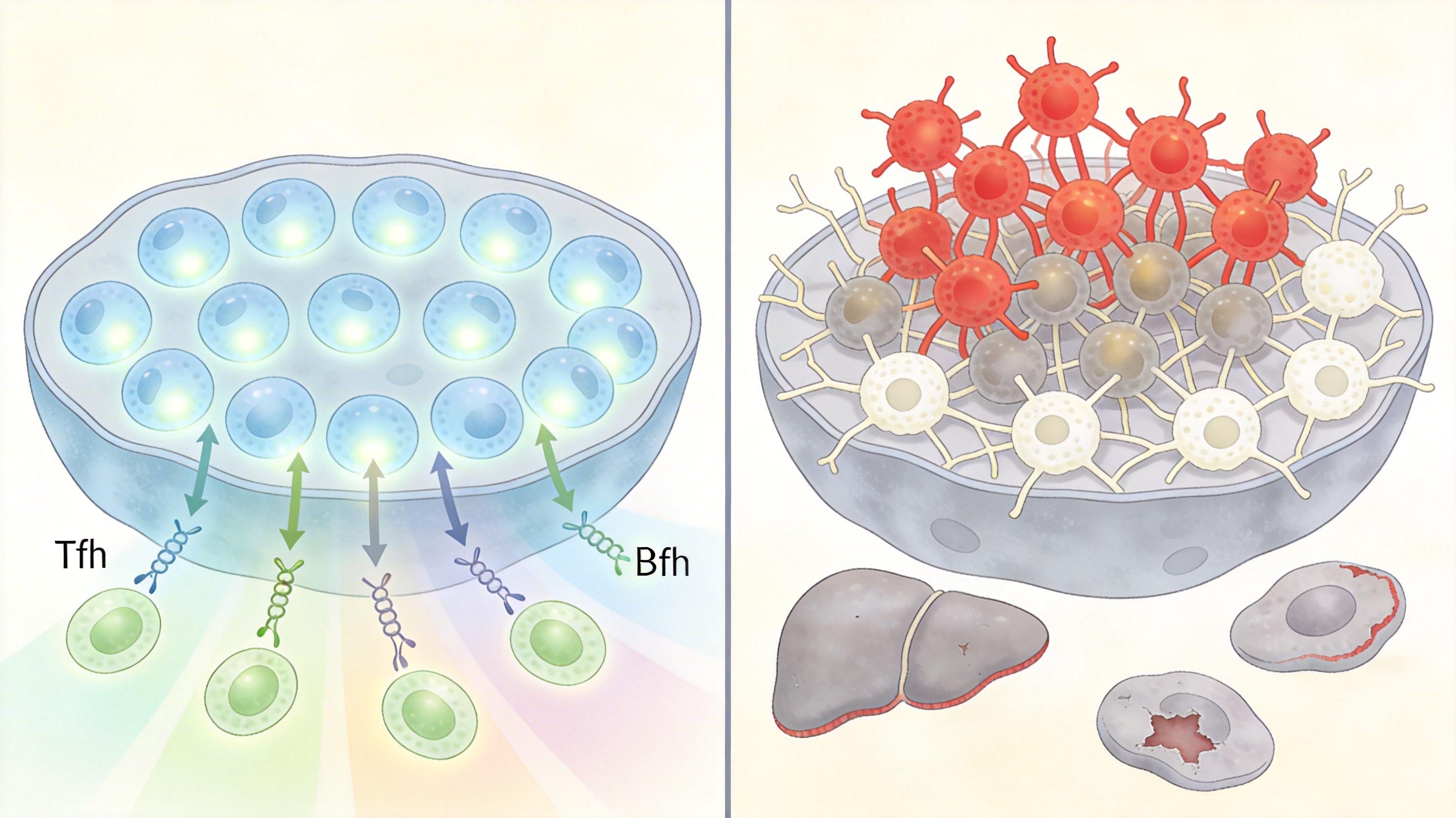
过去科学家想过用CAR-T技术改造调节性T细胞来抑制免疫,但效果总是打折扣——就像只派了一队警察去维持混乱的街区,却没搞定背后挑事的“黑手”。而山东大学团队的思路更直接:既然Tfh细胞是混乱的源头,那干脆把它改造成秩序的管理者。
他们用了一套“纳米快递+基因重编程”的组合拳:
简单说,就是给叛变的Tfh细胞植入了“停止攻击+守护肝脏”的双重指令,让它从纵火犯变成了消防员。
这项技术的厉害之处,在于它不是只搞定了Tfh细胞,而是实现了“一网打尽”式的免疫调节。
在AIH小鼠模型里,被改造后的CAR-Tfh细胞会直接奔赴肝脏战场:它们能精准识别表达CYP2D6的肝细胞,一方面分泌IL-10、TGF-β等免疫抑制因子,叫停正在攻击肝脏的致病性T细胞;另一方面,它们还能抑制过度活跃的B细胞,切断自身抗体的来源;甚至连帮忙递呈抗原、煽风点火的树突状细胞,也会被它们压制。
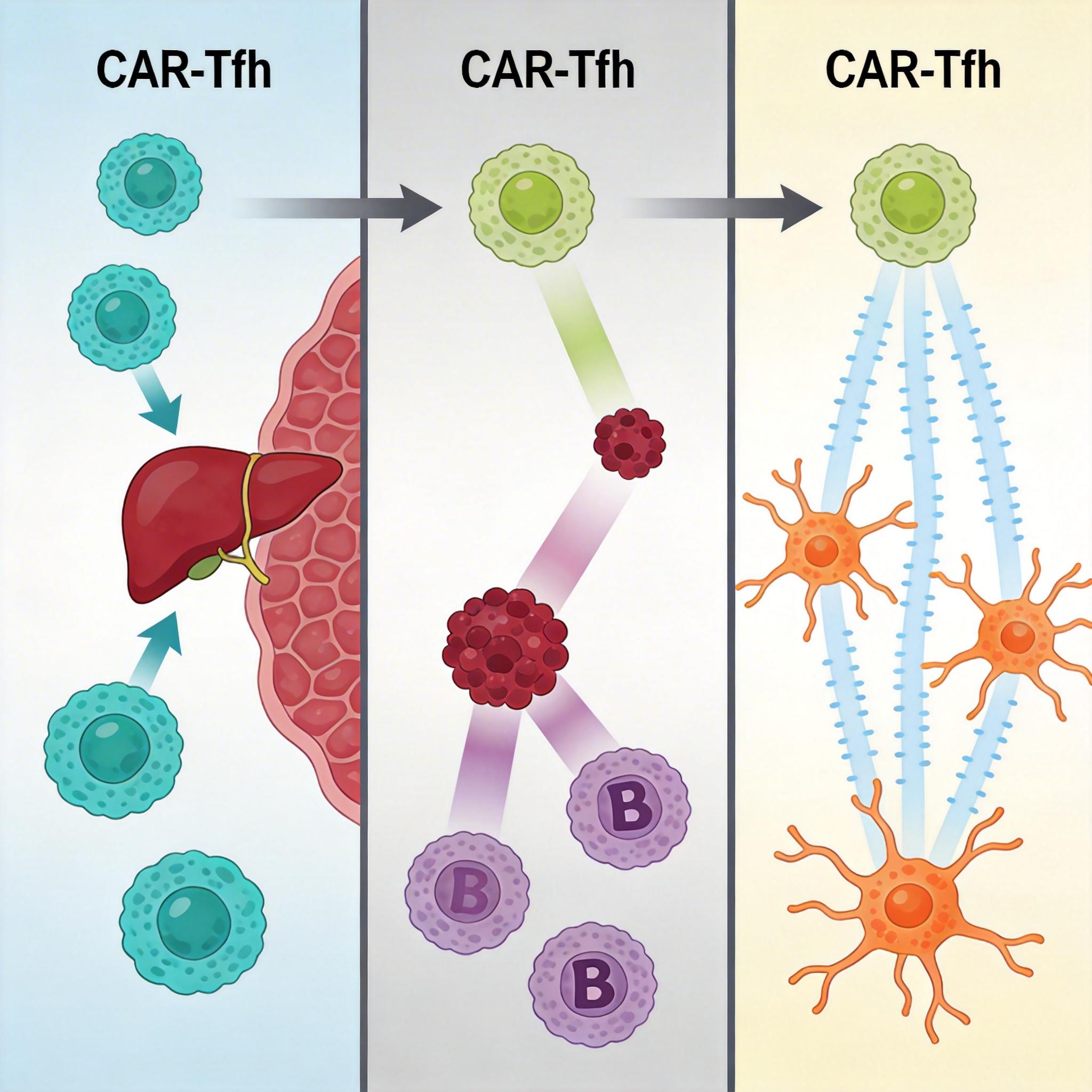
实验数据给出了最直接的证明:接受治疗的小鼠,肝脏里的炎症细胞浸润减少了一半以上,肝功能指标(ALT、AST)降到了接近正常水平,原本疯长的自身抗体也被打回了安全线。更重要的是,这种治疗是“精准打击”——它只针对肝脏里的致病免疫细胞,不会像传统免疫抑制剂那样,把整个免疫系统搞得一团糟,让患者连感冒都扛不住。
我认为,这项研究最被忽略的价值,是它跳出了“单一靶点治疗”的思维定式。过去治疗自身免疫病,要么抑制T细胞,要么清除B细胞,就像拆炸弹只剪一根线,总有漏掉的引信。而CAR-Tfh细胞是一个“多任务处理器”,能同时调控T、B、树突状细胞三个关键免疫群体,从根源上重建肝脏的免疫耐受。
当然,这项技术离真正用于患者,还有几道必须跨过去的坎。
首先是长期安全性。虽然用脂质纳米粒递送mRNA避免了病毒载体的插入突变风险,但Tfh细胞被改造后的稳定性还需要观察——会不会过段时间又变回“内奸”?会不会在体内引发意想不到的免疫反应?这些都需要更长时间的动物实验和临床试验来验证。
其次是递送效率的优化。目前的纳米粒虽然能靶向Tfh细胞,但还做不到100%精准,总有一部分会被其他细胞“截胡”。未来需要给纳米粒装上更精准的“导航系统”,比如针对Tfh细胞表面CXCR5受体的靶向配体,让每一份基因指令都能送到正确的细胞手里。
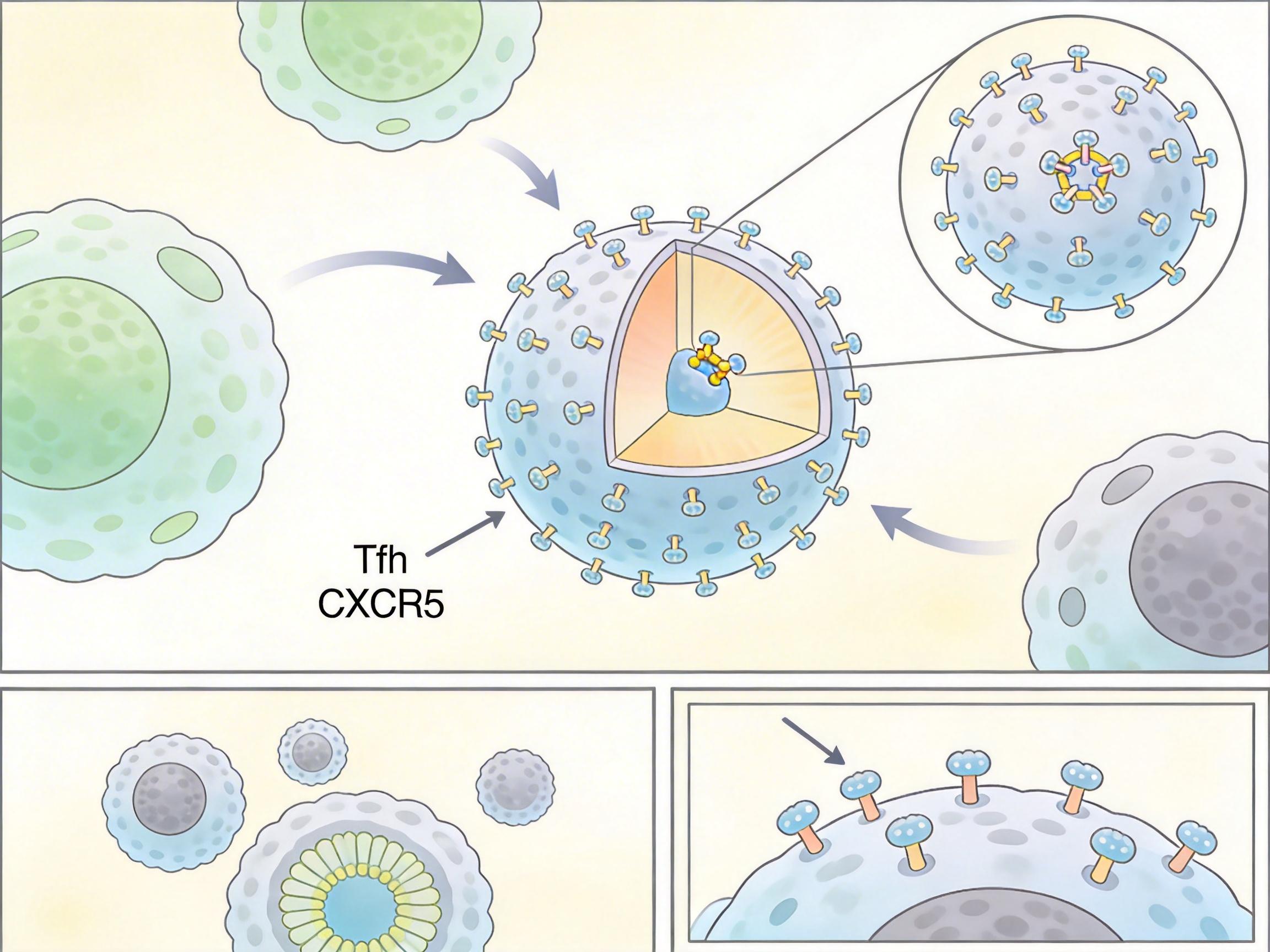
最后是成本和可及性。传统CAR-T疗法因为要体外培养细胞,成本高到普通人用不起,但这项体内重编程技术跳过了体外培养的步骤,理论上能把成本降到原来的十分之一甚至更低。但要实现规模化生产,还需要解决纳米粒的批量制备、质量控制等问题。
不过,这些挑战都挡不住一个核心事实:这项研究给自身免疫病治疗打开了一扇新的大门——与其被动地抑制整个免疫系统,不如主动地把叛变的免疫细胞改造成守护者。
我们总把免疫系统比作忠诚的卫士,却忘了它也可能出现“内部叛变”。自身免疫病的本质,就是免疫系统的“身份识别系统”出了故障,把自己人当成了敌人。
山东大学团队的研究,本质上是给故障的“身份识别系统”打了个补丁——不是粗暴地关掉整个系统,而是精准修正了叛变者的程序。这不仅为AIH患者带来了新希望,更给所有自身免疫病的治疗提供了一个全新的思路:与其对抗,不如转化。
“与其灭火,不如改造纵火者。”这句话或许会成为未来免疫治疗的核心逻辑。当我们学会和自己的免疫系统对话,而不是一味压制它时,那些困扰人类已久的自身免疫病,或许就能找到真正的治愈之道。
点击充电,成为大圆镜下一个视频选题!