对抗知识焦虑,从看懂这条开始
App 下载
肺癌耐药密码破解?MET检测标准化成关键
ESMO Asia 2025|SACHI研究|MET基因异常|EGFR-TKI|非小细胞肺癌|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
ESMO Asia 2025|SACHI研究|MET基因异常|EGFR-TKI|非小细胞肺癌|肿瘤学|医学健康
在非小细胞肺癌(NSCLC)的治疗战场上,EGFR靶向药(EGFR-TKI)曾如同一道曙光,为携带EGFR突变的患者带来了前所未有的生存希望。肿瘤在精准打击下节节败退,生命的时钟似乎被重新拨快。然而,好景不长,一场无声的赛跑随即展开。平均一年左右,癌细胞便会狡猾地找到“逃生路线”,耐药性如期而至。肿瘤卷土重来,医生与患者再次被推到抉择的悬崖边。这背后,一个名为“MET”的基因异常,正扮演着愈发关键的“幕后推手”角色。
这场与耐药的赛跑如何才能赢得先机?近日,在2025年欧洲肿瘤内科学会亚洲年会(ESMO Asia 2025)上,一项名为SACHI的研究公布了其关于MET检测一致性的最新分析数据。这一消息并未发布一款革命性新药,却在肿瘤学界激起了巨大波澜。因为它直指当前困境的核心:我们如何才能在耐药的迷雾中,精准地找到那些可以被再次“拯救”的患者?答案,或许就藏在“标准化”这三个字里。
要理解这场斗争的本质,我们必须先认识MET。MET基因编码一种名为c-MET的蛋白,它如同细胞表面的一个“信号接收器”。正常情况下,它在细胞生长、修复中扮演重要角色。但在肿瘤中,这条通路一旦被异常激活,就成了驱动癌细胞疯狂增殖、侵袭和转移的“高速公路”。
在接受EGFR-TKI治疗的肺癌患者体内,当原有的EGFR“主干道”被药物成功阻断后,癌细胞为了生存,会不惜一切代价开辟“旁路”。而MET基因扩增,正是那条最常见、也最凶险的“旁门左道”。数据显示,在第三代EGFR-TKI奥希替尼治疗耐药的患者中,高达20%的元凶是MET扩增。它通过“旁路激活”,绕过被抑制的EGFR通路,重新点燃下游的增长信号,让治疗功亏一篑。
更严峻的是,MET扩增不仅是耐药的驱动者,更是一个强烈的“凶兆”。临床数据显示,无论使用第几代EGFR-TKI,一旦出现MET扩增,患者的无进展生存期(PFS)都将显著缩短。因此,能否在耐药发生时,快速、准确地揪出MET这个“主谋”,成为决定后续治疗成败、扭转患者不良预后的关键第一步。
精准治疗,检测先行。然而,在识别MET扩增的战场上,我们却面临着一座沟通不畅、标准不一的“巴别塔”。目前,临床上有三种主流的检测方法,但每一种都有其难以克服的局限性,导致不同医院、不同研究得出的结论常常无法直接对话。
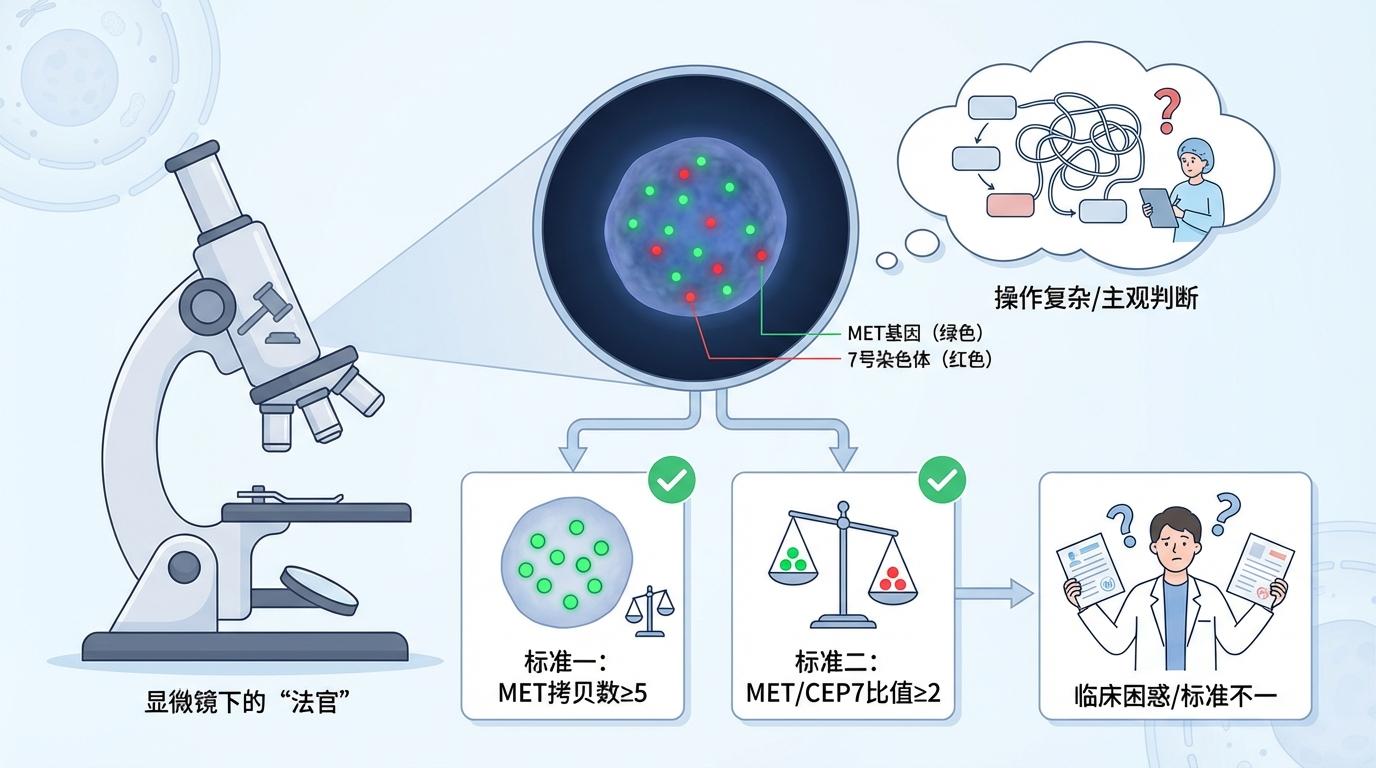
FISH被认为是检测MET扩增的传统“金标准”。它像一位法官,在显微镜下直接清点每个细胞核内MET基因的“物证”(拷贝数)。它直观、可靠,是许多关键临床研究的基石。但这位“老法官”也有烦恼:操作流程复杂,极度依赖检验师的技术和经验,结果判读带有相当的主观性。更重要的是,对于“多少个拷贝才算有罪”(即阳性阈值),业界至今没有统一裁决,有的研究用“基因拷贝数≥5”,有的则看“与7号染色体的比值≥2”,判决标准不一,让临床医生在解读报告时常常感到困惑。
免疫组织化学(IHC):普及的“侦探”,却常常“看走眼” IHC检测的是MET蛋白的表达水平,而非基因本身。它技术普及、成本低廉,像一名深入社区的“侦探”。但这位侦探的工具(抗体)五花八门,记录手法(评分标准)也各不相同。最关键的是,蛋白过表达(影子多)并不完全等同于基因扩增(人多),两者的一致性备受争议,容易造成“冤假错案”。
二代测序(NGS):新兴的“天网”,但需精准“校准” NGS技术如同一张覆盖全城的“天网”,能一次性扫描包括MET在内的数百个基因,提供肿瘤的全景基因图谱,尤其适合探究复杂的耐药机制。然而,这张“天网”的清晰度(准确性)高度依赖于测序深度、算法和阈值设定。近期一项研究甚至发现,与FISH相比,NGS可能漏检约三分之一的MET扩增患者。在组织样本稀缺的情况下,这种漏检是致命的。液体活检(抽血检测ctDNA)虽然便捷,但其灵敏度更低,假阴性率高,权威共识均不推荐单独使用。
正是在这样的背景下,本次ESMO Asia大会上公布的SACHI研究一致性分析,才显得尤为重要。它不啻为一次为NGS这张“天网”进行的关键“校准”。
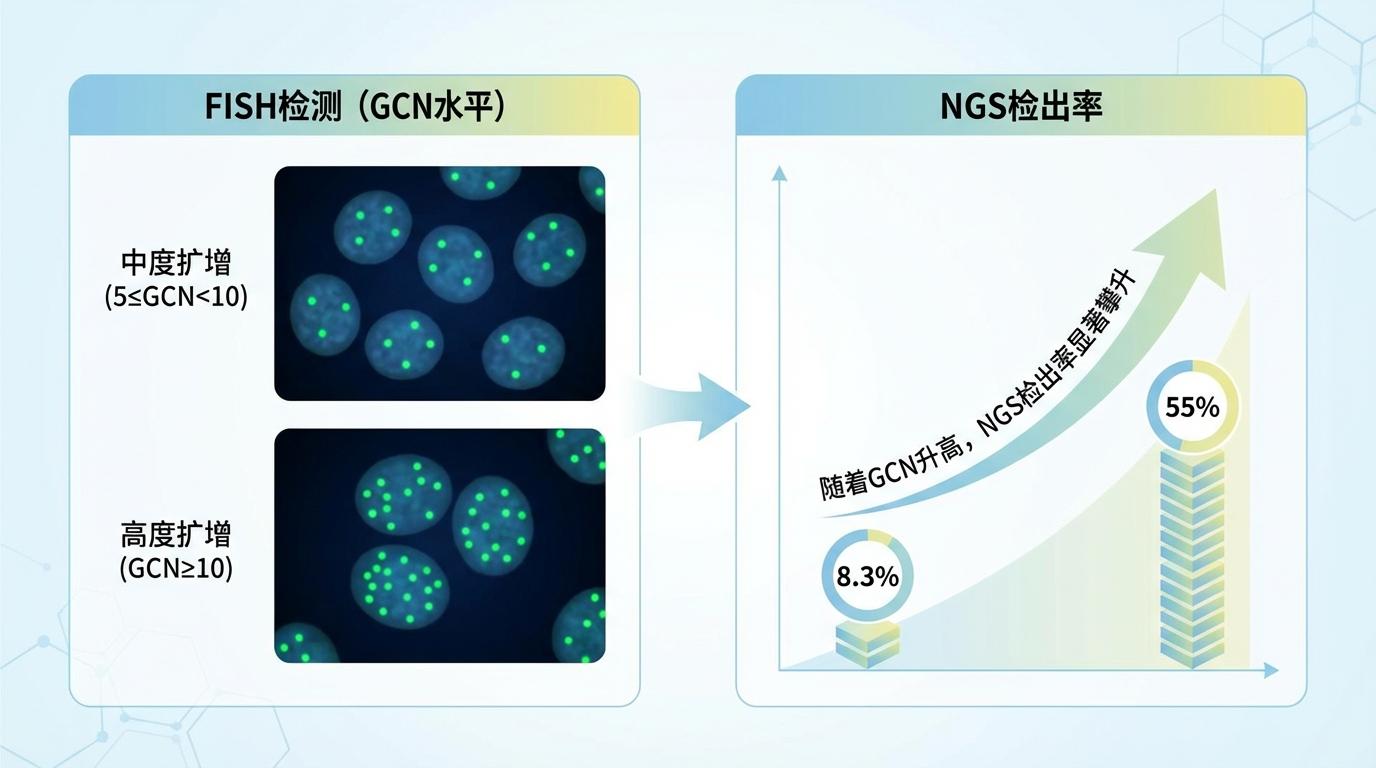
该分析对比了同一批患者中,FISH与NGS两种方法检测MET扩增的结果。数据显示,随着FISH检测到的MET基因拷贝数(GCN)水平的升高,NGS的检出率也显著攀升。 例如,在FISH判定为中度扩增(5≤GCN<10)的患者中,NGS的检出率为8.3%;而在FISH判定为高度扩增(GCN≥10)的患者中,NGS的检出率飙升至55%。
这一发现意义重大。它首次在大型III期临床研究中,清晰地揭示了NGS与“金标准”FISH检测结果之间的内在关联与量效关系。这不仅为NGS应用于MET扩增检测的性能提供了强有力的循证证据,更重要的是,它为未来统一和校准NGS的判读阈值,指明了一条清晰的道路。通过与临床疗效数据结合,未来我们有望为NGS设定一个科学的、能真正筛选出获益人群的“阳性线”,让这张“天网”看得更清、抓得更准。
打破MET检测的“巴别塔”,非一日之功,需要学界、产业界和监管机构的多方协作。
首先,建立全国性的实验室质量控制体系至关重要。通过定期的室间质评,确保各家医院的“法官”和“侦探”都遵循同一套办案规程,让检测报告在不同机构间可以互认。
其次,倡导多平台交叉验证。对于结果处于临界值或存在疑问的样本,鼓励使用另一种方法进行复核,例如NGS提示阳性,可用FISH进行确认,最大程度避免漏诊和误诊。
最后,也是最核心的,是基于大规模临床数据,逆向推导并统一各类检测方法的最佳临床判读阈值。SACHI研究已经迈出了关键一步,未来的方向是结合患者对MET抑制剂的真实治疗反应,为每一种检测方法都找到那个能最大化预测疗效的“甜蜜点”,并将其写入行业共识与指南。
“打捞”每一个可能获益的患者,是精准医疗的终极目标。 在非小细胞肺癌的漫长战役中,攻克EGFR-TKI耐药是决定胜负的关键一役。而推动MET检测的标准化,正是我们在这场战役中部署的最重要的“侦察系统”。唯有建立一个规范、可靠、可及的检测体系,我们才能精准地识别出那些因MET“旁路”而陷入困境的患者,并通过双靶联合治疗,重新为他们封闭癌细胞的“逃生之路”,最终将耐药带来的阴霾,化为生命延续的曙光。