对抗知识焦虑,从看懂这条开始
App 下载
PILRA激活小胶质细胞:阿尔茨海默病治疗新篇章?
加州大学尔湾分校|Denali Therapeutics|阿尔茨海默病|小胶质细胞|PILRA基因|神经退行性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
加州大学尔湾分校|Denali Therapeutics|阿尔茨海默病|小胶质细胞|PILRA基因|神经退行性疾病|医学健康
当记忆的潮水无声退去,当熟悉的容颜变得模糊,阿尔茨海默病(AD)——这个全球老龄化社会面临的巨大挑战,正悄然侵蚀着无数家庭的幸福。尽管近年来抗淀粉样蛋白抗体等疗法相继获批,但其有限的疗效和潜在的副作用,仍在呼唤着更深层次、更具突破性的干预策略。长久以来,我们对大脑的理解如同探索一片浩瀚的星海,而今,一道新的光芒正穿透迷雾,照亮了一个名为PILRA的基因,以及它所调控的大脑“清道夫”——小胶质细胞。这束光能否为阿尔茨海默病的治疗,开辟一条超越传统靶点的全新路径?
近期,来自加州大学尔湾分校与Denali Therapeutics的联合研究团队在《科学-转化医学》(Science Translational Medicine)上发表了一项里程碑式研究,为我们解答这个疑问提供了重要线索。这项研究的核心结论振奋人心:通过调节小胶质细胞中的PILRA通路,有望为阿尔茨海默病的治疗开辟新的途径。研究人员发现,PILRA基因的一种名为G78R的变异体,不仅能显著降低ApoE4携带者患AD的风险,更在健康百岁老人群体中普遍存在。然而,这个“长寿基因”如何发挥保护作用,一直是个未解之谜。这项最新研究正是揭示了PILRA在小胶质细胞功能调控中的关键作用,为未来的AD治疗策略指明了新方向。
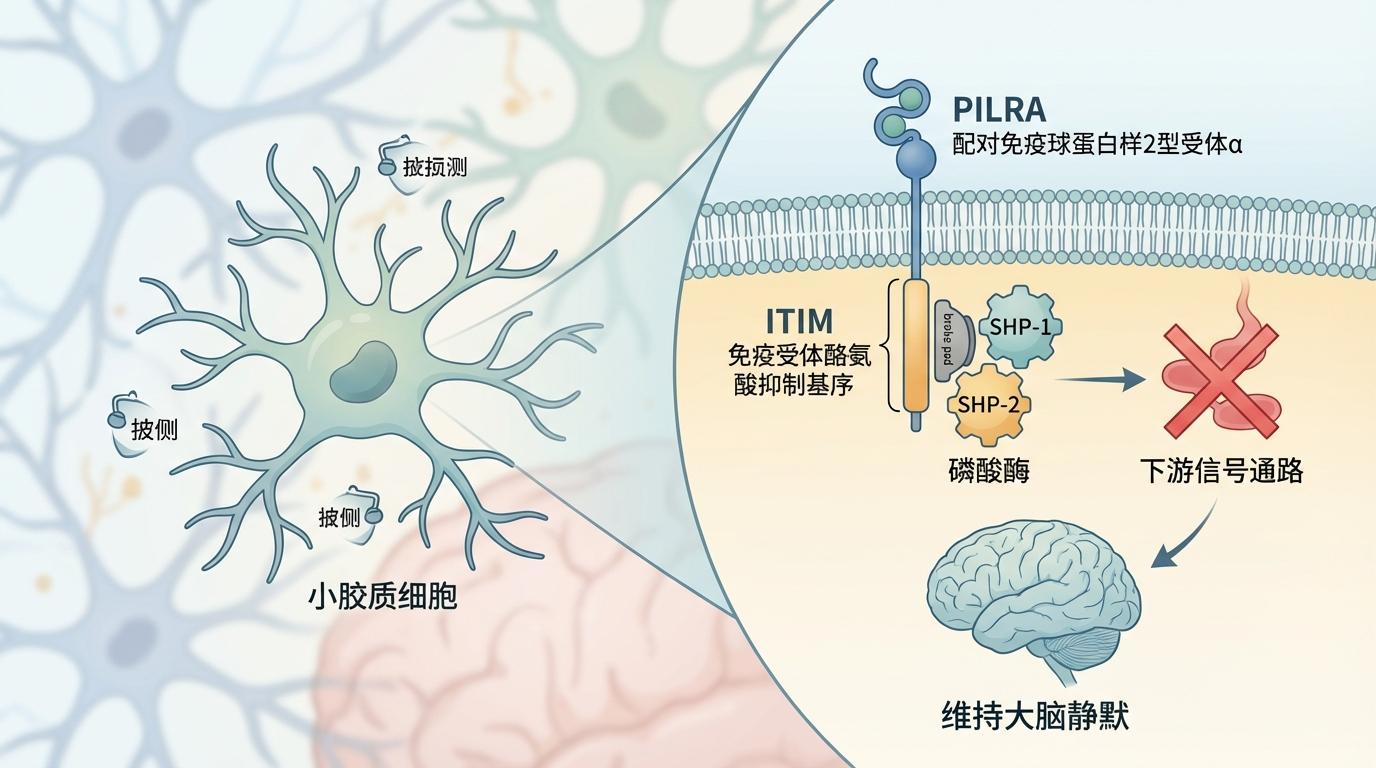
要理解PILRA的魅力,我们首先要认识小胶质细胞。它们是大脑中常驻的免疫细胞,如同忠诚的“哨兵”,时刻巡逻、清除垃圾、抵御病原体,维持着大脑的精妙平衡。然而,在阿尔茨海默病中,这些“哨兵”有时会迷失方向,从保护者转变为“帮凶”,加剧神经炎症和病理进展。而PILRA,全称“配对免疫球蛋白样2型受体α”,正是一种主要表达在小胶质细胞等髓系细胞表面的免疫球蛋白受体。它通过一个被称为“免疫受体酪氨酸抑制基序”(ITIM)的特殊结构传递信号,这个ITIM就像一个“刹车片”,能够招募磷酸酶(如SHP-1/SHP-2)来抑制下游信号通路,从而避免免疫系统过度激活,维持大脑的“静默”。
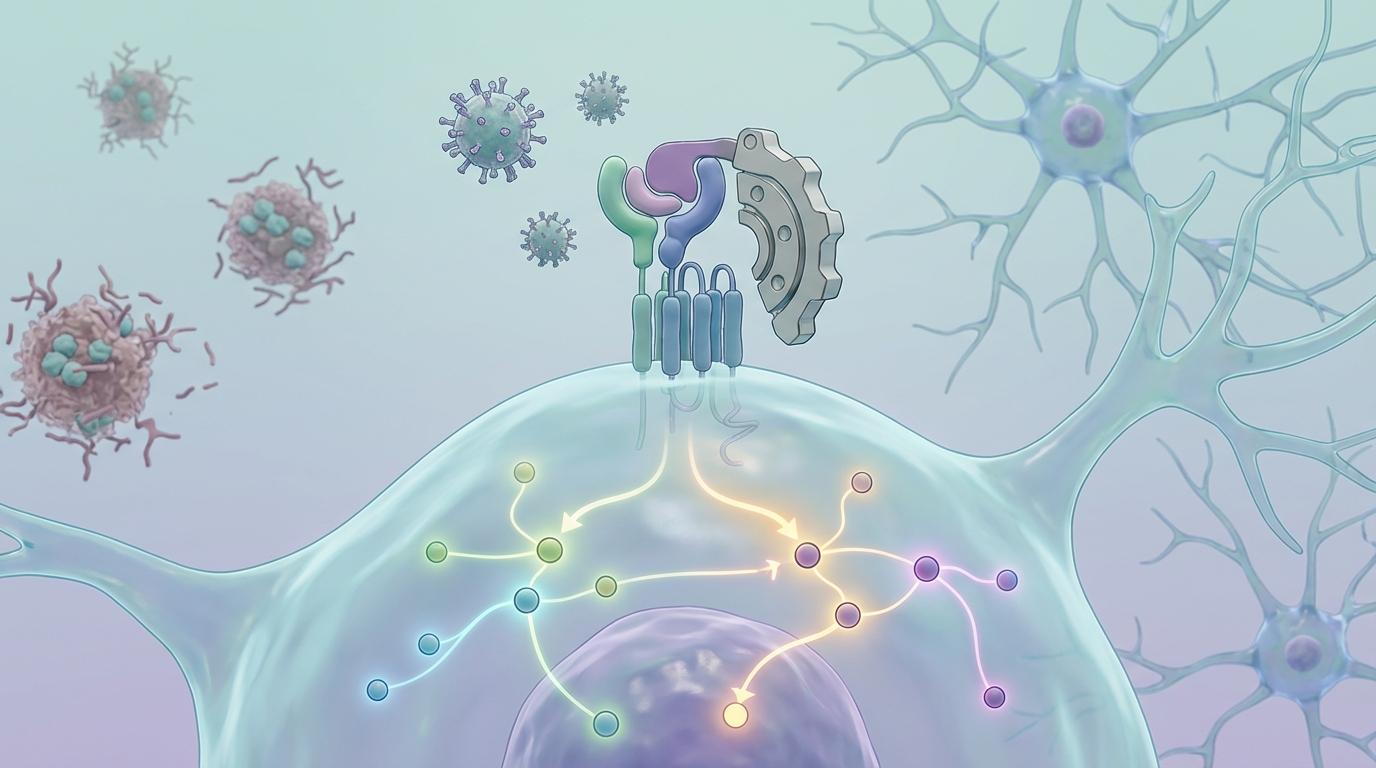
PILRA的G78R变异体之所以具有保护作用,正是因为它改变了PILRA与某些配体的结合,相当于减弱了这个“刹车片”的抑制作用。此外,研究还发现PPAR与STAT1/3信号通路参与了PILRA依赖性小胶质细胞的功能调控。这些复杂的分子机制共同编织了一张精密的网络,决定着小胶质细胞的命运与功能。值得一提的是,PILRA还被发现是单纯疱疹病毒1型(HSV-1)的进入共受体,而HSV-1感染与AD风险之间也存在关联,这暗示了PILRA可能在更广阔的神经免疫疾病中扮演角色。
一个多世纪前,阿洛伊斯·阿尔茨海默医生首次描述了阿尔茨海默病患者大脑中淀粉样蛋白斑块和神经纤维缠结。自那时起,针对这些病理特征的“淀粉样蛋白假说”和“Tau蛋白假说”一直是AD研究的主流。无数科学家前仆后继,试图通过清除淀粉样蛋白或Tau蛋白来治愈疾病。然而,尽管有诸多抗淀粉样蛋白抗体药物获批,其疗效和安全性仍未尽如人意,这促使科学界开始反思,并将目光投向了更广阔的领域,尤其是大脑的免疫系统和脂质代谢。
近年来的遗传学研究不断揭示,许多与AD风险相关的基因,其功能最终都指向小胶质细胞。例如,APOE4作为AD最强的遗传风险因素之一,其存在会显著改变小胶质细胞的功能,损害其清除淀粉样蛋白的能力,并促进炎症。大脑中一半以上的干重由脂质构成,而AD患者大脑中脂质代谢的严重破坏,也日益受到关注。小胶质细胞作为大脑的免疫细胞,在调节脂质代谢和维持血脑屏障稳态方面发挥着至关重要的作用。这种从单一蛋白质靶点向复杂细胞功能和代谢网络转变的范式,预示着AD治疗策略的深远变革,而PILRA正是这场变革中的一个关键棋子。
这项最新研究最令人兴奋之处在于,它详细揭示了PILRA如何通过重塑小胶质细胞的免疫代谢,从而发挥保护作用。研究人员首先在人诱导多能干细胞来源的小胶质细胞(iMG)中敲除PILRA,结果发现,这一操作能够奇迹般地逆转由ApoE4引发的免疫代谢缺陷。缺失PILRA的小胶质细胞仿佛被赋予了新的生命,展现出更为健康的代谢状态:
简而言之,PILRA的缺失让小胶质细胞从一个功能受损、炎症缠身的“疲惫战士”,蜕变为一个充满活力、高效运作的“超级清道夫”,能够更好地清除淀粉样蛋白,维护大脑健康。这种对小胶质细胞“生命之舞”的精准调控,为我们理解和治疗AD打开了一扇全新的大门。
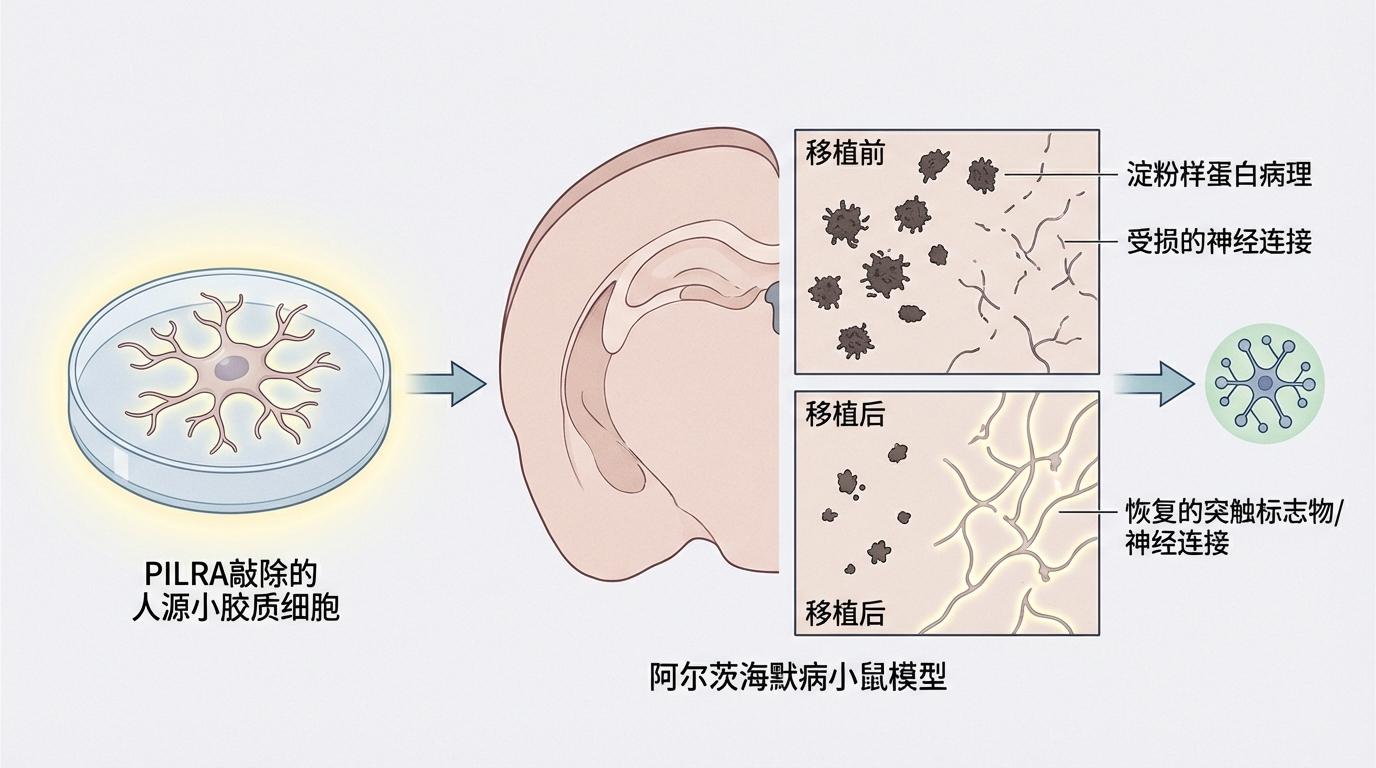
仅仅在细胞层面取得突破还不足以令人信服,真正的希望在于其在动物模型中的验证和药物开发的潜力。研究团队将PILRA敲除的人源小胶质细胞移植到阿尔茨海默病小鼠模型中,结果令人鼓舞:小鼠脑内的淀粉样蛋白病理明显减轻,同时,突触标志物的水平也有所恢复。这表明,调控小胶质细胞中的PILRA通路不仅能改善细胞自身的状态,还能直接影响阿尔茨海默病的核心病理进程,甚至可能修复已经受损的神经连接。
更进一步,研究团队还开发出了一种能够高亲和力阻断PILRA与配体结合的抗体。这种抗体在iMG中成功重现了PILRA敲除后的关键表型,这不仅为PILRA作为药物治疗靶点的潜力提供了强有力的支持,也为未来的药物开发提供了具体的工具。这种抗体能够选择性地结合PILRA的两种变体形式(G78和R78),且不会激活外周免疫细胞,避免了不必要的副作用。它不仅能增强细胞迁移和抗炎基因表达,还能提高细胞呼吸和脂肪酸代谢,从而全面提升小胶质细胞的功能。这意味着,我们或许可以通过一种靶向PILRA的药物,唤醒大脑深处的守护者,让它们重新投入到对抗阿尔茨海默病的战斗中去。
PILRA通路的发现无疑为阿尔茨海默病的治疗带来了新的曙光,但这条道路依然充满挑战。小胶质细胞在AD中的作用是复杂的“双刃剑”,它们既能清除有害物质,也可能在过度激活时释放炎症因子,加剧神经元损伤。因此,未来的干预策略需要极其精细的调控,以避免对小胶质细胞正常生理功能产生不利影响。针对PILRA的干预,需要进一步阐明其在不同AD病理阶段的作用,以及长期使用的安全性、有效性和潜在影响。例如,小胶质细胞的自噬功能、脂质代谢、甚至与血脑屏障的相互作用,都可能受到PILRA调控的影响,需要全面评估。
此外,阿尔茨海默病本身就是一种多因素、多通路的复杂疾病,涉及淀粉样蛋白、Tau蛋白、炎症、脂质代谢、血管损伤等多个环节。PILRA的干预可能只是其中一环,未来或许需要与其他靶点(如TREM2、CD33、HK2、Peli1等)结合,形成多靶点、协同作用的组合疗法。同时,考虑到PILRA G78R变异在不同人群中的频率差异,以及APOE4基因型对治疗响应的影响,未来的治疗可能需要走向个性化和精准化,根据患者的基因背景和疾病阶段制定专属方案。人类对大脑的探索永无止境,每一次的突破都像在浩瀚的宇宙中点亮一颗新的星辰,指引我们前行。
PILRA的发现,标志着阿尔茨海默病研究从“清除垃圾”向“重塑守护者”的深刻转变。它提醒我们,大脑的健康不仅仅依赖于对单一病理蛋白的清除,更在于其内在免疫系统——小胶质细胞的活力与平衡。通过精准调控PILRA通路,我们有望唤醒那些沉睡或功能失调的小胶质细胞,让它们重新成为大脑最忠诚、最强大的守护者。这不仅仅是医学的胜利,更是对生命奥秘更深层次的理解。当记忆不再被无情地抹去,当亲人能再次认出彼此的笑脸,那将是人类智慧与韧性最动人的篇章。这条充满希望的道路,我们才刚刚开始。